- •Лабораторная работа № 2.1 Определение коэффициента Пуассона методом адиабатного расширения и сжатия
- •1.Теоретическая часть
- •1.1 Первый закон термодинамики
- •1.2. Теплоёмкость газа при различных изопроцессах
- •1.3.Адиабатныйпроцесс
- •2.Экспериментальная часть
- •2.1.Цель работы: Определение коэффициента Пуассона для воздуха.
- •2.2.Приборы и принадлежности: сосуд, манометр, резиновая груша.
- •2.3.Экспериментальная установка.
- •2.4. Порядок проведения измерений
- •1.Измерения с нагнетанием воздуха
- •2.Измерения с выпусканием воздуха
- •3.Вывод расчётной формулы
- •4.Обработка результатов измерений
- •Контрольные вопросы
- •Литература
1.3.Адиабатныйпроцесс
Адиабатным называется такой процесс, который протекает без теплообмена с окружающей средой (dQ=0 ).
Теплоёмкость газа, совершающего адиабатный процесс, равна нулю.
Первый закон термодинамики для адиабатного процесса записывается в виде:
|
|
(1.10) |
Тогда
-
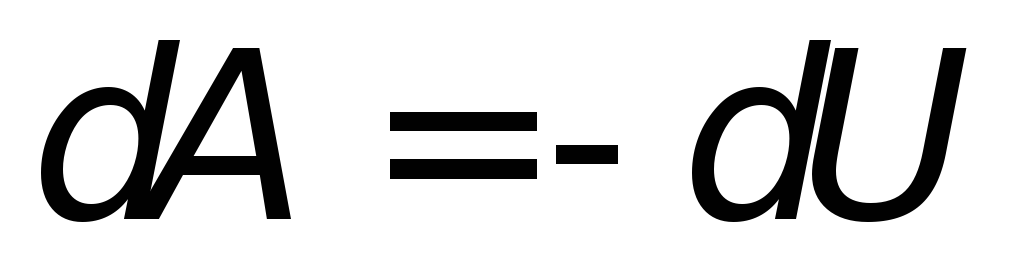 или
или
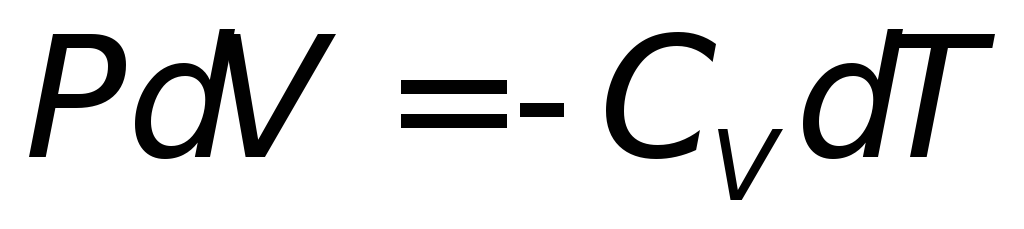
Отсюда видно, что если газ адиабатно расширяется (dV>0), то он совершает положительную работу (dA>0) и, следовательно, dU<0, т.е. газ совершает работу за счёт убыли внутренней энергии системы, что приводит к её охлаждению (dT<0).
Если же газ адиабатно сжимается то dA<0 , dU>0 и dT>0 ,т.е. газ нагревается. На этом основано явление так называемого пневматического огнива, которое находит применение в дизелях, где зажигание горючей смеси осуществляется путем адиабатного сжатия.
При адиабатном процессе изменяются все параметры газа P , V и T. Взаимосвязь между этими параметрами даётся уравнением Пуассона, вывод которого приведём для одного моля идеального газа.
Подставляя в уравнение (1.10) выражения для dA и dU из (1.3) и (1.5), получим:
|
|
(1.11) |
Выразим из уравнения Менделеева-Клапейрона давление P и подставим в (1.11):
Из формулы Майера найдём R и разделим на CV:
|
|
(1.12) |
где =Ср./CV - коэффициент Пуассона.
Проинтегрировав (1.12), получим уравнение Пуассона:
|
|
(1.13) |
Выразив Т из уравнения Менделеева-Клапейрона и подставив в (1.13), получим вторую запись уравнения Пуассона:
|
|
(1.14) | ||
|
|
P Изотерма
Адиабата
V
Рис.1 |
| |
Можно
также показать, что показатель адиабаты
связан с числом степеней свободы* молекул
іследующим
соотношением
![]() .
Из этого следует также, что показатель
адиабаты имеет также верхнюю числовую
границу(
.
Из этого следует также, что показатель
адиабаты имеет также верхнюю числовую
границу(![]() ).
Тогда
).
Тогда
![]()
*)Число степеней свободы – это число независимых координат при помощи которых можно определить положение тела (молекулы).
2.Экспериментальная часть
2.1.Цель работы: Определение коэффициента Пуассона для воздуха.
2.2.Приборы и принадлежности: сосуд, манометр, резиновая груша.
2.3.Экспериментальная установка.
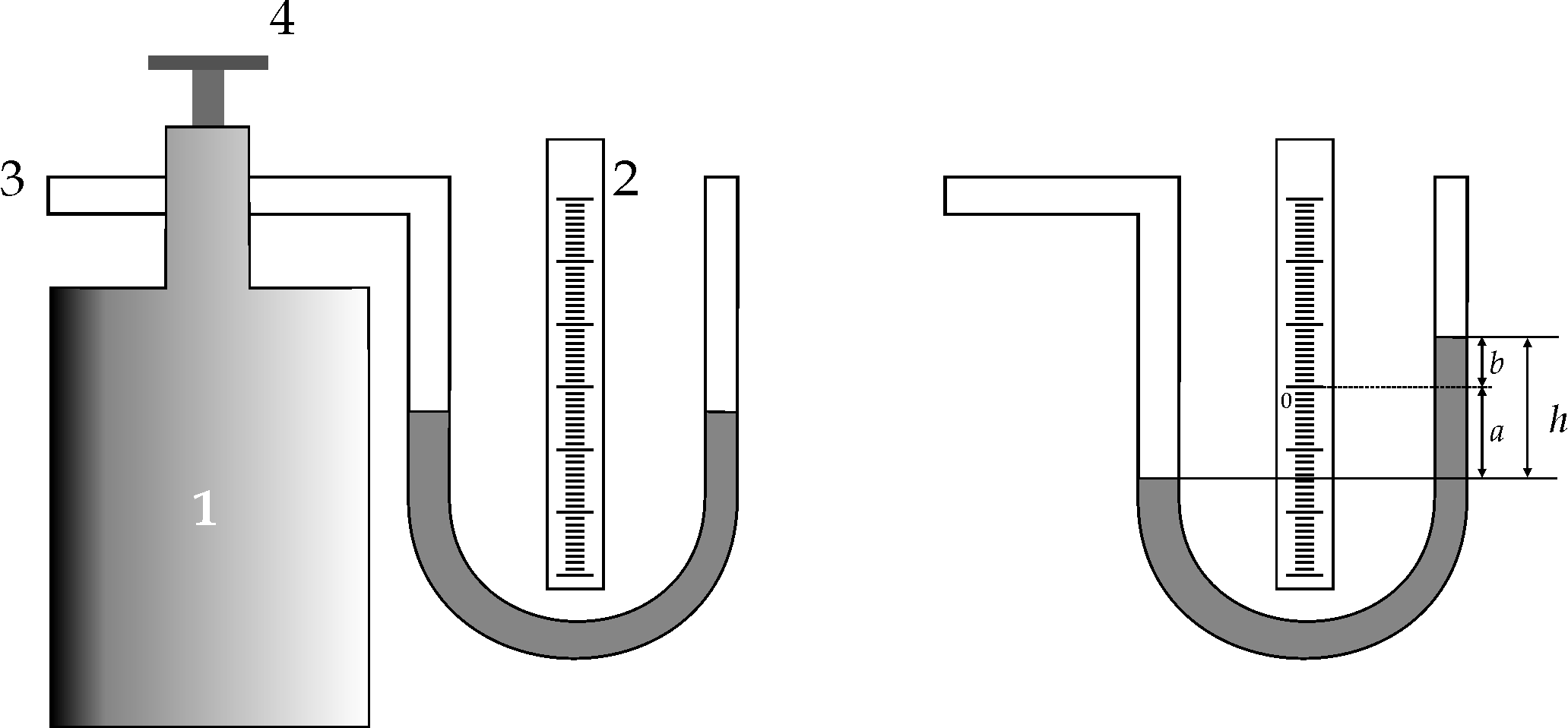
Схема экспериментальной установки показана на рис.2. Сосуд 1 сообщается с окружающим воздухом через патрубок 3. Клапаном 4 регулируют поступление воздуха в сосуд. Давление воздуха в сосуде, избыточное над атмосферным, измеряют жидкостным манометром.
|
| |
|
Рис.2 |
Рис.3 |
Так как уровень манометрической жидкости может не совпадать с нулём шкалы манометра, то при определении давления в сосуде необходимо отсчитывать смещение обоих менисков жидкости
относительно нуля шкалы. Сумма этих двух отсчётов a+b=h (рис.3) даст высоту столба манометрической жидкости, гидростатическое давление которого равно избытку давления в сосуде по сравнению с внешним атмосферным давлением Pa .Таким образом, абсолютное давление газа в сосуде равно сумме атмосферного давления и давления столба жидкости высотой h в манометре.






 Зависимость
P =f(V)
в адиабатном процессе описывается
кривой, называемой адиабатой. В
координатах (P,V)
адиабата идёт круче изотермы (PV=const),
так как показатель адиабаты больше
единицы (
>1) (рис.1)
Зависимость
P =f(V)
в адиабатном процессе описывается
кривой, называемой адиабатой. В
координатах (P,V)
адиабата идёт круче изотермы (PV=const),
так как показатель адиабаты больше
единицы (
>1) (рис.1)