
TITVM_Texty_2[1]
.doc
СОВРЕМЕННЫЕ ПРОБЛЕМЫ ЭНЕРГОРЕСУРСОВ
Существование и развитие человеческого общества на планете характеризуется непрерывным увеличением производства и потребления энергии. Анализ статистических данных говорит о том, что, несмотря на повышение эффективности использования источников энергии, каждые 20 лет производство энергии возрастает вдвое. В этих условиях с полной серьёзностью встаёт вопрос о перспективах в отношении энергоресурсов. В связи с этим рассматриваются невозобновляемые и возобновляемые энергоресурсы.
К невозобновляемым энергоресурсам относятся уголь и его разновидности, нефть, природный газ, сырьё для получения ядерной энергии, то есть такие, запасы которых в результате использования со временем истощаются вплоть до полного исчезновения. По сложившимся на настоящее время взглядам при современной интенсивности добычи запасов нефти может хватить на 80…100 лет, природного газа на 100…200 лет, угля на 300…500лет. В отношении источников ядерной энергии сведения весьма ненадёжны.
К возобновляемым, то есть практически неистощимым энергоресурсам относятся энергия Солнца, ветра, речных и морских течений, океанских приливов, волнения моря, геотермальная энергия.
Все возобновляемые источники требуют для их использования больших капитальных затрат, в частности из-за необходимости строить крупные инженерные сооружения и, как правило, вследствие низкого коэффициента полезного использования энергии. Вряд ли эта область технической деятельности человека в ближайшем будущем подвергнется быстрому и широкомасштабному прогрессу, особенно если учесть малую изученность и отсюда непредсказуемость последствий крупномасштабных технических вмешательств человека в среду его обитания.
На судах морского флота основным источником энергии являются жидкие топлива, получаемые из нефти. Основная тенденция здесь – ухудшение качества топлив и связанное с этим усложнение энергетического оборудования судов. Так, если ещё 20 лет назад допустимое содержание серы (вредный компонент) в топливах составляло 3,5%, то сейчас оно составляет 5% и имеются точки зрения относительно его дальнейшего возрастания. Как следствие повышения трудностей с добычей и переработкой нефти возрастает стоимость нефтепродуктов, например, стоимость дизельного топлива за прошедшие 50 лет возросла в 10 раз. Ухудшение качества топлив требует применения дорогостоящих смазочных масел, которые обеспечили бы длительное и качественное функционирование энергетических установок. Очень сильно возрастают расходы на подготовку топлив к использованию непосредственно на судне. В настоящее время доля эксплуатационных расходов на топливо составляет до 70% от общих эксплуатационных расходов по судну. В этих условиях главная задача состоит в разработке и применении мер, направленных на экономичное использование энергетических ресурсов.
ПОЛУЧЕНИЕ ТОПЛИВ И МАСЕЛ
Все отдельные продукты, получаемые из нефти, мы будем в дальнейшем обобщённо называть нефтепродуктами. Известны следующие основные способы получения топлив.
Способ прямой перегонки. Исходная нефть подвергается нагреванию, в процессе которого отдельные её фракции испаряются и после отбора паров последние конденсируются. Процессы испарения могут вестись при атмосферном давлении и под вакуумом в атмосферных и атмосферно-вакуумных установках. При температурах конденсации до приблизительно 150°С происходит отбор бензинов, до приблизительно 250 - 300°С получают керосины, до приблизительно 350°С отгоняются дизельные топлива. Эти нефтепродукты называют дистиллятами. Оставшиеся продукты, называемые остаточными, могут быть использованы частично для получения смазочных масел.
Второй способ – переработка остаточных продуктов путём крекинга. При этом молекулы фракций с большой молекулярной массой, оставшиеся после отбора дистиллятов, разрушаются на более мелкие. В результате отбираются крекинг-бензины и мазуты. Окончательные остатки представляют собой гудрон.
Используют две разновидности крекинга: термический и каталитический. При термическом крекинге процесс ведётся при температуре около 500…550°С и давлении 5…6 МПа. Каталитический крекинг происходит при температурах 500…550°С, давлении, близком к атмосферному, и в присутствии катализаторов, в качестве которых применяются чаще всего алюмосиликаты – соединения окислов алюминия и кремния.
Третий способ – гидрогенизация, заключается в обработке (насыщении) водородом исходных продуктов (нефтяных остатков, углей и углесодержащих твёрдых продуктов) при температурах 450…500°С и давлениях 20…70 МПа в присутствии катализаторов (хром, магний, никель, цинк). Как будет показано дальше, водород является весьма ценным компонентом топлива, повышающим его энергетическую ценность.
Четвёртый способ – синтин-процесс. При этом в условиях высоких температур и давлений из простейших веществ СО и Н2 получаются жидкие нефтепродукты из исходных газообразных. Эти процессы также протекают при высоких температурах и давлениях в присутствии катализаторов. Синтетическое топливо характеризуется высоким цетановым числом (80…100), в таких топливах практически отсутствуют сера, зола и вода.
Наиболее распространены первые два способа.
Сырьём для производства масел служит неиспарившийся остаток прямой перегонки нефти – мазут, полугудрон и гудрон. Производство масел осуществляется на атмосферно-вакуумных установках. Полученные масляные фракции очищают от смолы, нафтеновых кислот, сернистых соединений, используя для этого отбеливающие земли, серную кислоту, щёлочь, особые растворители. Для повышения качества масел в них добавляют специальные присадки.
ЭЛЕМЕНТНЫЙ И ФРАКЦИОННЫЙ СОСТАВ ТОПЛИВ
Элементный состав и горение топлива
По своему основному химическому составу топлива представляют собою углеводороды, то есть соединения углерода с водородом. В относительно заметных количествах в них присутствует сера, в небольших – кислород и некоторые другие элементы (азот, натрий, ванадий, алюминий, кремний). В топливах, хранящихся на судне, может присутствовать вода (иногда до 2%).
Примерное содержание в топливах: углерода – 84…87%, водорода – 11…13%, серы – до 5%, кислорода – 0,4…0,6%.
Горючими веществами являются углерод, водород и сера.
В процессе подготовки к сжиганию и сжигании жидкое топливо проходит следующие фазы:
1. Дробление струй топлива на капли размером 10…50 мкм (распыливание).
2. Испарение капель топлива в камере сгорания при высокой температуре.
3. Перемешивание паров топлива с воздухом и создание горючей смеси.
4. Воспламенение горючей смеси. В установках непрерывного сжигания (топки паровых котлов, камеры сгорания газовых турбин) оно происходит от уже горящего факела, в карбюраторных двигателях – от искры, в дизелях – самовоспламенение под действием высокой температуры в конце процесса сжатия воздушного заряда.
5. Собственно горение, то есть соединение горючих веществ с кислородом. При этом повышается температура среды и увеличивается интенсивность испарения распыливаемого топлива.
При полном сгорании горючих компонентов топлива протекают следующие реакции (в нижеприведенных термохимических уравнениях символы и формулы означают килограмм-атомы или килограмм-молекулы).
Сгорание углерода:
С + О2 = СО2 + 393000 кДж.
Сгорание водорода (с учётом конденсации паров воды):
2Н2 + О2 = 2Н2О + 490000 кДж.
Сгорание серы:
S + O2 = SO2 + 294500 кДж.
2S + 3О2 = 2SО3 + 781600 кДж.
При пересчёте на килограмм сгорающего элемента получаем:
- для углерода – 393000/12 = 32750 кДж;
-
для водорода – 490000/4 = 122500 кДж;
-
для серы при сгорании в SO2 – 294500/32 = 9200 кДж;
- для серы при сгорании в SO3 – 781600/64 = 12200 кДж.
Отсюда видно, что наиболее энергетически ценным в топливе является водород, наименее – сера.
Таким образом, в продуктах сгорания топлив содержатся углекислый газ, вода и серный ангидрид. При неполном сгорании присутствуют угарный газ СО и сернистый ангидрид SО2.
Фракционный состав топлив
Углеводороды, входящие в состав топлив, различаются по количеству входящих в их молекулы атомов и по способам соединения атомов. Различают следующие три основные группы углеводородов.
1. Алифатические. 2. Нафтеновые. 3. Ароматические.
В нефтях различного происхождения соотношение этих компонентов различно. В зависимости от того, какая группа превалирует в той или иной нефти, исходные нефти получают название. Рассмотрим подробно каждую из групп.
Алифатические углеводороды в свою очередь делятся на три подгруппы.
1. Парафины, или алканы. Это предельные углеводороды, имеющие общую формулу СnН2n+2. Молекулы их содержат незамкнутые цепи из атомов углерода, соединённых между собой единичными связями. Простейшим из них является метан СН4 :
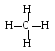
Д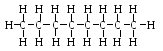 ругой
пример – октан С8Н18 :
ругой
пример – октан С8Н18 :
При атмосферных условиях парафины с числом атомов водорода до 4 – газы, остальные – жидкие или твёрдые вещества. В так называемом петролейном эфире содержатся углеводороды от С5Н12 до С7Н16 , в бензине – от С7Н16 до С9Н20 , в керосине – от С10Н22 до С16Н34 . Дизельные топлива также представляют собой смеси либо растворы углеводородов. Некоторые из них содержат до 20 атомов углерода в молекуле. Ещё более тяжелые углеводороды содержатся в смазочных маслах, мазутах, вазелине и парафине.
С увеличением числа атомов в молекулах предельных углеводородов возникает ещё одна качественная особенность – появление всё большего числа изомеров, имеющих разветвлённые углеродные цепи. Метан СН4 , этан С2Н6 и пропан С3Н8 изомеров не имеют, пентан С5Н12 имеет три изомера, а формулу С14Н30 могут иметь уже 1818 различных углеводородов.
2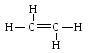 .
Олефины (алкены). Общая формула для них
- СnН2n . В составе их цепей
имеются атомы водорода, соединённые
двойными связями. Простейший из олефинов
– этилен С2Н4 :
.
Олефины (алкены). Общая формула для них
- СnН2n . В составе их цепей
имеются атомы водорода, соединённые
двойными связями. Простейший из олефинов
– этилен С2Н4 :
3. Ацетилены (алкины), имеющие общую формулу СnН2n – 2. Имеют тройные связи между атомами углерода. Простейший из них – собственно ацетилен С2Н2 :
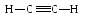
Нафтеновым углеводородам свойственно наличие замкнутых колец из атомов углерода. Типичным представителем таких углеводородов является циклопентан С5Н10 :
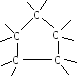
Здесь и далее для упрощения структурной схемы на концах внешних связей подразумевается наличие не показанных атомов водорода.
Ароматические углеводороды характеризуются наличием замкнутых структур типа бензольного кольца. Типичным их представителем является бензол С6Н6 :
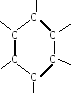
При подготовке к горению молекулы претерпевают разложение на атомы, причём разложение кольцевых структур, особенно бензольного типа, происходит при температурах, более высоких, чем цепных. С этой точки зрения нефти парафинового происхождения более приемлемы, тем более, что они имеют бóльшую энергетическую ценность (бόльшую теплоту сгорания).
ФИЗИКО-ХИМИЧЕСКИЕ ПОКАЗАТЕЛИ ТОПЛИВ
1. Плотность ρ, [кг/м3]. Для различных топлив она варьирует в диапазоне от 700 до 1015. Меньшие значения относятся к бензинам, бóльшие – к мазутам. Именно отсюда происходят термины "лёгкие" и "тяжёлые" топлива. Плотность дизельных топлив составляет 830…860 кг/м3.
Плотность топлив заметно изменяется с изменением температуры, понижаясь с повышением последней. Для пересчёта плотности ρ1 при температуре Т1 на плотность ρ2 при температуре Т2 пользуются формулой
![]() ,
,
где у – температурный коэффициент плотности, определяемый по таблицам в зависимости от плотности. На основании статистической обработки данных фирмы Шелл автором получено приблизительное выражение для коэффициента у:
у = 0,95 – 0,0003ρ1 ,
с хорошей точностью описывающее свойства топлив в реальном диапазоне плотностей.
2. Вязкость. Существуют понятия динамической и кинематической вязкости. Динамическая вязкость μ [Па*с] характеризует внутреннее трение в жидкости и её единица представляет собою силу взаимодействия между двумя параллельными слоями топлива, каждый площадью 1м2, находящимися на расстоянии 1м один от другого и движущимися один относительно другого со скоростью 1м/с. Кинематическая вязкость ν[м2/с] представляет собой отношение динамической вязкости к плотности
![]() .
.
В судовой практике понятие динамической вязкости используется редко. Вследствие неудобства использования слишком большой единицы измерения [м2/с] для кинематической вязкости используются такие единицы, как стокс,
1Ст = 1*10-4 м2/с
и чаще сантистокс,
1сСт = 1*10-6 м2/с.
Помимо указанных единиц измерения, вязкость выражают в условных единицах, таких, как градусы Энглера. Эта единица распространена на европейском континенте. Вязкость в градусах Энглера [°Е] (у нас часто именуется "вязкость условная", [°ВУ]) представляет собою отношение времени истечения 200мл топлива при температуре измерения к времени истечения 200мл воды при 20°С на приборе Энглера. Отметим, что вода при температуре 20°С имеет вязкость 1сСт.
В Великобритании пользуются такой единицей, как секунды Редвуда [с R-1] – это время истечения в секундах 50мл топлива на приборе Редвуда при 100 по Фаренгейту (37,8°С). На американском континенте распространена единица измерения секунда Сейболта [с Su]. Вязкость в секундах Сейболта – это время истечения 60мл топлива на приборе Сейболта при 20°С.
Вязкость зависит от температуры, понижаясь с повышением последней. Известна следующая эмпирическая формула, выражающая температурно-вязкостную зависимость:
lg lg (ν + 0.8) = A – B lgT,
где ν – кинематическая вязкость, Ст;
Т – температура топлива, °С;
А и В – коэффициенты, характерные для данного топлива.
Диаграммы температурно-вязкостной зависимости строятся обычно таким образом, что неравномерный масштаб по оси вязкости позволяет представить температурно-вязкостную зависимость топлив в виде прямых, многие из которых практически параллельны (рис. 1). Линии более вязких топлив располагаются выше. С помощью такой диаграммы можно определить температуру, до которой следует греть топливо для обеспечения необходимой вязкости. Предположим, что нам известна вязкость некоторого топлива ν1 при температуре Т1. Проведя соответствующие линии на диаграмме, получим точку температурно-вязкостной зависимости этого топлива А. Через эту точку проведём линию температурно-вязкостной зависимости данного топлива как параллельную имеющейся на диаграмме линии С – С какого-нибудь другого топлива. Проведя теперь горизонталь через отметку ν2 требуемой вязкости до пересечения с линией нашего топлива в точке В и опустив из точки В перпендикуляр на ось абсцисс, получим требуемую температуру подогрева Т2 .
Пересчёт вязкости, выраженной в одних единицах, в другие может быть выполнен опять-таки с помощью диаграммы либо, более точно, с помощью специальных таблиц, имеющихся во многих литературных источниках по рассматриваемому вопросу.
Как правило, при одинаковых температурах топлива более высокой плотности имеют более высокую вязкость.

Рис. 1. Определение температуры подогрева топлива.
3. Теплота сгорания
[кДж/кг] – это количество теплоты,
выделяющееся при полном сгорании 1
килограмма топлива. Различают два
понятия теплоты сгорания: высшая рабочая
![]() и низшая рабочая теплота сгорания
и низшая рабочая теплота сгорания
![]() .
Высшая рабочая теплота сгорания – это
количество теплоты, выделившееся при
сгорании топлива с учётом теплоты
конденсации паров воды из продуктов
сгорания. Низшая рабочая теплота сгорания
– это количество теплоты за вычетом
теплоты конденсации паров воды. Поскольку
температура уходящих газов для всех
механизмов, преобразующих энергию
топлива в теплоту, выше температуры
конденсации паров воды, во всех расчётах
используется понятие низшей рабочей
теплоты сгорания.
.
Высшая рабочая теплота сгорания – это
количество теплоты, выделившееся при
сгорании топлива с учётом теплоты
конденсации паров воды из продуктов
сгорания. Низшая рабочая теплота сгорания
– это количество теплоты за вычетом
теплоты конденсации паров воды. Поскольку
температура уходящих газов для всех
механизмов, преобразующих энергию
топлива в теплоту, выше температуры
конденсации паров воды, во всех расчётах
используется понятие низшей рабочей
теплоты сгорания.
Высшая и низшая рабочая теплота сгорания с хорошей точностью могут быть вычислены по формулам Д. И. Менделеева:
![]() ;
;
![]() .
.
В этих формулах С, Н, S, О, W – процентное содержание в топливе по массе соответственно углерода, водорода, серы, кислорода и воды.
Формулы приведены с использованием старых единиц теплоты, автор данного пособия этим отдаёт должное простоте и изяществу их вида. Напомним, что
1ккал = 4,187 кДж.
Как следует из приведенных формул, наиболее энергетически ценным компонентом топлива является водород, наименее ценным – сера. Низшая рабочая теплота сгорания для жидких топлив составляет от 43000 кДж/кг (бензины, керосины) до 39000 кДж/кг (высокосернистые обводнённые мазуты).
Низшая рабочая теплота сгорания может быть также вычислена по формуле Standard ISO 8217 (в МДж/кг):
![]() ,
,
где ρ – плотность топлива при 15°С, S, Y, W – содержание в процентах по массе соответственно серы, золы и воды.
Как следует из формул Менделеева, наличие кислорода в топливе снижает его энергетическую ценность. Так, например, этиловый спирт С2Н6О вследствие содержания кислорода почти 35% по массе имеет низшую рабочую теплоту сгорания всего 27500 кДж/кг, то есть в полтора раза меньше, чем у дизельного топлива (около 42000 кДж/кг).
При нормативных
расчётах двигателей внутреннего сгорания
в качестве топлива принимается дизельное,
имеющее
![]() кДж/кг, и расчёты удельных расходов
топлива ведутся именно на такую теплоту
сгорания.
кДж/кг, и расчёты удельных расходов
топлива ведутся именно на такую теплоту
сгорания.
Температурные показатели.
4. Температура вспышки – это такая наинизшая температура, при которой пары топлива в смеси с воздухом вспыхивают при контакте с открытым огнём. Есть два способа измерения температуры вспышки: в открытом и в закрытом сосуде. Во втором случае она выше, чем в первом, на 10…15 градусов. В судовой технике употребляется первый способ.
5. Температура воспламенения - наинизшая температура, при которой пары топлива в смеси с воздухом вспыхивают и горение продолжается на поверхности не менее 5 секунд. Она выше температуры вспышки на 10…15 градусов.
6. Температура помутнения – наивысшая температура, при которой в топливе начинается выпадение кристаллов парафина, при более высоких температурах растворённого в более лёгких фракциях. Топливо при этом мутнеет.
7. Температура застывания - наивысшая температура, при которой топливо теряет подвижность. Критерий потери подвижности – топливо, налитое в пробирку, после наклона пробирки на 45° не изменяет положения своей верхней границы в течение одной минуты.
8. Сера в топливе – попадает в топливо из исходной нефти. Содержание серы в дизельных топливах по стандартам СНГ не более 0,5%, в мазутах – не более 3,5%, по стандартам ISO (международная организация по стандартизации) – до 5%.
9. Вода в топливе – попадает в топливо при хранении и транспортировке (конденсация из атмосферы на стенках цистерн и трубопроводов, случайные протечки, использование для разогрева топлива прямого пропускания пара). В дистиллятных топливах не допускается, в мазутах – не более 1%, а если для разогрева топлива используется прямое пропускание пара – до 2%.
10. Механические примеси в топливе имеют неорганическое и органическое происхождение. К неорганическим относятся ржавчина, песок, глина, которые могут попадать в топливо извне. К органическим – карбены и карбоиды, это твёрдые частицы, образующиеся в процессе переработки нефти.
11. Кокс – остаток после нагревания топлива без доступа воздуха. Определяется на приборе Конрадсона. В дистиллятных топливах допускаются доли процента, в мазутах по стандартам СНГ не более 10%, по стандартам ISO – до 22%.
12. Зола – остаток после сжигания топлива. Включает в себя различного рода неорганические примеси (песок, глина, ржавчина). В дистиллятных топливах допускается содержание золы до 0,01%, в мазутах не более 0,2%.
13. Алюминий и кремний – попадают в топливо в процессе каталитического крекинга.
14. Натрий и ванадий. Натрий попадает в топливо из морской атмосферы, ванадий – из исходной нефти.
15. Цетановое число. Применяется только для дистиллятных топлив. Характеризует время задержки самовоспламенения топлива в камере сгорания дизеля. Определяется как процентное содержание цетана С16 Н34 в смеси с альфаметилнафталином С11Н10, когда в эксперименте на опытном двигателе подобранная смесь имеет такое же время задержки самовоспламенения, как и испытуемое топливо.
ВЛИЯНИЕ ФИЗИКО-ХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ТОПЛИВ
НА РАБОТУ ДВИГАТЕЛЕЙ
1. Плотность – на работу двигателей влияния не оказывает, однако она должна учитываться при операциях приёмки – сдачи топлива, поскольку количество принятого топлива измеряется в единицах объёма, а оплата за него осуществляется по массе. Плотность топлива играет большую роль при настройке топливных сепараторов. Чем ближе плотность топлива к плотности воды, тем более затруднительна сепарация. В подобных случаях следует вести сепарацию при подаче сепараторов, составляющей половину, а то и треть от номинальной подачи, указанной в паспорте сепаратора.
2. Вязкость играет большую роль в работе двигателя. Существует некоторый диапазон оптимальных вязкостей топлива, подаваемого форсункой, при которых полнота сгорания топлива наибольшая. Этот диапазон составляет 2…2,5°Е. В ряде случаев для достижения такой вязкости необходимо греть топливо до 150…160°С. Существование такого диапазона можно объяснить следующим.
Если топливо слишком вязкое, то в камере сгорания оно распыливается относительно крупными каплями. Капля испаряется и горит снаружи, внутри капли воздуха не хватает, и это является причиной неполноты сгорания, то есть снижения к.п.д. двигателя. Кроме того, крупные капли летят далеко, оседают и коксуются на стенках камеры сгорания и в канавках поршневых колец. Это приводит к потере кольцами подвижности, увеличению пропусков газов в полости под поршнем, повышает вероятность задира втулки цилиндра.
Если топливо маловязкое, оно распыливается облаком вблизи форсунки. Это облако горит снаружи, где произошло достаточно хорошее перемешивание топлива с воздухом, внутри же облака воздуха не хватает, и вновь имеет место неполнота сгорания и снижение к.п.д. Кроме того, топливо коксуется на распылителях форсунок, что может привести к прекращению подачи форсункой топлива.
3. Теплота сгорания. Чем выше теплота сгорания топлива, тем выше его энергетическая ценность и тем меньше его нужно для получения необходимой мощности. Удельный эффективный расход топлива bе определяется по формуле
![]() ,
,
где ηe – эффективный к.п.д. двигателя, на который теплота сгорания практически не влияет.
4 и 5. Температура вспышки и температура воспламенения характеризуют пожарную опасность топлива. На судах морского флота допускается использование топлив с температурой вспышки не ниже 61°С, за исключением топлив для аварийных дизельгенераторов, где допускается температура вспышки не ниже 43°С (по соображениям повышения надёжности запуска). В открытых цистернах топливо должно храниться при температуре по меньшей мере на 15° ниже температуры вспышки, но не выше 90°С во избежание местного перегрева и выброса топлива с парами воды.
6. Температура помутнения. Кристаллы парафина, выделяющиеся в топливе, забивают топливные трубопроводы и фильтры, что влечёт за собой прекращение подачи топлива и остановку двигателя.
7. Температура застывания. При этой температуре затрудняется перекачка топлива и, хотя она ещё возможна, возрастает нагрузка на электроприводы топливоперекачивающих насосов. Если топливо имеет температуру застывания выше -5°С, то ёмкости, в которых оно хранится, должны иметь систему подогрева, расположенную по всей площади дна цистерны, а не только подогревающие устройства в районе приёма топлива к насосам. Следует отметить, что топлива с высокими температурами застывания часто имеют хорошие характеристики сгорания, что объясняется хорошим качеством сгорания превалирующих в них парафинов.
