
- •Лекція № 2. Білки
- •Загальна характеристика та функції білків
- •Амінокислоти
- •Пептиди
- •Класифікація білків
- •Прості білки
- •Складні білки
- •Амінокислотний склад рослинних білків
- •Проблема харчового білка та шляхи її вирішення
- •Загальні шляхи синтезу амінокислот
- •Утворення амінокислот при фотосинтезі
- •Утворення амінів
- •Метилювання амінокислот
- •Пул вільних амінокислот та їхня роль у рослині
- •Біосинтез білка
- •Література:
Загальні шляхи синтезу амінокислот
Таких шляхів два – пряме амінування кетокислот і переамінування. Ці процеси подібні у рослин і тварин.
При прямому амінуванні аміак приєднується до кетокислоти за участю відновлювача NАDРН і при виділенні води. Реакцію каталізує відповідна дегідрогеназа.

Цю реакцію каталізує аланіндегідрогеназа.
У рослин, крім кетокислот, прямому амінуванню може піддаватися фумарова кислота під дією аспартат-аміак-ліази, що активується Са2+.
При переамінуванні відбувається перенесення аміногрупи з амінокислоти на кетокислоту, в результаті утворюються нові амінокислота і кетокислота. Реакція відбувається під дією амінотрансфераз, простетичною групою яких є похідне вітаміну В6 – фосфопіридоксаль.
Найактивнішу участь у переамінуванні беруть дикарбонові амінокислоти – аспарагінова і глутамінова та їхні аміди.


Утворення амінокислот при фотосинтезі
Амінокислоти, поряд із вуглеводами, є продуктами фотосинтезу. У процесі фотосинтезу утворюються 5 амінокислот: серин, аланін, цистеїн, гліцин, аспарагінова кислота.
Безпосередньо з 3-ФГК утворюються серин і аланін. Із серину шляхом заміщення -ОН групою –SН виникає цистеїн.

У С4-шляху після карбоксилювання фосфоенолпірувату (ФЕП) утворюється щавлевооцтова кислота (ЩОК), яка в результаті переамінування дає аспарагінову кислоту.

У процесі фотодихання з гліоксилевої кислоти при переамінуванні утворюється гліцин.

Із амінокислот, що виникають при фотосинтезі, можуть утворюватися інші амінокислоти як шляхом їх перетворення, так і шляхом переамінування.
Механізми знешкодження аміаку
Вихідною речовиною для синтезу азотистих сполук у рослинах є аміак. Він надходить у рослину з ґрунту, утворюється при відновленні NO3– і при розпаді білків та амінокислот. Однак вільний аміак отруйний і зазвичай міститься в рослинах у невеликій кількості. Рослина змушена знешкоджувати аміак, не допускаючи його накопичення.
Існує ряд механізмів знешкодження аміаку в рослинах. Основні з них три: утворення амідів, сечовини та амонійних солей.
Утворення і роль амідів у рослині
Аміди синтезуються з аспарагінової і глутамінової кислот шляхом приєднання молекули аміаку. Реакції каталізують аспарагін- і глутамінсинтетаза відповідно. У реакції бере участь АТР, тому що для утворення C-N-зв'язку потрібна енергія. Синтетази активуються іонами Mg2+.
Таким чином, кожна молекула дикарбонової амінокислоти може зв'язати і знешкодити одну молекулу аміаку. Аміди можуть накопичуватися у великих кількостях. Особливо багато їх утворюється при проростанні насіння бобових у темноті, коли відбувається інтенсивний розпад запасних білків і утворюється велика кількість аміаку. До того ж у темноті через нестачу вуглеводів знижується використання NH3 у синтезі амінокислот.
Аміди відіграють у метаболізмі рослин дуже важливу роль:
1) утворюють механізм знешкодження аміаку в рослині;
-
як і дикарбонові амінокислоти, беруть активну участь у переамінуванні, віддаючи амідну групу не тільки на утворення амінокислот, але й інших сполук (глюкозамін, азотисті основи та ін.);
-
складають резерв дикарбонових амінокислот, яким належить значна роль в азотному обміні;
-
входять до складу багатьох рослинних білків;
-
утворюють транспортну і запасну форми азоту.

Утворення сечовини
Сечовина – нешкідлива для рослин сполука, що може накопичуватися в певній кількості, особливо в рослинах, які мають на коренях мікоризу. Використовується сечовина, що розкладається із виділенням аміаку під дією ферменту уреази.

Молекула сечовини знешкоджує 2 молекули аміаку. Утворення її відбувається в результаті кількох ферментативных реакцій, що складають орнітиновий цикл. Цей цикл у рослин ідентичний тваринному, що вивчається у курсі загальної біохімії.
Утворення амонійних солей
Простіше знешкоджується аміак у так званих «кислих» рослин. Це рослини з кислим клітинним соком (рН 1,2-1,5), що містить багато органічних кислот (щавлева, яблучна, ізолимонна та і 11.) – щавель, ревінь, осоки, хвощі, бегонія тощо. У таких рослин аміак зв'язується не ферментативним, а хімічним шляхом у вигляді амонійних солей.
Це дуже ємний механізм. «Кислі» рослини витримують у 4-5 разів більш високий вміст аміаку, ніж рослини, у яких рН клітинного соку близький до нейтрального.

Загальні шляхи розпаду амінокислот
Таких шляхів два – дезамінування і декарбоксилювання. Дезамінування – це розпад амінокислот до аміаку і кетокислот.

Реакція відбувається в два етапи: на першому від амінокислоти відщеплюються два атоми водню й утворюється імінокислота, на другому – під дією води з імінокислоти утворюється кетокислота і видаляється аміак.
У рослинах реакції першого етапу відбуваються інакше, ніж у тваринних організмів. У них беруть участь два ферменти – дегідрогеназа і поліфенолоксидаза, а також поліфеноли і хінони, здатні взаємно перетворюватися. Етап перетворення амінокислоти в імінокислоту можна подати у вигляді наступної схеми.
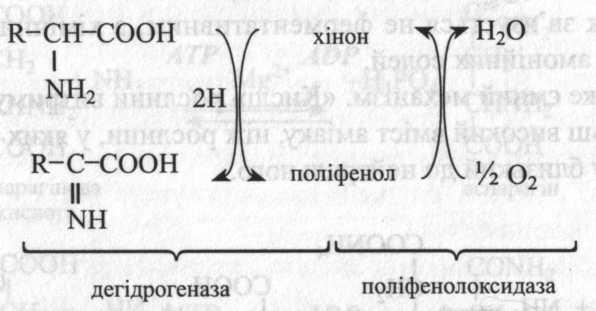
Перетворення хінонів у поліфеноли можна уявити так:

У рослинах дезамінування фенілаланіну і тирозину відбувається інакше, ніж інших амінокислот, з утворенням ненасичених ароматичних кислот – коричної та гідроксикоричної (кумарової). Реакція відбувається під дією відповідних аміак-ліаз.
З коричної та гідроксикоричної кислот утворюються фенольні сполуки.
При декарбоксилюванні амінокислот утворюються аміни і вуглекислий газ. Із моноаміномонокарбонових амінокислот утворюються моноаміни, з діаміномонокарбонових – діаміни. Реакції здійснюють ферменти декарбоксилази, що як кофермент містять фосфопіридоксаль.


