
юрин физиология растений
.pdf
разованию лимонной кислоты. Промежуточным продуктом этого преобразования является öèñ-аконитовая кислота:
Катализируются обе реакции аконитазой. Затем изоцитрат дегидрируется с участием изоцитратдегидрогеназы, коферментом которой является НАД . В результате окисления образуется ща- велево-янтарная кислота (оксалосукцинат).
Последняя кислота декарбоксилируется. СО2 ацетильного остатка, вступившего в цикл в виде ацетил-СоА, отсоединяется. В результате декарбоксилирования образуется очень активная-кетоглутаровая кислота ( -кетоглутарат).
-Кетоглутарат в свою очередь подвергается тем же изменениям, которые происходят перед началом цикла с пируватом: одновременное окисление и декарбоксилирование.
В реакции принимает участие -кетоглутарат-дегидрогеназ- ный комплекс:
-кетоглутарат НАД СоА-SН сукцинил-S-СоА СО2 НАДН Н ; сукцинил-S-СоА АДФ Н3ÐÎ4 янтарная кислота АТФ СоА-SН.
Освободившийся СО2 является другой частицей, которая отщепляется от ацетильного остатка. Образовавшаяся в результате этих сложных преобразований янтарная кислота (сукцинат) вновь дегидрируется, и образуется фумаровая кислота (фумарат). Реакция происходит с помощью сукцинатдегидрогеназы. Фумарат после присоединения молекулы воды легко преобразуется в яблочную кислоту (малат). В реакции задействована фумаратгидротаза. Яблочная кислота, окисляясь, преобразуется в ЩУК при участии НАД — специфической малатдегидрогеназы.
Таким образом цикл Кребса заканчивается и может начинаться сначала. Одно условие — подача новых молекул ацетил-СоА.
Главное значение цикла Кребса состоит в запасании энергии, которая освобождается в результате разрушения пирувата, в макроэргических связях АТФ. Поставляя в клетку АТФ, цикл Кребса может выступать регулятором других процессов, идущих с за-
172
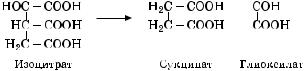
тратой энергии, таких как транспорт воды и солей, синтез и транспорт органических веществ. Чем быстрее проходит преобразование веществ в цикле, тем больше может синтезироваться АТФ, тем быстрее пойдут указанные процессы.
Промежуточные вещества, образуемые в цикле, могут использоваться на синтез белков, жиров, углеводов. Например, аце- тил-СоА — необходимый продукт для синтеза жирных кислот,-кетоглутарат может в результате восстановительного аминирования преобразовываться в глутаминовую, а фумарат или ЩУК — в аспарагиновую кислоты.
Суммарный результат цикла Кребса сводится, таким образом, к тому, что каждая ацетильная группа (двухуглеродный фрагмент), образуемая из пирувата (трехуглеродный фрагмент), расщепляется до СО2. Во время этого процесса восстанавливается НАД , ФАД и синтезируется АТФ.
В регуляции цикла трикарбоновых кислот важное значение имеет соотношение между НАДН и НАД , а также концентрация АТФ. Высокое содержание АТФ и НАДН угнетает активность таких ферментов цикла Кребса, как пируватдегидрогеназа, цитратсинтетаза, изоцитратдегидрогеназа, малатдегидрогеназа. Повышение концентрации оксалоацетата угнетает ферменты, активность которых связана с его синтезом, — сукцинатдегидрогеназы и малатдегидрогеназы. Окисление 2-оксиглутаровой кислоты ускоряется аденилатами, а сукцината — АТФ, АДФ и убихиноном. В цикле Кребса есть и ряд других пунктов регулирования.
3.5. Глиоксилатный путь
При прорастании богатых жиром семян ход цикла Кребса изменяется. Эта разновидность цикла Кребса, в которой участвует глиоксиловая кислота, получила название глиоксилатного цикла (рис. 3.3).
Первые этапы до образования изоцитрата (изолимонной кислоты) идут подобно циклу Кребса. Затем ход реакций изменяется. Изоцитрат при участии изоцитратлиазы расщепляется на янтарную и глиоксиловую кислоты:
173
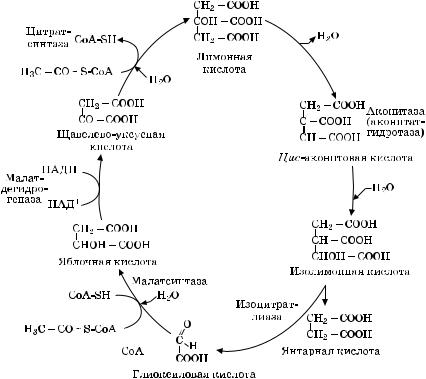
Ðèñ. 3.3. Глиоксилатный цикл
Сукцинат (янтарная кислота) выходит из цикла, а глиоксилат связывается с ацетил-СоА, и образуется малат. Реакция катализируется малатсинтазой. Малат окисляется до ЩУК, и цикл закан- чивается. Кроме двух ферментов — изоцитратазы (изоцитратлиазы) и малатсинтазы, — все остальные те же, что и в цикле Кребса. При окислении малата восстанавливается молекула НАД . Источ- ником ацетил-СоА для этого цикла служат жирные кислоты, образующиеся при разрушении жиров. Суммарное уравнение цикла можно записать в виде
2ÑÍ3ÑÎ~S-ÑîÀ 2Í2Î ÍÀÄ
2ÍS-ÑîÀ ÑÎÎÍ~ÑÍ2~ÑÍ2~ÑÎÎÍ ÍÀÄÍ Í .
Глиоксилатный цикл происходит в специальных органеллах — глиоксисомах.
174
Значение цикла сводится к следующим закономерностям. Восстановленный НАДН может окисляться с образованием трех молекул АТФ. Сукцинат (янтарная кислота) выходит из глиоксисомы и поступает в митохондрию, где включается в цикл Кребса. Тут он преобразуется в ЩУК, затем в пируват, фосфоенолпируват и дальше в сахар.
Таким образом, с помощью глиоксилатного цикла жиры могут преобразовываться в углеводы. Это очень важно особенно при прорастании семян, так как сахара могут транспортироваться из одной части растения в другую, а жиры лишены такой возможности. Глиоксилат может служить материалом для синтеза порфиринов, а это значит, и хлорофилла.
3.6. Окислительный пентозофосфатный цикл
Кроме гликолиза и цикла Кребса, существует и другой универсальный, присущий всем организмам, путь полного окисления глюкозы — пентозофосфатный. Ферменты, которые участвуют в этом процессе, локализованы в цитоплазме (гиалоплазме). Исходным веществом для этого цикла является глюкозо-6-фос- фат (Гл-6-Ф), который принимает участие и в гликолизе. Пентозофосфатный путь, как и гликолиз, разделяют на две фазы: фазу окисления глюкозо-6-фосфата и фазу его регенерации (рис. 3.4).
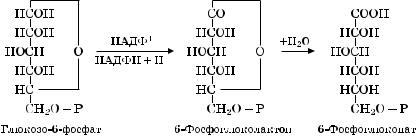
При окислении глюкозо-6-фосфата образуется 6-фосфоглюко- лактон. Последний неустойчив и преобразуется в 6-фосфоглю- конат (6-ФГ).
В процессе окисления глюкозо-6-фосфата участвует фермент глюкозо-6-фосфатдегидрогеназа, коферментом которой выступает НАДФ ; последний в результате окисления глюкозо-6-фосфата восстанавливается:
175
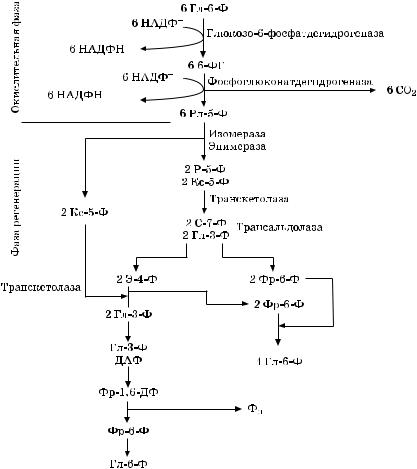
Ðèñ. 3.4. Окислительный пентозофосфатный цикл
6-Фосфоглюконат в свою очередь подвергается окислительному декарбоксилированию, образуется рибулозо-5-фосфат (Рл-5-Ф), и восстанавливается НАДФ , который является коферментом фосфоглюконатдегидрогеназы.
Если во время гликолиза одна молекула преобразуется в две триозы, то в пентозофосфатном цикле от глюкозо-6-фосфата отщепляется один атом углерода и образуется пентоза. Отсюда и другое название пентозофосфатного цикла — апотомический, в отличие
176
от гликолиза, называемого дихотомическим. Образованием рибу- лозо-5-фосфата окислительная фаза цикла заканчивается.
Затем рибулозо-5-фосфат изомеризуется в рибозу-5-фосфат (Р-5-Ф) и ксилулозу-5-фосфат (Кс-5-Ф) при участии соответственно рибозофосфатизомеразы и рибозофосфатэпимеразы.
Рибозо-5-фосфат и ксилулозо-5-фосфат взаимодействуют между собой (реакция катализируется транскетолазой) и образуют гли- церальдегид-3-фосфат (ГА-3-Ф) и седагептулозо-7-фосфат (С-7-Ф). Эти соединения в свою очередь взаимодействуют в присутствии трансальдолазы и образуют фруктозо-6-фосфат (Фр-6-Ф) и эритро- зо-4-фосфат (Э-4-Ф). В присутствии транскаталазы, Э-4-Ф и Кс-5-Ф образуется ГА-3-Ф и фруктозо-6-фосфат, которые в дальнейшем могут быть метаболизированы по гликолитическому пути.
В фазе регенерации участвуют только фосфорные эфиры сахаров. Процесс идет от пентоз через образование седагептулозо-7- фосфата, эритрозо-4-фосфата, фруктозо-6-фосфата и фосфоглицеринового альдегида. Триозы могут конденсироваться до гексоз. В результате альдольной конденсации двух триоз образуется фруктозо-1,6-дифосфат (Фр-1,6-ДФ). Гидролиз фосфатной связи приводит к образованию фосфорной кислоты и глюкозо-6-фос- фата. Цикл заканчивается.
Итак, в результате этого цикла из шести молекул глюкозо-6- фосфата одна молекула окисляется до СО2, а пять молекул регенерируют вновь и выходят из цикла. При этом восстанавливается 12 молекул НАДФ . Суммарное уравнение пентозофосфатного цикла можно записать в виде
6Ãë-6-Ô 12ÍÀÄÔ 7Í2Î5Ãë-6-Ô 6ÑÎ2 12НАДФН 12Н Н3ÐÎ4.
На примере этого цикла еще раз подтверждается справедливость вывода Палладина: окисление веществ происходит в результате дегидрирования, кислород воздуха в окислении дыхательного субстрата не участвует.
В реакциях пентозофосфатного цикла участвуют те же фосфорные эфиры сахаров, что и в фотосинтетическом цикле Кальвина. Последний в связи с этим называют восстановительным пентозофосфатным циклом в отличие от окислительного.
Образование одинаковых промежуточных продуктов в разных циклах говорит о том, что продукты одного цикла могут использоваться в случае необходимости в реакциях другого. Таким образом, каждый цикл не обязательно должен идти до конца, а возможны переходы с одного в другой.
177
ФГА, образующийся во время пентозофосфатного окислительного цикла, превращается в пируват при включении в гликолиз и дальше участвует в цикле Кребса.
Пентозофосфатный цикл — это аэробное окисление углеводов. Он идет в гиалоплазме при высокой концентрации кислорода.
Большое физиологическое значение этот цикл имеет как источ- ник НАДФН, который является донором водорода для восстановительного аминирования и других процессов. Кроме того, пентозы, которые появляются в этом цикле, используются для синтеза таких важных соединений клетки, как АТФ, АДФ, АМФ, нуклеиновые кислоты, пиридиновые ферменты и другие. Эритрозо-4-фосфат — промежуточный продукт этого цикла — участвует в образовании шикимовой кислоты, необходимой для синтеза гормонов роста. Таким образом, этот цикл дыхания наряду с гликолизом и циклом Кребса очень важен для растений.
Один и тот же дыхательный субстрат, например глюкоза, может преобразовываться в клетке разными путями. Выбор пути, по которому пойдет окисление, определяется следующими факторами:
наличие кислорода. Так, пентозофосфатный окислительный
цикл идет только в присутствии О2; анаэробные условия подавляют активность дегидрогеназ этого цикла. В анаэробных условиях идет гликолиз;
активность ферментов. Когда активны ферменты гликолиза, тогда ферменты пентозофосфатного цикла неактивны;
фосфатный баланс, т. е. от отношения неорганического фосфата к АТФ. При низких соотношениях оба пути замедленны.
Рассмотрение преобразований органических веществ при дыхании показывает, что дыхание является центральным процессом обмена веществ, объединяющим преобразование углеводов, белков и жиров. Промежуточные продукты дыхания — аце- тил-СоА, пируват, кетоглуторат и другие — могут использоваться для синтеза различных соединений. Участие одних и тех же веществ в разных циклах доказывает возможность переключения от одного цикла на другой в зависимости от потребностей клетки.
3.7. Электрон0транспортная цепь дыхания
В процессе субстратного фосфорилирования (разрушение органических веществ) происходит синтез АТФ и восстановление НАД , НАДФ , ФАД . В результате гликолиза в анаэробных условиях образуются две молекулы АТФ и две молекулы НАДН; при
178
последовательном осуществлении гликолиза и цикла Кребса в аэробных условиях — четыре молекулы АТФ, 10 молекул НАДН и две молекулы ФАДН2. Во время глиоксилатного цикла восстанавливается одна молекула НАД . При разрушении глюкозо-6- фосфата в пентозофосфатном окислительном цикле восстанавливается 12 молекул НАДФ .
Таким образом, часть энергии, которая освобождается при разрушении дыхательного субстрата, запасается в макроэргиче- ских связях АТФ, а часть, причем большая, содержится в восстановленных коферментах.
Образовавшиеся молекулы АТФ используются в качестве источника энергии для работы клетки, а восстановленные коферменты могут служить донорами водорода для восстановительных процессов, проходящих в клетках. Кроме того, они могут окисляться с образованием воды и одновременным синтезом АТФ. В этом случае кофермент включается в электрон-транспорт- ную цепь.
Поскольку в восстановленных коферментах заключено довольно большое количество энергии, освобождаться она должна постепенно, путем передачи Н и электрона от этих коферментов целому ряду переносчиков. Эти переносчики связаны с белками и образуют цепь транспорта электронов или дыхательную цепь.
Электрон-транспортная цепь и АТФаза находятся во внутренней мембране митохондрий. АТФаза располагается в грибовидных выростах внутренней мембраны.
Порядок размещения компонентов в цепи зависит от величи- ны их окислительно-восстановительного потенциала (ОВП). Стандартный ОВП донора электронов НАДН равен 0,32 В. Каждый следующий переносчик находится на более низком уровне восстановленности и в соответствии с этим содержит меньше энергии, чем предыдущий. Однако подобные системы очень динамичны.
Б. Чанс и другие ученые (США) в 50-х гг. ХХ в. разместили компоненты ЭТЦ в следующем порядке (рис. 3.5).
Несколько позднее Д. Грин (1961) пришел к выводу, что все переносчики электронов в митохондриальной мембране сгруппированы в четыре комплекса; это было подтверждено дальнейшими исследованиями.
Таким образом, дыхательная цепь митохондрий включает в себя четыре основных мультиэнзимных комплекса и два небольших по молекулярной массе компонента: убихинон и цитохром ñ (òàáë. 3.1).
179

Ðèñ. 3.5. Передача энергии по цепи переносчиков электронов в мембране митохондрий
Таблица 3.1
Компоненты ЭТЦ митохондрий растений и их стандартные окислительно-восстановительные потенциалы (Е)
Компоненты |
Характеристика |
Å, Â |
|
|
|
Комплекс I (НАД(Ф)Н — убихинон-оксидоредуктаза) |
|
|
|
|
|
ÍÀÄ(Ô)Í |
Никотинамидадениндинуклеотид восстановленный |
–0,320 |
ÔÌÍ |
Флавинмононуклоеотид — кофермент дегидрогена- |
–0,070 |
|
зы, окисляющей эндогенный НАДН |
–0,300 |
|
|
|
FeSN1 |
Железосерные центры (белки): |
–0,305 |
FeSN2 |
N1 – 2Fe2S; N2, N3 – 4Fe4S |
–0,245 |
FeSN3 |
|
–0,020 |
Комплекс II (сукцинат — убихинон-оксидоредуктаза) |
|
|
|
|
|
ÔÀÄ |
Флавинадениндинуклеотид — кофермент сукцинат- |
–0,045 |
|
дегидрогеназы |
|
FeSS1 |
Железосерные белки: |
–0,007 |
FeSS2 |
S1, S2 — 2FeS-òèïà |
(0,230) |
FeSS3 |
S3 — 4Fe4S-òèïà |
0,080 |
180
Окончание табл. 3.1
Компоненты |
Характеристика |
Å, Â |
QУбихинон — липидорастворимый одно- и двухэлек- 0,070 тронный переносчик
Комплекс III (убихинол — цитохром ñ-оксидоредуктаза)
Цитохромы |
Гемопротеины, в которых гем связан с белком неко- |
|
|
|
валентно |
|
|
b556 |
|
|
0,075 |
b560 |
|
|
0,080 |
Öèò ñ1 |
Цитохром ñ552 — гемопротеин; гем ковалентно свя- |
0,235 |
|
|
зан с белком |
|
|
FeSR |
Железосерный белок Риске (2Fe2S) |
0,280 |
|
Öèò ñ |
Цитохром ñ550 — гемопротеин; гем ковалентно свя- |
0,235 |
|
|
зан с белком; водорастворим |
|
|
|
|
|
|
Комплекс IV (цитохром ñ-кислород-оксидоредуктаза); (цитохромоксидаза) |
|||
|
|
|
|
Öèò à |
Цитохром à — гемопротеин, гем которого некова- |
0,190 |
|
|
лентно связан с белком |
0,210 |
|
|
|
|
|
CuÀ |
Атом меди, функционирующий с Öèò à как редокс- |
|
|
|
компонент комплекса |
|
|
Öèò à3 |
Цитохром à3 — гемопротеин; способен взаимодей- |
0,385 |
|
|
ствовать с кислородом |
|
|
CuB |
Атом меди, функционирующий с Öèò à3 ïðè îáðà- |
|
|
|
зовании комплекса с кислородом |
|
|
Î2, Í2Î |
1/2Î2 2Í 2e |
Í2Î |
0,816 |
Комплекс I осуществляет перенос электронов от НАД(Ф)Н к убихинону Q. Его субстратом служит молекула внутримитохондриального НАДН, который восстанавливается в цикле Кребса. В состав комплекса входит флавиновая ФМН-зависимая НАД(Ф)Н — убихинон-оксидоредуктаза, содержащая три железосерных центра (FeSN1–3). При встраивании в искусственную фосфолипидную мембрану этот комплекс функционирует как протонная помпа.
Комплекс II катализирует окисление сукцината убихиноном. Эту функцию выполняет флавиновая (ФАД-зависимая) сукцинат — убихинон-оксидоредуктаза, в состав которой также входят три железосерных центра (FeS1–3).
181
