
- •Министерство образования и науки Российской Федерации
- •Редкие элементы ia подгруппы. Общая характеристика элементов
- •Свойства элементов iа подгруппы
- •2. Литий
- •2.1. Химия лития
- •2.1.1. Соединения лития с кислородом
- •Свойства гидроксидов щелочных металлов
- •2.1.2. Галогениды лития
- •Свойства галогенидов лития
- •2.1.3. Соединения лития с другими элементами
- •2.1.4. Сплавы лития с металлами
- •2.2. Важнейшие области применения лития и его соединений
- •2.3. Геохимия лития и сырьевые источники
- •2.3.1. Минералы лития
- •2.3.2. Извлечение лития из солевых растворов
- •Характеристика лгмс наиболее известных месторождений мира
- •2.4. Технология переработки литиевого сырья
- •2.4.1. Обогащение литиевого рудного сырья
- •2.4.2. Общие вопросы технологии лития
- •2.4.3. Переработка сподумена
- •2.4.4. Переработка лепидолита
- •2.4.5. Переработка карбоната лития на гидроксид и хлорид
- •2.5. Получение металлического лития
- •Рекомендуемая литература
2.1.2. Галогениды лития
Галогениды лития и других щелочных элементов – это соединения элементов с самыми ярко выраженными металлическими свойствами и самыми типичными неметаллами. Все галогениды щелочных металлов – ионные соединения с небольшой долей ковалентности. Для галогенида любого щелочного металла доля ковалентности связи уменьшается в ряду F – Cl – Br – I. Фтор в соединениях проявляет степень окисления только –1, хлор, бром и иод – от –1 до +7. Фториды – наиболее прочные галогениды, они имеют более высокие температуры плавления и кипения (табл. 3).
Фторид лития, LiF, - бесцветное кристаллическое вещество с гранецентрированной кубической решеткой (ГЦК) типа NaCl (Z = 4; a = 4,028 Ǻ, к.ч. Li = 6). Фторид лития наиболее тугоплавкий и высококипящий из галогенидов лития (табл. 3). Плотность (20 ºC) – 2,20 г/см3. Энтальпия образования ΔH = – 617 кДж/моль. При температуре 1100-1200 ºC (значительно ниже точки кипения) начинается быстрое его испарение. Фторид лития не гигроскопичен, кристаллогидратов не образует, в воде растворяется плохо: при 25 ºC – 0,13 г/100 г H2O. Растворимость понижается в присутствии аммиака и, особенно, фторида аммония; в HNO3и H2SO4растворяется при комнатной температуре, в плавиковой кислоте образуется гидрофторид, LiHF2, лучше растворимый в воде, чем LiF.
Таблица 3
Свойства галогенидов лития
|
Соединение |
Т пл.,ºC |
Т кип.,ºC |
– ΔH |
d, г/см3 |
|
LiF |
848 |
1681 |
617 |
2,2 |
|
LiCl |
607 |
1385 |
405 |
2,07 |
|
LiBr |
550 |
1310 |
349 |
2,9 |
|
LiJ |
469 |
1171 |
271 |
3,3 |
При нагревании гидрофторид разлагается на LiF и HF. В отличие от других галогенидов лития LiF не растворяется в большинстве органических растворителей. Фторид лития образует двойные соединения с фторидами многих элементов. Для получения LiF используют реакцию взаимодействия Li2CO3с плавиковой кислотой или осаждение из растворов солей лития фторидами калия, натрия, аммония.
Незначительная растворимость LiF в воде используется в аналитической химии для отделения лития от других щелочных металлов. Предлагалось использовать LiF для выделения лития из разбавленных производственных растворов после первичного осаждения Li2CO3. Фторид лития применяется в качестве компонента многих флюсов, используемых при плавке металлов и при получении алюминия в бокситкриолитовых ваннах. Монокристаллы LiF применяются (вместо CaCl2) в оптических приборах, тат как они прозрачны для лучей с длиной волны до 1000Ǻ и имеют практически постоянную дисперсию в пределах всего видимого спектра.
Х
Рис.
6. Политерма растворимости LiCl
в воде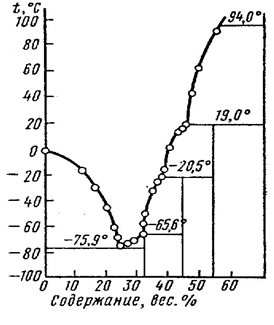
Как видно из рис. 6, система LiCl – H2O характеризуется следующими температурами фазовых переходов:
94ºC LiCl↔LiCl∙H2O
190 ºC LiCl∙H2O↔LiCl∙2H2O
–20,5ºC LiCl∙2H2O↔LiCl∙3H2O
–65,6ºCLiCl∙3H2O↔LiCl∙5H2O
Эвтектическая точка 25 масс.% LiCl и –75,9 ºC. В водных растворах LiCl сильно диссоциирован, в 1М растворе степень диссоциации 84,1%, а в 0,002М – 97%. Хлорид лития хорошо растворяется во многих органических растворителях – спиртах, в том числе многоатомных, хлороформе, ацетоне, пиридине, сложных эфирах. Растворение часто сопровождается разогреванием вследствие образования сольватов (LiCl∙CH3OH).
Вследствие способности ионов Li+к гидратации хлорид лития является энергичным высаливающим и дегидратирующим агентом. Сухой LiCl и его растворы поглощают аммиак, образуя комплексные ионы [Li(NH3)4]+. LiCl образует двойные соединения с хлоридами многих элементов.
Хлорид лития получается хлорированием металлического лития, Li2O или LiOH хлором или газообразным HCl или по реакции:
Li2SO4+ BaCl2↔LiCl + BaSO4 (12)
В промышленном масштабе используется реакция
Li2CO3 + HCl → 2LiCl + H2O + CO2 (13)
Хлорид лития имеет важное промышленное значение, так как является практически единственным соединением, используемым для получения металлического лития. Способность LiCl и его растворов поглощать аммиак и обратимо поглощать пары воды при изменении температуры и влажности окружающего воздуха определили применение LiCl для кондиционирования воздуха в производственных помещениях и общественных зданиях.
Бромид лития, LiBr, – бесцветное кристаллическое вещество с кубической гранецентрированной решеткой типа NaCl (a = 5,501 Ǻ), плотность 3,464 г/см3, Т пл. 552 ºC; энтальпия образования ΔH = – 349 кДж/моль (табл. 3). Выше температуры плавления начинает разлагаться. Расплавленный LiBr разрушает стекло, фарфор и платину. Бромид лития более гигроскопичен, чем LiCl и лучше, чем LiCl, растворяется в воде (при 20 ºC – 177 г/100 г H2O). Из водных растворов выделяется в виде кристаллогидратов с 2, 3 и 5 молекулами воды; обезвоживается с трудом. Бромид лития растворяется в спиртах, ацетоне, пиридине, глицерине и других органических растворителях, взаимодействует с аммиаком с образованием соединения LiBr∙nNH3(n = 1÷4). Получают LiBr при непосредственном взаимодействии элементов, реакция протекает менее энергично, чем между литием и хлором. В промышленности используют реакцию Li2CO3с бромисто-водородной кислотой. Монокристаллы бромида лития используются в оптике.
Иодид лития, LiI, – кристаллическое вещество, как и остальные галогениды лития, имеет кристаллическую решетку типа NaCl (ГЦК; a = 6,012Ǻ). Самый неустойчивый галогенид лития, имеет самую низкую энтальпию образования (– 271 кДж/моль), а также температуры плавления и кипения (табл. 3). Расплавленный LiIразрушает стекло, фарфор, платину, очень гигроскопичен, хорошо растворяется в воде (при 19ºC – 164 г/100г H2O). Из водных растворов выделяется в виде кристаллогидратов с 0,5; 1; 2 и 3 молекулами воды. Обезвоживается при нагревании в токе HI, при пропускании через расплавленную соль сухого водорода или возгонкой в вакууме. Растворяется в спиртах, пиридине, с аммиаком образует продукты присоединения LiI∙nNH3(n = 1÷7). При взаимодействии расплавленного LiIсI2образуются полигалогениды LiIn(n = 3÷9). При добавлении в раствор LiIсоляной, азотной или серной кислоты выделяется иод. Получают LiIпо реакции между Li2CO3и HIс последующим упариванием и высушиванием образующегося кристаллогидрата в токе HIи удалением иода путем пропускания через расплавленную соль водорода. Иодид лития применяется в медицине и в производстве фотореактивов, в виде раствора с иодидом ртути (“тяжелые жидкости”) используется для разделения минералов.
Литий образует соли со всеми кислородсодержащими кислотами хлора: LiCl+1O (гипохлорит), LiCl+3O2(хлорит), LiCl+5O3(хлорат), LiCl+7O4(перхлорат). Все эти соли – сильные окислители, из них наиболее устойчив перхлорат, Тпл.которого 236 ºC; выше 400 ºC разлагается на LiCl и O2. LiClO4гигроскопичен, хорошо растворяется в воде, спиртах, эфирах.
Для брома и иода известны только отдельные представители соединений этого типа. Наиболее интересным из них является иодат лития LiIO3, обладающий уникальным комплексом свойств – акустических, пьезоэлектрических.
