
Вьюник. Лекция № 14
.pdf
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Для практичного вирiшення задачi приходиться вводити наступнi спрощення:
1Припускається, що бiльшiсть e¯не приймає участi в утворенi МО, локалiзована поблизу ядер;
2В утворенi МО приймають участь лише зовнiшнi валентнi або частина валентних e¯;
3Хвильова функцiя МО подається у виглядi ЛКАО.
Вразi застосування МО ЛКАО до КС спочатку обчислюють хвильову функцiю ΨL молекулярних орбiталей лiган-
дiв: ΨL = c1ψ1 + c2ψ2 + ··· + ciψi + ··· + cnψn, де n- координацiйне число, ψi- атомнi хвильовi функцiї тих e¯, якi
вносять основний вклад в утворення хiмiчного зв‘язку з комплексоутворювачем.
31/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Для обчислення хвильової функцiї МО комплексної сполу-
ки (Ψкс): Ψкс = aψЦА + bΨL, де ψЦА-хвильовi функцiї АО комплексоутворювача, якi дають основний внесок в утво-
рення хiмiчного зв‘язку.
При обчисленi необхiдно мати на увазi, що молекулярнi хвильовi функцiї лiгандiв ΨL утворюються лише iз таких атомних функцiй ψi лiгандiв, орбiталi яких здатнi до утворення σ- зв‘язку з комплексоутворювачем.
Для октаедричних комплексiв, наприклад , такими атомними хвильовими функцiями L є s,px,py,pz,dx2−y2,dz2. Функцiї dxy,dyz,dxz для цих цiлей не можуть бути використанi.
32/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Проте, можуть бути i такi випадки, коли лiганди мають орбiталi, здатнi до утворення π-зв‘язкiв.
У випадку утворення π-зв‘язкiв обчислюють ще одну молекулярну хвильову функцiю лiгандiв Ψ′L, яка потiм може комбiнуватися з атомними функцiями комплексоутворювача ψЦА, здатними до утворення π- зв‘язкiв.
Для октаедричних комплексiв такими орбiталями ЦI можуть бути px,py,pz,dxy,dxz,dyz.
Як вiдомо математичний апарат квантової механiки дозволяє вияснити, якi МО є в даному комплексi (зв‘язуючi, розпушуючi, незв‘язуючi), яка їх енергiя i який розподiл електронної густини.
Все це залежить як вiд природи ЦI i L , так i вiд будови КС. У випадку однакової будови енергетичнi дiаграми дуже подiбнi.
33/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
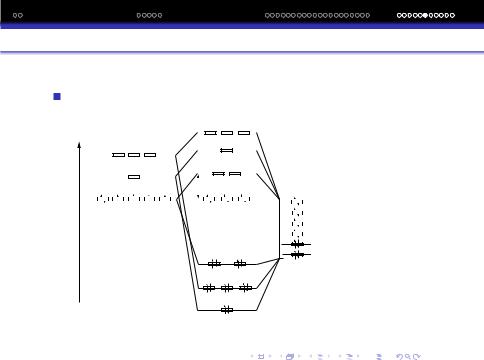
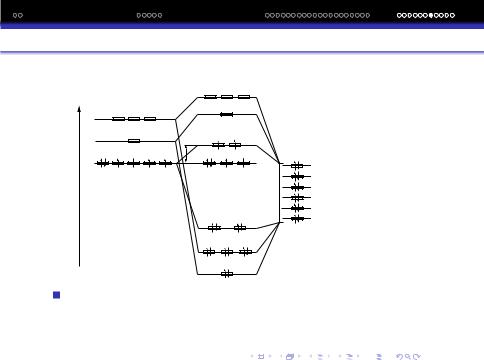
Схема для октаедричного комплекса приведена
|
|
|
|
|
|
|
|
|
|
|
АО |
|
|
|
|
|
|
|
МО |
|
|
|
|
|
|
|
|
|
|
АО |
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
σ |
р |
σ р |
σ |
р |
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
|
|
|
y |
|
|
|
|
z |
|
|
|
|
|||||||||||||||||
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4p |
|
|
|
|
|
|
|
σsр |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
σxр2-y2 σzр2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
] 3+ |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4s |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[Co(NH |
3 |
) |
6 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3d |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
πxz |
πyz |
πxy |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
σxзв2-y2 σzзв2
σxзв  σyзв
σyзв  σzзв
σzзв
σsзв
34/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
|
Теорiя кристалiчного поля |
|
Теорiя поля лiгандiв |
||
Теорiя поля лiгандiв |
|
|
|
|
|
|
|
|
АО |
|
МО |
|
АО |
|
|
|
|
σ р |
σ р |
σ |
р |
|
|
|
|
x |
y |
z |
|
|
|
E |
4p |
|
σsр |
|
|
|
|
|
|
|
|
|
|
|
|
|
4s |
σxр2-y2 σzр2 |
[CoF6 |
] |
3 – |
||
|
|
|
|
|
|
||
|
3d |
|
|
|
|
|
|
|
|
πxz |
πyz |
πxy |
|
|
|
σxзв2-y2 σzзв2
σxзв  σyзв
σyзв  σzзв
σzзв
σsзв
За результатами квантово-механiчних розрахункiв будують дiаграму енергетичних рiвнiв МО i визначають електронну будову (конфiгурацiю) комплекса.
35/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Для цього у вiдповiдностi з принципом Паулi електрони розмiщують по два (↑↓) на кожну одноелектронну МО, щоб заповнити їх вiдповiдно до принципу найменшої енергiї.
Розподiл e¯ суттєво залежить вiд енергiї спарювання (P) електронiв i рiзницi в енергiях t2g- i eg- орбiталей ( =
Eeg − Et2g).
Остання за аналогiєю з ТКП називається параметром розщеплення.
Якщо P > , то спочатку t2g i eg орбiталi заповнюються по 1-му e¯, а потiм починається утворення ЕП.
Цей випадок за аналогiєю з ТКП називається випадком слабкого поля.
36/39

Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Якщо ж P < , то спочатку закiнчується заповнення t2g- орбiталей електронними парами, а потiм починається заповнення eg- орбiталей.
Цей випадок називається випадком сильного поля.
Метод МО ЛКАО є найбiльш загальним i точним iз практично прийнятних методiв квантової хiмiї.
Утворення хiмiчних зв‘язкiв у вiдповiдностi до цього методу вiдбувається за рахунок такого розподiлу електронної хмаринки на зв‘язуючих орбiталях, при якому вона стягує до себе ядра системи, утворюючи мiж ними щось подiбне до спайки.
37/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
На цих орбiталях енергiя e¯ менша, чим на вiдповiдних АО, з яких вони утворенi. На розрихлюючих орбiталях навпаки. Очевидно, що зв‘язок утворюється у випадку i за рахунок переваги зв‘язуючих МО над розрихлюючими.
Порiвняння МО ЛКАО з ТКП показує, що в рядi випадкiв вони дають аналогiчнi ззовнi подiбнi результати. До недолiкiв ТПЛ вiдносяться: значнi розрахунковi труднощi.
ТПЛ в принципi може враховувати любу ступiнь ковалентностi i π-зв‘язок. Теорiя використовується для пояснення спектрiв, магнiтних властивостей, стiйкостi КС, енергiї зв‘язкiв, окисно-вiдновних властивостей i т.iнш.
38/39
Теорiя Косселя-Магнуса |
Теорiя валентних зв‘язкiв |
Теорiя кристалiчного поля |
Теорiя поля лiгандiв |
Теорiя поля лiгандiв
Головний недолiк: неможливо зробити кiлькiснi розрахунки енергiї електронiв. У порiвнянi з другими квантово-механiчними теорiями ТПЛ дає бiльш точнi результати. Можливостi застосування її не обмежуються iоннiстю або ковалентнiстю зв‘язкiв. ТПЛ менш наочна.
39/39
