
Вьюник. Лекция № 16
.pdf
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Ланцюговi реакцiї
Ланцюговi реакцiї: Радикальнi реакцiї звичайно протiкають за ланцюговим механiзмом.
Особливiсть ланцюгових реакцiй полягає в тiм, що один первинний акт активацiї приводить до перетворення величезної кiлькостi молекул вихiдних речовин.
Теорiя ланцюгових реакцiй була створена працями академiка М.М.Семенова, Хiншельвуда i др. учених.
Iснує 2-а типа ланцюгових реакцiй: з нерозгалудженими i з розгалудженими ланцюгами.
Прикладом реакцiй 1-го типу є фотохiмiчний синтез HCl. Виникненю ланцюга вiдповiдає реакцiя утворення атомiврадикалiв
Cl2 + hν = 2 Cl·; ECL−CL = 240 Кдж/моль, H2 + hν = 2 H·, EH−H = 440 Кдж/моль.
21/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Ланцюговi реакцiї
Валентноненасичений атом-радикал ·Cl потiм взаємодiє з молекулою H2, утворюючи при цьому молекулу HCl i радикал ·H; ·Cl+H2 = HCl+·H. Останнiй взаємодiє з молекулою Cl2: ·H + Cl2 = HCl + · Cl.
Довжина ланцюга елементарних хiмiчних актiв взаємодiї досягає сотень тисяч ланок. Природно можливi i зiткнення вiльних радикалiв один з одним, що приводить до обриву ланцюга ·H + · H = H2 або ·Cl + · Cl = Cl2.
Однак, це вiдбувається лише у випадку, коли надлишкова енергiя вiдбирається третiм тiлом (потрiйне спiвударяння 2-х радикалiв i молекули або передача енергiї стiнкам посудини). Тому швидкiсть ланцюгових реакцiй чутлива до домiшок i до форми посудини.
22/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Ланцюговi реакцiї
Прикладом процесiв з нерозгалуженими ланцюгами є хлорування вуглеводнiв, розкладання органiчних сполук, полiмеризацiя.
Процеси з розгалуженими ланцюгами вiдрiзняються тим, що в них одинична реакцiя одного вiльного радикала приводить до виникнення бiльш нiж одного нового вiльного радикала. Один з них продовжує ланцюг, а другий - починає новий.
Як приклад розглянемо процес окиснення водню:
а |
·H + O2 = ·OH + · O; |
|
|
||
б |
|
·OH + H2 = H2O + ·H; |
|
||
в |
|
·O + H2 = ·OH + · H i т. д. |
|
|
|
23/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Ланцюговi реакцiї
Таким чином, прогресивно збiльшується число активних частинок i рiзко зростає швидкiсть хiмiчної реакцiї.
Речовини, якi в малих кiлькостях (дозах) уповiльнюють хiмiчну реакцiю (викликають обрив ланцюга) називаються iнгiбiторами. В реакцiї синтезу HCl це молекули O2.
Ранiше їх помилково називали вiд‘ємними каталiзаторами. Однак, O2 пiсля реакцiї не залишається у вiльному станi.
Iнгiбiтори мають велике практичне застосування (тетраетилсвинець, I2 i iншi добавки до пального є антидетонаторами).
24/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Ланцюговi реакцiї
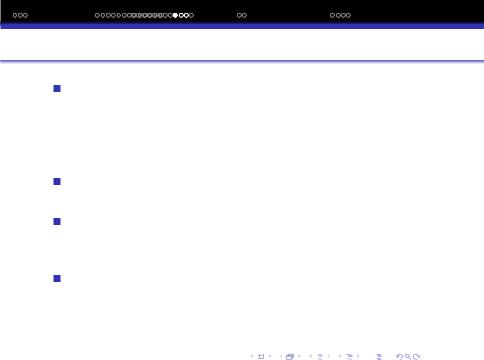
Шлях, яким протiкає процес взаємодiї визначається енергiями активацiї елементарних актiв.
Акт взаємодiї |
Х= Cl |
X= Br |
X= I |
Механiзм |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
− |
|
|
209 |
188 |
168 |
молекулярний |
H2 + X2−2 HX |
|||||||||
|
|
1 |
− |
|
|
117 |
96 |
71 |
ланцюговий |
|
|
2 X2−X |
|
|
|||||
X |
+ |
H2 |
− |
+ |
H |
25 |
73 |
143 |
|
|
−HX |
|
|
||||||
Σ,Кдж/моль |
142 |
169 |
214 |
|
|||||
|
|
|
|
|
|
|
|
|
|
25/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Фiзичнi методи стимулювання хiмiчних перетворень
Фiзичнi методи стимулювання хiмiчних перетворень. У зв‘язку з пошуками нових шляхiв проведення хiмiчних процесiв в хiмiчнiй технологiї розробляються рiзнi методи направленого регулювання реакцiйної здатностi речовин. Окрiм того, iнтенсивно вивчаються методи стимулювання.
На реакцiйну здатнiсть речовин значний вплив оказують: свiтло, iонiзуючi випромiнювання, тиск, механiчна дiя i др. Дiю свiтла на хiмiчнi реакцiї вивчає фотохiмiя (синтез HCl, синтез органiчних речовин в рослинах, розкладання H2O2, свiтлочутливих матерiалiв i т. iнш).
Фотохiмiчна дiя свiтла полягає в тiм, що молекули реагуючих речовин, поглинаючи квант свiтла, збуджуються (стають реакцiйноздатними або розкладаються на iони i радикали).
26/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Фiзичнi методи стимулювання хiмiчних перетворень
Фотографiя, фотохлорування, фотосульфохлорування використовують фотохiмiчнi процеси.
Створення штучних систем, якi здiйснюють фотосинтез, аналогiчний фотосинтезу в рослинах мало б неоцiниме значення.
Лазерне випромiнювання викликає селективне збудження молекул: CH3OH, CD3OD + Br2; пiд його дiєю графiт алмаз.
Рентгенiвськi променi (X), α-променi, γ-променi, потiк нейтронiв викликають глибиннi фiзико-хiмiчнi змiни в речовинах i iнiцiюють численi хiмiчнi реакцiї.
Радiацiйна хiмiя, радiолiз води (·H, ·OH, ·HO2, H2O+, H2O−). Механохiмiя (механiчнi дiї, розтирання V2O5·4H2O-розривання зв‘язкiв (вальцування), подрiбнення, перетирання.
27/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Фiзичнi методи стимулювання хiмiчних перетворень
Ще бiльш сильнiшi змiни вiдбуваються пiд дiєю надвисоких тискiв (десятки тисяч атмосфер): графiт алмаз, бiлий графiт боразон.
Хiмiя ударного стиснення (ударна хвиля) при детонацiї вибухових речовин окрiм роздрiбнення можуть утворитися i бiльш складнi речовини: сирий каучук резину , амiнокислоти простi бiлки.
28/35
Загальнi положення Каталiз Механiзм хiмiчних реакцiй Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу
Механiзм хiмiчних реакцiй
Експериментальне визначення швидкостi реакцiї та константи хiмiчної рiвноваги
Експериментальне визначення швидкостi реакцiї та константи хiмiчної рiвноваги:
1Хiмiчний аналiз проб. Вiдбирають проби, швидко їх охолоджують або хiмiчним шляхом зупиняють реакцiю i викону-
ють аналiтичне визначення,
2 Вимiрювання поглинання свiтла вiдповiдної довжини хвилi,
3 Визначення концентрацiї за допомогою поляриметрiї,
4 Вимiрювання ЕП,
5 Вимiрювання тиску пари над розчином,
6 За змiною забарвлення.
Для визначення Kхр необхiдно знати початкову концентрацiю реагуючих речовин i рiвноважну концентрацiю тiльки однiєї реагуючої речовини або продукту реакцiї. Вимiрюють густину розчину, тиск пари над розчином, поглинання свiтла, ЕП, рефракцiя i т. iнш.
29/35
Загальнi положення Каталiз |
Механiзм хiмiчних реакцiй |
Зв‘язок мiж G◦ i Kхр Вплив змiни умов на хiмiчну рiвновагу |
Зв‘язок мiж |
G◦ i Kхр |
|
Зв‘язок мiж Kp , Kc i |
G◦. Константа хiмiчної рiвноваги |
|
зв‘язана зi змiною стандартної енергiї Гiббса хiмiчної реа- |
||
кцiї простим рiвнянням |
G = H − T S = −RT lnK. |
|
Отже, якщо для заданої реакцiї вiдомими є G0 або H i S, то можна розрахувати Kхр i навпаки.
Це спiввiдношення є унiверсальним. Воно застосовується для любих рiвноваг.
Iз цього спiввiдношення видно, що великим вiд‘ємним значенням G0 вiдповiдає велике значення Kхр. Це означає, що в рiвноважнiй сумiшi переважають продукти взаємодiї. Якщо ж G0 > 0, то в сумiшi переважають вихiднi речо-
вини, Kхр-мала. При G0 = 0 ; Kхр = 1.
H0 S
Рiвнянню можна придати вигляд K = e− RT ·e R . Це рiвняння вiдбиває протилежний вплив ентальпiйного та ентропiйного факторiв.
30/35
