
- •Белорусский государственный медицинский университет
- •Биологическая химия
- •Содержание
- •Предисловие
- •Структура и функции белков и пептидов. Сложные белки
- •Классификация белков
- •I. Функциональная (по функции, выполняемой в организме)
- •II. По форме молекулы
- •Свойства аминокислот
- •Уровни структурной организации белковых молекул
- •Сложные белки
- •Методы исследования структуры белков и пептидов
- •Этапы исследования первичной структуры белков и пептидов
- •Методы разделения белков Отделение белков от низкомолекулярных примесей
- •Разделение белков по молекулярной массе
- •Выделение индивидуальных белков
- •Анализ гомологичных белков
- •Установление ак-последовательности белка
- •I. Определение n-концевой ак
- •II. Определение с-концевой ак
- •III. Определение ак-последовательности
- •Белки соединительных тканей (Молекулы внеклеточного матрикса)
- •Фибриллярные структурные белки
- •Фибриллярные адгезивные белки
- •Введение в энзимологию. Свойства ферментов
- •Классификация и номенклатура ферментов
- •Строение фермента
- •Единицы измерения активности
- •Влияние температуры
- •Влияние рН
- •Влияние концентрации субстрата
- •Регуляция активности ферментов Принципы регуляции химических процессов в клетке
- •Влияние ингибиторов
- •Ковалентная модификация структуры фермента
- •Примеры использования ингибиторов в медицинской практике
- •Множественные формы ферментов
- •Медицинские аспекты энзимологии
- •Причины гиперферментемий
- •Применение ферментов в медицине
- •2 Стороны метаболизма
- •Общая схема катаболизма пищевых веществ атф и адениловая система клетки
- •Окислительное декарбоксилирование пирувата
- •Последовательность реакций, катализируемых пируватдегидрогеназным комплексом
- •Регуляция пируватдегидрогеназного комплекса
- •Лимоннокислый цикл Кребса, цикл трикарбоновых кислот (цтк)
- •Функции цикла Кребса
- •Регуляция цтк
- •Тканевое дыхание, окислительное фосфорилирование
- •Комплексы дыхательной цепи
- •Пути утилизации кислорода клеткой
- •Переваривание, всасывание, поступление в клетку углеводов. Метаболизм гликогена
- •Переваривание углеводов
- •Всасывание углеводов
- •Транспорт глюкозы в клетки
- •Превращение глюкозы в клетках
- •Метаболизм гликогена
- •Синтез гликогена (гликогенез)
- •Распад гликогена (гликогенолиз)
- •Гликолиз. Аэробное окисление глюкозы. Глюконеогенез гликолиз
- •Патогенетическая взаимосвязь углеводов пищи и кариеса
- •Аэробное окисление глюкозы
- •Глюконеогенез
- •Пентозофосфатный путь. ГлюкуроновЫй путь пентозофосфатный путь
- •ГлюкуроновЫй путь
- •Переваривание липидов в желудочно-кишечном тракте, система их доставки в клетки Классификация липидов по химическому строению
- •Переваривание и всасывание
- •Ресинтез липидов в клетках слизистой тонкого кишечника:
- •Депонирование и мобилизация липидов из жировых депо, внутриклеточный обмен жирных кислот
- •Внутриклеточный метаболизм жирных кислот
- •Окисление жирных кислот в пероксисомах
- •Синтез жирных кислот
- •Происхождение ненасыщенных жирных кислот в клетках
- •Синтез и нарушения обмена холестерола, метаболизм кетоновых тел
- •Синтез холестерола de novo
- •Регуляция синтеза холестерола
- •Роль нарушений обмена холестерола в развитии атеросклероза
- •Факторы, влияющие на уровень лпнп у человека
- •Факторы, связанные с низким или высоким уровнем хс лпвп
- •Образование и утилизация кетоновых тел
- •Система свёртывания крови
- •Свёртывающая (гемокоагуляционная) система крови
- •Антикоагулянтная система
- •Фибринолитическая система
- •Оценка состояния обмена белков, протеолиз азотистый баланс
- •Протеолиз, свойства протеаз. Ограниченный и тотальный протеолиз
- •Переваривание белков в желудочно-кишечном тракте
- •Транспорт аминокислот в клетки
- •Внутриклеточный обмен аминокислот общие пути катаболизма аминокислот Реакции переаминирования
- •Реакции дезаминирования
- •Пути обезвреживания аммиака в организме — синтез глутамина и мочевины.
- •Химия нуклеопротеинов Нуклеиновые кислоты— биополимеры, мономерами которых являются нуклеотиды.
- •Строение рнк
- •Биосинтез нуклеотидов
- •Фосфорибозиламин
- •Инозинмонофосфат
- •ДТмф дУмф умф
- •Образование дезоксирибонуклеотидов
- •Биосинтез днк
- •Биосинтез рнк
- •Структура рнк-полимеразы прокариот
- •R Аминоацил-тРнк
- •Гормоны. Общий механизм действия гормонов
- •Механизм действия гормонов, взаимодействующих
- •Механизм действия гормонов, взаимодействующих с 1-тмс-рецепторами
- •Механизм действия гормонов, взаимодействующих с внутриклеточными (r)
- •Гормоны — производные белков, пептидов и аминокислот гормоны гипоталамуса
- •Гормоны аденогипофиза Это гормоны белково-пептидной природы.
- •Гормоны задней доли гипофиза
- •Гормоны поджелудочной железы
- •2. Окисление и изомеризация прегненолона в прогестерон. Прегненолон является предшественником всех стероидных гормонов.
- •Половые гормоны
- •Биохимия питания. Макро- и микроэлементы
- •Макроэлементы
- •Концентрация электролитов вне и внутри клетки существенно различается: натрий и кальций преобладают во внеклеточном пространстве, калий и магний — внутри клетки. Кальций
- •Кальцитонин
- •Паратирин (паратгормон)
- •Витамин д (кальциферол), антирахитический
- •Микроэлементы Железо
- •Биохимия питания. Витамины и другие незаменимые факторы питания. Синдром недостаточного питания
- •Витамины
- •Биохимия соединительных тканей и органов полости рта (костная, хрящевая ткани; зубы)
- •Неколлагеновые белки костной ткани и их роль в процессах минерализации
- •Химический состав тканей зуба и кости (весовые %)
- •Биохимия ротовой жидкости
- •Химический состав ротовой жидкости
- •Функции ротовой жидкости
- •1. Защитная.
- •3. Очищающая.
- •Ферменты ротовой жидкости и их роль
- •Поверхностные образования на эмали
- •Фтор (f) и его роль в организме
- •Биохимия печени
- •Функции печени
- •Миофибриллярные (сократительные) белки
- •Молекулярный механизм мышечного сокращения
- •Источники энергии мышечного сокращения
- •Механизмы энергообеспечения мышечного сокращения
Общая схема катаболизма пищевых веществ атф и адениловая система клетки
В энергетическом обеспечении клетки важнейшую роль играет адениловая система, которая включает АМФ, АДФ, Н4Р2О7 (пирофосфат), Н3РО4 (неорганический фосфат)ицАМФ (циклический АМФ).Вопрос об адениловой системе сводится к процессам распада, синтеза АТФ и ее значению для процессов жизнедеятельности клетки. Главным компонентом адениловой системы клетки являетсяАТФ.Это макроэргическое соединение. Как известно, к макроэргическим относятся соединения, при гидролизе которых высвобождается не менее, чем 5 ккал/моль. В ряду макроэргов клетки АТФ отводится главная роль.
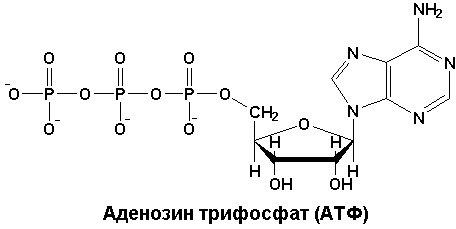
Две фосфоангидридные связи в молекуле АТФ являются макроэргическими.Свободная энергия гидролиза каждой из них равна 7,3 ккал/моль (32 кДж/моль). АТФ обладает высоким потенциалом переноса фосфатных групп на другие вещества (глюкоза, глицерол), тем самым активируя их. С другой стороны, макроэрги, которые имеют больший энергетический потенциал, чем АТФ (например, креатинфосфат), могут переносить свою фосфатную группу на АДФ с образованием АТФ. Таким образом, АТФ занимает центральное положение в ряду других фосфорилированных соединений клетки и является универсальным макроэргом клетки. Это так называемая клеточная энергетическая валюта.
АТФ используется клетками для процессов биосинтеза (анаболические реакции), активации многих молекул (глюкоза, глицерол), выполнения механической работы, переноса веществ через мембраны, обеспечивает точную передачу генетической информации и др. При этом АТФ может гидролизоваться двумя способами:
АТФ + Н2О = АДФ + неорганический фосфат + энергия (32 кДж\моль);
АТФ + Н2О = АМФ + пирофосфат + энергия (32 кДж\моль).
Синтез АТФ носит название фосфорилированияи описывается уравнением:
АДФ + Н3РО4 = АТФ + Н2О.
Эта реакция происходит при условии обеспечения энергией в количестве не менее 32 кДж/моль.
Если источником этой энергии является транспорт электронов по дыхательной цепи внутренней мембраны митохондрий, говорят об окислительном фосфорилировании. Это главный путь синтеза АТФ в аэробных клетках.
Если источником энергии является гидролиз макроэргической связи субстрата, говорят о субстратном фосфорилировании. Такой механизм имеет место в цитозоле и митохондриях и может происходить в анаэробных условиях.
У растений существует фотосинтетическое фосфорилированиев хлоропластах. Источником энергии в данном случае являются кванты солнечного света.
Следует особо подчеркнуть, что процесс окислительного фосфорилированиятесно связан (сопряжен) сокислительно-восстановительными реакциями (ОВР), а именно среакцией окисленияводорода кислородом до воды — тканевым дыханием.Реакция образования водыinvitro(в пробирке) сопровождается одномоментным выделением около 230 кДж /моль энергии и описывается как реакция взрыва гремучего газа. В живой клетке такой путь термодинамически невозможен, поэтому окисление водорода до водыinvivo(в организме) характеризуется двумя важными особенностями.
Во-первых, газообразный водород в клетках не образуется. Он входит в состав субстратов и отделяется от них путем дегидрирования. Ферменты, которые катализируют эти реакции, —дегидрогеназы (ДГ). Это двухкомпонентные ферменты; они делятся напиридиновые (ПДГ),которые в качестве кофермента используют производные витамина РР —НАД+ и НАДФ+, ифлавиновые,которые в качестве кофермента используют производные витамина В2—ФМН и ФАД. В ходе ОВР субстраты окисляются, а коферменты восстанавливаются:
Дегидрогеназа
SH2 S+ восстановленный кофермент(НАДН Н+, НАДФН Н+, ФМН·Н2 , ФАД Н2)
Кофермент
Во-вторых, выделение энергии происходит постепенно, порциями, для чего процесс окисления водорода осуществляется в несколько стадий с участием ферментов дыхательной цепи. Часть этой энергии запасается в виде АТФ в реакции окислительного фосфорилирования.
Восстановленные субстраты, поставляющие атомы водорода для дыхательной цепи, это небольшие молекулы (карбоновые кислоты, кетокислоты, аминокислоты и др.). Основными поставщиками восстановленных субстратов являются центральные метаболические пути — окислительное декарбоксилирование пировиноградной кислоты и цикл лимонной кислоты.Оба локализованы в матриксе митохондрий, в ходе этих процессов происходят реакции декарбоксилирования (большая часть всей углекислоты, образующейся в клетках, образуется именно здесь). Кроме того, как уже говорилось, в ходе этих процессов происходят реакции дегидрирования субстратов, образуются восстановленные коферментные формы НАДН·Н+и ФАДН2, водород которых поступает в дыхательную цепь внутренней мембраны митохондрий, где происходит его окисление кислородом до воды и синтез АТФ.

Переходим к рассмотрению центральных метаболических путей.
