
- •«Расчет насадочной ректификационной колонны непрерывного действия для разделения бинарной смеси толуол - о-ксилол»
- •2007 Оглавление
- •Введение.
- •1.Методика и расчет полной насадочной ректификационной колонны.
- •Равновесие в системах пар-жидкость.
- •1.2 Определение оптимального флегмового числа
- •1.3 Материальный баланс и уравнения рабочих линий.
- •1.3.1. Уравнение рабочей линии для укрепляющей части колонны
- •1.3.2. Уравнение рабочей линии для исчерпывающей части колонны
- •1.4 Расчет скорости пара и диаметра ректификационной колонны
- •1.5 Расчет высоты насадки.
- •1.6 Расчет гидравлических сопротивлений насадки.
- •2.Расчет трубопровода.
- •2.3. Перевод массового расхода жидкости к объёмному
- •2.4. Определение ориентировочного диаметра трубопровода
- •2.5. Выбор стандартного диаметра трубопровода
- •2.7. Определение режима движения жидкости
- •2.8. Определение коэффициента гидравлического сопротивления
- •2.9. Нахождение коэффициентов местных сопротивлений
- •2.10. Определение полной потери напора в трубопроводе
- •2.11. Построение характеристики трубопроводной сети
- •2.12. Выбор насоса
- •Список литературы.
1.Методика и расчет полной насадочной ректификационной колонны.
Исходные данные:
Исходная бинарная смесь – толуол-о-ксилол.
Производительность установки по исходной смеси F=8000кг/ч.
Составы жидкости, масс. доли: Исходной смеси XF=0,7
Дистиллята XP=0,95
Кубового остатка Xw=0,02
Давление Р=0,0999 МПа
Равновесие в системах пар-жидкость.
Парциальное давление пара каждого компонента для идеальных жидких смесей зависит от температуры и пропорционально мольной доле данного компонента в жидкости (закон Рауля):
рнкк=Рнкк*х (1)
рвкк=Рвкк*(1-х) (2)
где рнкк и рвкк – парциальные давления низкокипящего и высококипящего компонентов,Па
Рнкк и Рвкк – упругость или давление насыщенных паров над чистыми компонентами, Па
Х – содержание низкокипящего компонента в жидкости, мольн. доли
Общее давление пара над жидкостью равно сумме парциальных давлений (закон Дальтона)
Р=рнкк+рвкк=Рнкк*х+Рвкк*(1-х) (3)
Решая это уравнение относительно х, получаем
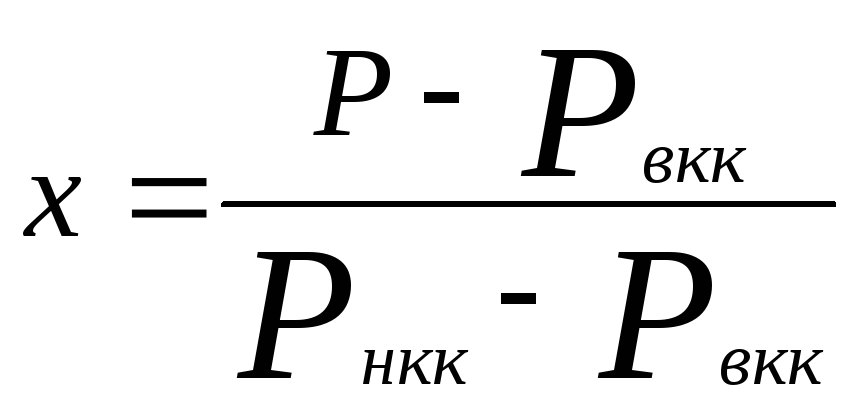 (4)
(4)
Парциальное давление компонента можно получить по закону Дальтона
Рнкк=Р*ункк или Рнкк*х=Р*ункк (5)
Где ункк – содержание низкокипящего компонента в парах, мольн. доли
При совместном решении уравнений (1) и (5) можно получить равновесный состав пара
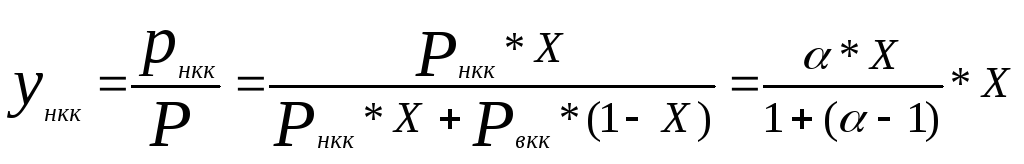 (6)
(6)
Где α - относительная летучесть НКК.
При решении приведенных уравнений строятся следующие графики:
Изобара равновесных составов, называемая кривой равновесия, определяющая равновесные составы пара и жидкости при постоянном давлении (рис.2);
Изобары температур кипения и конденсации, определяющие температуру кипения жидкости и температуру конденсации паров заданного состава (рис3);

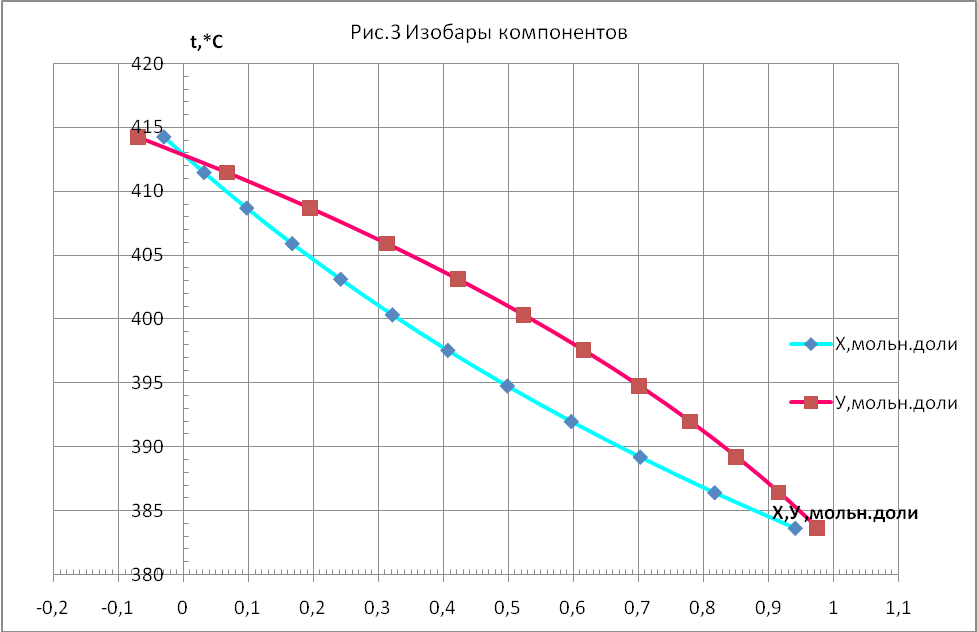
Для построения этих графиков необходимо задаться рядом температур, лежащих между температурами кипения чистого толуола(383,62К) и чистого о-ксилола (417,45К).
Давление паров отдельных компонентов при заданных температурах находятся по уравнению Антуана
![]() (7)
(7)
Где Р – давление паров над чистым компонентом при какой-то температуре,мм.рт.ст
Т – температура,К
А, В,С – эмпирические константы
Таблица 1- Значения констант А, В, С
|
Соединение |
А |
В |
С |
|
толуол |
16,0137 |
3096,52 |
-53,67 |
|
О-ксилол |
16,1156 |
3395,37 |
-59,46 |
![]() ,
Ро-кс=315,08
мм.рт.ст
,
Ро-кс=315,08
мм.рт.ст
При температуре 400,32К давление паров толуола равняется
![]() ,
Рт=1220,79
мм.рт.ст
,
Рт=1220,79
мм.рт.ст
Давления паров толуола и о-ксилола при других температурах в указанном интервале рассчитываются аналогично, и данные заносятся в таблицу 2.
По упругости паров компонентов при различных температурах находятся равновесные составы жидкости (формула 4) и пара (формула 6), причем общее давление берется 749,44 мм.рт.ст (по условию).
Определяем состав смеси, дистиллята и кубового остатка в мольных долях по низкокипящему компоненту по уравнению
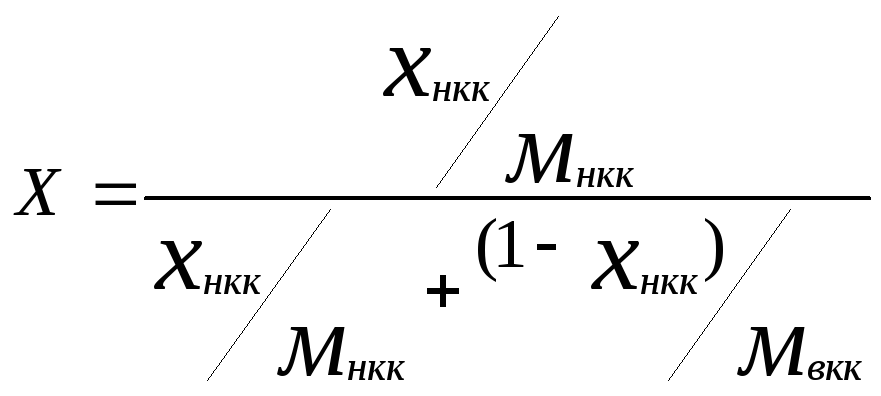 (8)
(8)
Пересчитаем по формуле (8) в мольные доли
Исходное питание XF=
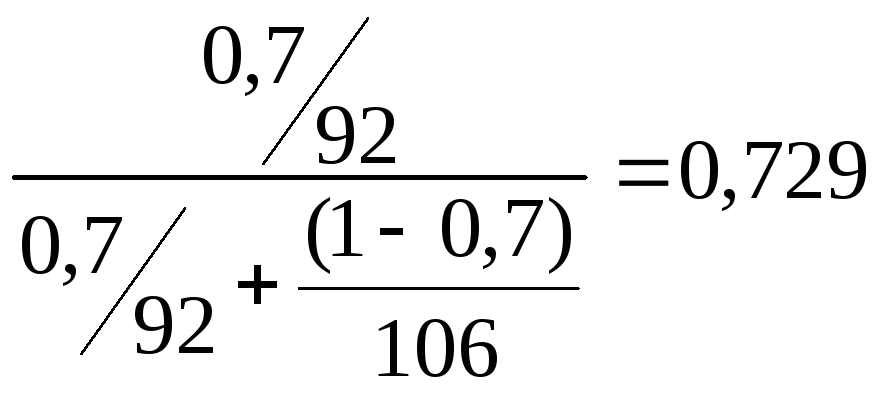

Дистиллят XP=
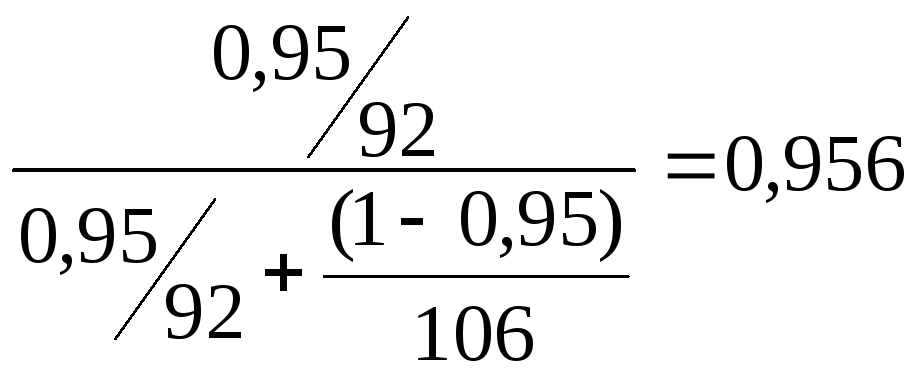
Кубовый остаток Xw=
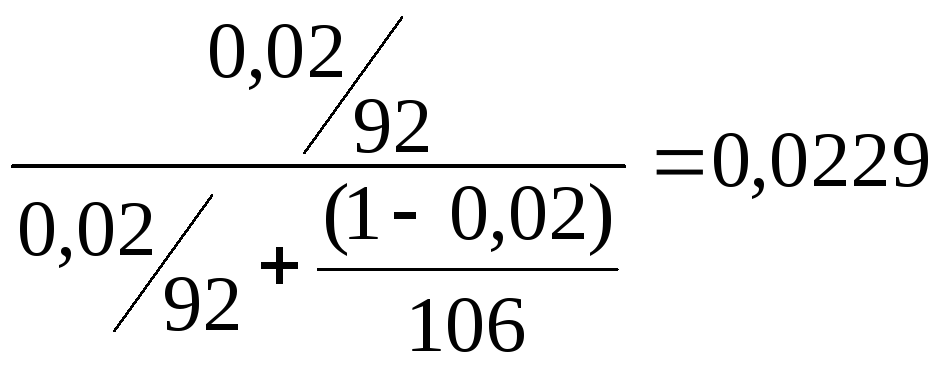
Таблица 2 - Расчет равновесия смеси толуол – о-ксилол.
-
Т
Рнкк,мм.рт ст.
lg PHkk
Рвкк,мм.рт.ст
lgPвкк
Х.мольн.доли
У,мольн.доли
Робщ.мм.рт.ст
383,62
776,801
6,655
315,083
5,753
0,941
0,975
749,44
386,4
840,233
6,734
344,466
5,842
0,817
0,916
749,44
389,19
907,662
6,811
376,023
5,930
0,702
0,851
749,44
391,97
979,258
6,887
409,869
6,016
0,596
0,779
749,44
394,75
1055,193
6,961
446,123
6,101
0,498
0,701
749,44
397,54
1135,643
7,035
484,906
6,184
0,407
0,616
749,44
400,32
1220,785
7,107
526,344
6,266
0,321
0,523
749,44
403,1
1310,801
7,178
570,565
6,347
0,242
0,423
749,44
405,88
1405,872
7,248
617,700
6,426
0,167
0,314
749,44
408,67
1506,184
7,317
667,883
6,504
0,097
0,196
749,44
411,45
1611,925
7,385
721,252
6,581
0,032
0,068
749,44
414,23
1723,283
7,452
777,946
6,657
0,03
0,06
749,44
На основании расчетных данных строятся изобары равновесия х-у и изобары температур кипения и конденсации.
