- •Лабораторные работы по курсу «Материаловедение»
- •Анализ кристаллического строения
- •Задание
- •Контрольные вопросы
- •Испытание материалов на твердость Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Задание
- •Контрольные вопросы
- •Испытание образцов на растяжение Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Задание 1
- •Порядок выполнения работы 1
- •Задание 2
- •Порядок выполнения работы 2
- •Контрольные вопросы
- •Определение ударной вязкости материала Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Задание
- •Порядок выполнения работы 1
- •Порядок выполнения работы 2
- •Контрольные вопросы
- •Фрактографический анализ разрушения металлических материалов Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Изломы, полученные при однократных видах нагружения
- •Изломы, полученные при многократных (циклических) видах нагружения.
- •Задание
- •Контрольные вопросы
- •Влияние холодной пластической деформации и температуры рекристаллизации на структуру и свойства металлов
- •3.2. Влияние температуры рекристаллизации на структуру и свойства холоднодеформированных металлов
- •4. Порядок выполнения работы
- •5. Содержание отчета
- •6. Контрольные вопросы
- •Термический анализ сплавов
- •3.2. Построение диаграмм состояния
- •3.3. Анализ диаграмм состояния
- •Сущность термического анализа
- •3.6 Определение температур кристаллизации Рb, Sb и сплавов Рb-Sb
- •4. Порядок выполнения работы
- •5. Содержание отчета
- •6. Контрольные вопросы
- •Макроскопический анализ (макроанализ) структуры металлических материалов Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Задание
- •Задание
- •Контрольные вопросы
- •Исследование структуры углеродистых сталей в равновесном состоянии методом микроанализа Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Зависимость механических свойств стали от содержания углерода
- •Задание
- •Контрольные вопросы
- •Исследование структуры углеродистых чугунов методом микроанализа Цель работы
- •Приборы, материалы и инструменты
- •Краткие теоретические сведения
- •Влияние скорости охлаждения
- •Задание
- •Контрольные вопросы
- •Закалка углеродистых сталей
- •1. Цель работы
- •2. Приборы, материалы, учебные пособия
- •3. Краткие теоретические сведения
- •4. Порядок выполнения работы
- •5. Содержание отчета
- •6. Контрольные вопросы
- •Отпуск углеродистой стали Цель работы
- •Приборы, материалы и инструмент
- •Краткие теоретические сведения
- •Порядок выполнения задания 1
- •Порядок выполнения задания 2
- •Контрольные вопросы
- •Отжиг и инормализация стали
- •1. Цель работы
- •2. Приборы, материалы, учебные пособия
- •3. Превращение при отжиге
- •4. Порядок выполнения работы
- •5. Содержание отчета
- •6. Контрольные вопросы
- •Химико-термическая обработка стали
- •1. Цель работы
- •2. Приборы, материалы, учебные пособия
- •3. Химико-термическая обработка стали
- •4. Содержание отчета
- •5. Контрольные вопросы
- •Влияние легирующих элементов на прокаливаемость стали, определенную методом торцевой закалки
- •1. Цель работы
- •2. Приборы, материалы и инструмент
- •3. Краткие теоретические сведения
- •4. Задание
- •5. Контрольные вопросы
- •Классификация, маркировка и применение конструкционных материалов
- •1. Цель и задачи работы
- •2. Указания к самостоятельной работе
- •3. Классификация материалов
- •4. Способы маркировки металлических материалов
- •5. Углеродистые стали
- •5.1. Конструкционные углеродистые стали обыкновенного качества общего назначения
- •5.2. Качественные конструкционные углеродистые стали для деталей машин
- •5.3. Инструментальные углеродистые стали
- •6. Маркировка легированных сталей
- •7. Особые способы маркировки сталей
- •7.1. Маркировка сталей для отливок
- •7.2. Маркировка автоматных сталей
- •7.3. Стали для подшипников
- •7.4. Маркировка быстрорежущих сталей
- •7.5. Маркировка строительных сталей
- •7.6. Магнитные стали
- •7.7. Стали специальных способов выплавки
- •7.8. Нестандартные легированные стали
- •8. Чугуны
- •9. Порошковые материалы
- •10. Медь и сплавы на основе меди
- •10.1. Латуни
- •10.2. Бронзы
- •11. Алюминий и сплавы на основе алюминия
- •12. Магний и сплавы на основе магния
- •13. Титан и сплавы на основе титана
- •14. Содержание отчета
- •15. Контрольные вопросы
- •Библиографический список
3.2. Построение диаграмм состояния
Сущность термического метода построения диаграммы состояния сводится к определению критических температур при нагревании или охлаждении металлов и сплавов. Критическими называются температуры, при которых происходят фазовые превращения в сплаве (начало и конец кристаллизации, полиморфные превращения и другие).
В процессе охлаждения сплава (рис. 1) вначале скорость охлаждения велика, затем она уменьшается, т.к. происходит кристаллизация одной из фаз, при которой выделяется некоторое количество тепла. При кристаллизации эвтектики происходит остановка охлаждения (площадка на кривой охлаждения), так как выделяемое тепло, в связи с кристаллизацией двух и более фаз одновременно, полностью компенсирует теплоотвод.
При охлаждении сплавов с различным содержанием компонентов получают ряд кривых, изображающих ход процесса охлаждения сплава.
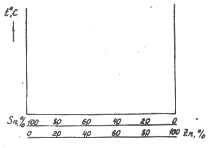
Для двухкомпонентных систем при построении диаграмм по оси ординат откладывается температура, по оси абсцисс – концентрация элементов в сплаве (рис. 2).
|
|
|
|
Рисунок 1 График процесса кристаллизации сплавов |
Рисунок 2 Координатные оси при построении диаграммы состояния сплавов олово-цинк |
Общее содержание компонентов в сплаве 100%, и поэтому каждой точке на диаграмме соответствует определенное содержание компонентов.
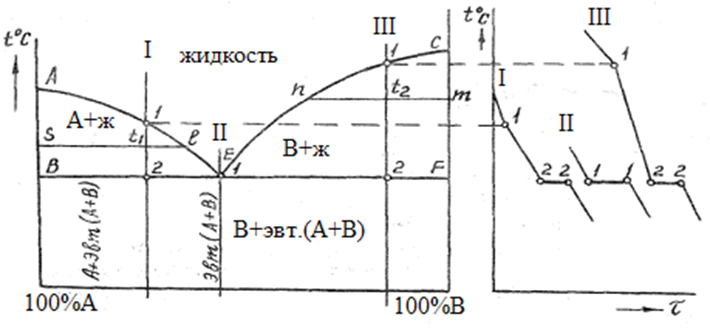
Критические температуры начала и конца кристаллизации, полученные при охлаждении сплавов, переносятся на координатные оси «температура–концентрация». Затем плавными линиями соединяются точки начала и конца кристаллизации сплавов. При наличии эвтектики в сплаве точки конца кристаллизации сплавов располагаются на одной прямой при температуре кристаллизации эвтектики (рис. 3).
Сплавы на диаграмме состояния, располагающиеся до точки эвтектики (слева направо), называются доэвтектическими, соответствующие точке эвтектики – эвтектическими, располагающиеся за точкой эвтектики – заэвтектическими. Структура этих сплавов на примере системы Zn-Sn показана на рисунке 4.
|
|
|
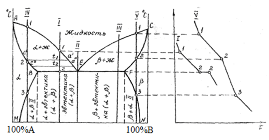
Рисунок 3 Диаграмма состояния сплавов, компоненты которой неограниченно растворимы в жидком состоянии, нерастворимы в твердом и при кристаллизации образуют смесь (эвтектику) |
|
|
|
Рисунок 4 Схематическое изображение структуры системы олово-цинк: а) доэвтектический сплав, олово+эвтектика (Sn+Zn); б) эвтектический сплав, эвтектика (Sn+Zn); в) заэвтектический сплав цинк+эвтектика (Sn+Zn) |
3.3. Анализ диаграмм состояния
По диаграмме состояния можно определить критические точки сплава при нагревании и охлаждении и установить его структуру, выбрать сплав, обладающий наилучшими литейными свойствами, правильно назначить режим термической обработки.
Диаграмма состояния сплавов, компоненты которой неограниченно растворимы в жидком состоянии, нерастворимы в твердом и при кристаллизации образуют эвтектику (рис. 3):
АЕС – ликвидус, начало кристаллизации сплавов.
ВЕF – солидус, конец кристаллизации сплавов; на этой линии происходит одновременная эвтектическая кристаллизация компонентов А и В при постоянной температуре. Линия называется эвтектической.
АЕ – начало кристаллизации компонента А.
ЕС – начало кристаллизации компонента В.
Точка Е называется эвтектической, в ней происходит одновре- менная кристаллизация компонентов при самой низкой и постоянной температуре.
Кристаллизация и структурообразование сплавов (I–III)
Сплав I – доэвтектический. Критическая точка 1 – начало кристаллизации компонента А, две фазы: жидкость и зародыши зерен компонента А.
Критическая точка 2 – кристаллизация эвтектики, т. е. из оставшейся к этой температуре жидкости одновременно кристаллизуются компоненты А и В:
ЖЕ А + В (1)
На кривой охлаждения образуется площадка 2-2. Структура сплава после охлаждения состоит из зерен компонента А и эвтектики.
По мере охлаждения сплава между точками I и 2 жидкость меняет свою концентрацию по линии AЕ. Чтобы определить состав твердой и жидкой фаз при заданной температуре t1 сплава I (рис. 4), необходимо через точку t1 провести коноду, т. е. прямую линию, параллельную оси концентрации, до пересечения с линиями диаграммы и точки пересечения спроектировать на ось концентрации. Точка пересечения l c линией ликвидус покажет концентрацию компонентов А и В в жидкой фазе, точка S – в твердой (чистый компонент А).
Соотношение масс фаз при заданной температуре можно определить по правилу отрезков.
Правило отрезков. Массы фаз относятся между собой как обратная пропорция отрезков коноды. Например, при температуре t1 сплав I имеет 2 фазы: жидкую и твердую с количеством масс QЖ и QТВ, соотношение фаз определится выражением (2), а количество жидкой и твердой фаз – соотношениями (3) и (4):
Qж/Qтв = st1/t1l, (2)
Qж = Рst1/sl, (3)
Qтв = Рt1l/sl, (4)
где Р – общая масса сплава.
Сплав II – эвтектический. Критическая точка Е компоненты А и В кристаллизуются одновременно при постоянной температуре: ЖЕ А + В.
Присутствуют 3 фазы: жидкость эвтектического состава, компоненты А и В. На кривой охлаждения образуется площадка 1-1.
Структура сплава после охлаждения состоит из эвтектики (смеси кристаллов компонентов А и В).
Сплав III – заэвтектический. Критическая точка 1 – начало кристаллизации компонента В. Фазы две: жидкость, кристаллы компонента В. По мере охлаждения сплава жидкость меняет концентрацию по линии ликвидус ЕС. Например, при t2 состав жидкости определится точкой n, спроектированной на ось концентраций, а состав твердой фазы – проекцией точки m.
Критическая точка 2 – кристаллизация эвтектики, т. е. из оставшейся к этой температуре жидкости при постоянной температуре кристаллизуются оба компонента:
ЖЕ А + В.
Структура сплава после охлаждения состоит из зерен компонента В и эвтектики.
Правило фаз Гиббса устанавливает зависимость между числами фаз системы, ее компонентов и степеней свободы:
С = К – Ф + 1, (5)
где С – число степеней свободы, или вариантность системы;
К – число компонентов системы;
Ф – число фаз, находящихся в равновесии в данной критической точке.
Под числом степеней свободы понимается число независимых параметров системы, которые можно изменить, не изменяя равновесия, например, температуру без изменения числа фаз. Так как степень свободы не может быть меньше нуля и дробным числом, то
К – Ф + 1 0 (6)
Ф К + 1(7)
Следовательно, в двойной системе в равновесии может находиться не более трех фаз, в тройной – не более четырех и т. д.
Например, определим число степеней свободы у сплава I в 1-й критической точке (рис. 5):
С = К – Ф + 1, С = 2(А, В) – 2(А, Ж) + 1 = 1,
т. е. с изменением температуры между точками 1-2 число фаз не изменяется, а происходит переход одной фазы (жидкости) в другую (компонент А). Во второй точке
С = К – Ф + 1, С = 2(А, В) – 3(А, В, Ж) + 1 = 0,
т. е. процесс кристаллизации эвтектики идет при постоянной температуре, система нонвариантна. Изменение температуры ведет к изменению количества фаз.
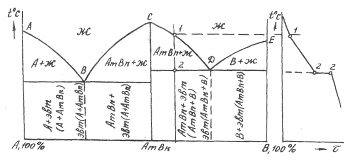
Диаграмма состояния сплавов, компоненты которой растворимы в жидком состоянии, нерастворимы в твердом и при кристаллизации образуют устойчивое химическое соединение (рис. 5).
|
|
|
Рисунок 5 Диаграмма состояний сплавов, компоненты которой неограниченно растворимы в жидком состоянии, нерастворимы в твердом и при кристаллизации образуют устойчивое химическое соединение |
Диаграмма рассматривается как совокупность двух диаграмм состояния, где в роли компонента выступает химическое соединение:
I часть диаграммы – компоненты А и АтВn;
II часть диаграммы – компоненты В и АтВn.
Обе части диаграммы характеризуются неограниченной растворимостью в жидком состоянии. В твердом состоянии они нерастворимы, при кристаллизации образуется эвтектическая смесь, состоящая из кристаллов компонента и химического соединения.
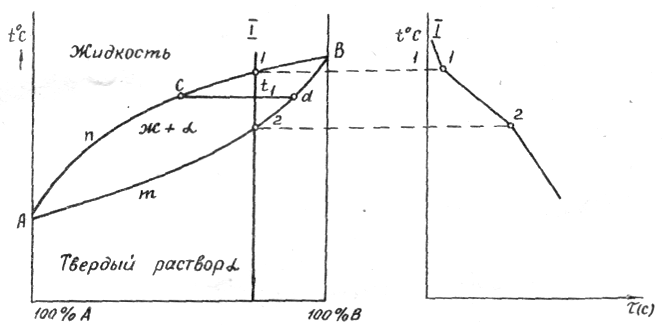
Диаграмма состояний сплавов, компоненты которой неограниченно растворимы друг в друге в жидком и твердом состояниях (рис. 6):
АnВ – ликвидус, начало кристаллизации твердого раствора;
АтВ – солидус, конец кристаллизации твердого раствора.
Кристаллизация и структурообразование сплавов (I)
Критическая точка 1 – начало кристаллизации твердого раствора α:
Ж .
Критическая точка 2 – конец кристаллизации твердого раствора α.
При кристаллизации в интервале температур между точками 1-2 жидкая и твердая фазы изменяют состав. Изменение концентрации жидкости определяется линией ликвидус АnВ, а концентрации твердого раствора – линией солидус АmВ. Например, в сплаве I при температуре t1 состав жидкой фазы соответствует точке c, твердой – точке d, спроектированными на ось концентраций. По правилу отрезков количество твердой фазы
Qтв = Pct1/cd (8)
Структура сплава: зерна однородного твердого раствора α.
|
|
|
Рисунок 6 Диаграмма состояния сплавов, компоненты которой неограниченно растворимы друг в друге в жидком и твердом состояниях |
Диаграмма состояния сплавов, компоненты которой неограничен но растворимы в жидком состоянии, ограниченно – в твердом, при кристаллизации образуют эвтектическую смесь (эвтектику) (рис. 7).
АЕС – ликвидус;
АВЕFС – солидус;
АЕ – начало кристаллизации твердого раствора α;
АВ – конец кристаллизации твердого раствора α;
ЕС – начало кристаллизации твердого раствора β;
СF – конец кристаллизации твердого раствора β;
ВМ – ограничение растворимости компонента В в кристаллической решетке компонента А.
FN – ограничение растворимости компонента А в кристаллической решетке компонента В.
Точки В, F – максимальная растворимость компонентов друг в друге.
Диаграмма отличается от диаграммы (рис. 3) наличием двух областей граничных твердых растворов α и β. Компоненты в чистом виде в сплавах этой системы макроскопически не присутствуют, а находятся только в виде твердых растворов α и β.
Кристаллизация и структурообразование в сплавах, состав которых находится в интервале проекций точек В и F диаграммы (рис. 7) на ось концентраций, происходят аналогично ранее рассмотренным примерам диаграммы с нерастворимыми в твердом состоянии компонентами, только вместо компонентов А и В присутствуют твердые растворы α и β.
Кристаллизация и структурообразование сплавов IV (V)
Критическая точка 1 – начало кристаллизации твердого раствора.α(β), две фазы: жидкость и α(β). В интервале температур между точками 1 и 2 идет кристаллизация:
Ж ().
Критическая точка 2 – конец кристаллизации α(β), в структуре сплава осталась одна фаза – α(β). В интервале температур между точками 2 и 3 – охлаждение твердого раствора α(β). За счет снижения растворимости твердый раствор становится насыщенным. Критическая точка 3 – начало выделения вторичного твердого раствора βII(αII) из пересыщенного твердого раствора α(β) вследствие уменьшения растворимости компонентов при снижении температуры. В интервале температур между точкой 3 и комнатной выделяется вторичный твердый раствор βII(αII). В структуре сплава две фазы:
IV ( + II); V ( + II).
|
|
|
Рисунок 7 Диаграмма состояния сплавов, компоненты которой неограниченно растворимы в жидком состоянии, ограниченно в твердом и при кристаллизации образуют смесь (эвтектику) |