
теплотех
.pdf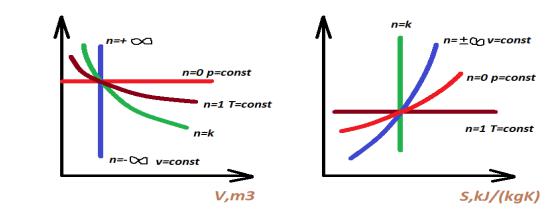
Розділ ІІІ. Ентропія і ентропійні діаграми
Ентропія – калориметричний параметр стану, диференціал якого дорівнює відношенню кількості теплоти в елементарному оборотному процесі до абсолютної температури, що є постійною на нескінченно малій ділянці процесу:
dS = |
|
(3.1) |
|
Одиниця виміру ентропії Дж/К, а одиниця виміру питомої ентропії S, віднесеної до 1 кг речовини, Дж/кг К. У технічній термодинаміці необхідно знати лише зміну питомої ентропії у процесі , яка дорівнює
S1 -S2 =∫ |
|
(3.2) |
|
Загальні формули для розрахунку змін ентропії при протіканні політропного процесу мають вигляд:
S1 |
-S2 = |
|
|
|
n |
|
|
|
n |
|
; |
(3.3) |
|
|
|
|
|
|
|||||||
S1 |
-S2= |
|
|
|
|
|
; |
|
|
(3.4) |
||
|
|
|
|
|
|
|||||||
S1 |
-S2 = |
|
|
|
n |
|
|
; |
|
|
(3.5) |
|
|
|
|
|
|
|
|
||||||
На рисунку приведені процеси в p-v і T-S діаграмах:
Р, Па |
T, K |
|
V, м3 |
|
S, Дж/(кг·К) |
|
|
|
|
|
|
Для основних процесів знаходимо:
ізохорний процес |
S2 –S1 = |
n |
|
|
|
= |
n |
|
|
|
; |
(3.6) |
||||
|
|
|
|
|
|
|||||||||||
ізобарний процес |
S2 –S1 = |
n |
|
|
= |
n |
|
|
|
; |
(3.7) |
|||||
|
|
|
|
|||||||||||||
ізотермічний процес |
S2 –S1 = |
|
|
|
n |
|
= n |
|
|
; |
(3.8) |
|||||
|
|
|
|
|
|
|||||||||||
адіабатичний процес |
S2 –S1 = , |
; |
S=const . |
(3.9) |
||||||||||||
21
Для визначення відносної ентропії приймаємо S0=0 при нормальних
фізичних умовах і тоді ентропія газу буде визначатися по формулах: |
|
|||||||
n |
|
+ n |
|
|
; |
(4.10) |
||
|
|
|
||||||
n |
|
|
n |
|
. |
(4.11) |
||
|
|
|
||||||
В цих формулах р і р0 необхідно брати в однаковій розмірності, при чому |
||||||||
Р0 = 1,033атм = 1,0133бар = 760 мм.рт.ст. =1,01 |
Па |
|||||||
Значення , , R для задач приймають постійними і беруть із додатку І , ІІ, і ІІІ.
3.1. Приклади розв’язування задач
1.Знайти значення ентропії 1 кг кисню при тиску 2бара і температурі 80 . Для рішення використовуємо формулу (4.11) для визначення відносної ентропії
n |
|
|
|
n |
|
|
n |
|
|
|
n |
|
: |
|
|
|
|
|
|
|
|||||||||||
2.3 3 . 5 |
|
|
. 5 |
. 55 |
|
=0.0592 |
|
. |
|||||||
|
. |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. 8м3 повітря , при нормальних фізичних умовах , розширяється політропно |
|||||||||||||||
зі зниженням температури від 60 до -30 |
. Початковий тиск становить 30 атм. |
||||||||||||||
Знайти : показник політропи, роботу розширення і зміну ентропії газу, якщо від нього відведено в процесі 333кДж теплоти.
Для визначення показника політропи скористаємося рівнянням
Q= |
|
|
, |
. , |
. |
||||
|
|||||||||
Роботи |
|
L= |
|
|
|
|
33 |
|
|
|
|
|
|
||||||
Зміни ентропії |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
3. 1кг повітря від початкового стану , який характеризується тиском 10атм і |
|||||||||
температурою 50 , |
ізобарно розширюється |
до v2=2v., |
а потім по адіабаті |
||||||
розширюється ще до v3=3v2. Визначити роботу , зміну внутрішньої енергії і ентропії в цих процесах і сумарно.
Р1=10атм., Т1=323 |
, v1=0,095 |
|
|
|
; |
||
|
|
|
|||||
Р2=10атм., Т2=646 |
, v2=0,19 |
|
|
|
; |
|
|
|
|
|
|||||
Р3=2,16 атм., Т3=417 |
, v3=0,57 |
|
. |
||||
|
|||||||
22 |
|
|
|
|
|
|
|

Ізобарний процес |
3.2 |
|
|
|
, |
|
|
23 .2 |
|
|
|
, |
. |
||
|
|
|
|
|
|
||||||||||
Адіабатний процес |
|
|
|
|
|
, |
|
|
|
|
, |
|
|||
|
|
|
|
|
|
|
|
|
|
||||||
Сумарний процес |
257,2 |
|
|
, |
7,2 |
|
|
, |
. |
||||||
|
|
|
|||||||||||||
3.2.Задачі для самостійної роботи
1.1кг азоту при температурі 50 знаходиться в балоні ємкістю 0,5м3. Знайти його ентропію.
2.1кг вуглекислоти при тиску 2 бар знаходиться в балоні ємкістю 400л. Знайти його ентропію.
3. Порахувати ентропію для 1 кг азоту з температурою 100 при таких тисках: 1,2,3,4,5 бар . Виконати аналіз впливу тиску газу на його ентропію.
4. Як зміниться ентропія 1 кг повітря , якщо його тиск збільшився з 2 до 10бар, а температура знизилась з 400 до 200 . Який це процес? Побудувати його
вр-v діаграмі.
5.4кг азоту політропно розширюють до v2=5v1 , при цьому тиск падає від 8 до 1 бар. Визначити показник політропи і зміну ентропії в цьму процесі.
6.1кмоль вуглекислоти ізобарно при тиску 5 бар збільшив свій об’єм в 2 раза. Початкова температура газу 20 . Визначити роботу розширення, кількість підведеної теплоти і зміни ентропії газу.
7.До 5кг окису вуглецю СО , при постійному тиску, підведено ззовні 600кДж теплоти. Початковий стан газу визначається об’ємом 2 м3 і температурою
17 . |
Визначити тиск, при якому проходить процес , кінцевий об’єм |
і |
||||
температуру, виконану газом роботу і зміну його ентропії. |
|
|
||||
|
|
8. В політропному процесі 1 кг кисню збільшив свою ентропію на 0,127 |
|
, |
||
|
|
|
||||
а його температура піднялась з 27 до 127 . Визначити показник політропи. |
|
|
||||
|
|
9. До 4 кг азоту по ізохорі підведено 300кДж теплоти. Початковий стан газу |
||||
характеризується тиском 4 бар і температурою 20 |
. Визначити об’єм балону, в |
|||||
якому знаходиться газ , зміну ентропії, кінцеву температуру і тиск. |
|
|
||||
|
|
10. Політропний процес 3 кг кисню, визначається ємністю процесу |
С=- |
|||
0,35 |
|
|
. Початковий стан газу характеризується |
тиском 5бар і температурою |
||
|
|
|||||
23
80 .Визначити показник політропи , роботу процеса , зміну внутрішньої |
енергії |
і ентропії , якщо протягом процесу до газу підведено 105 кДж тепла. |
|
11.Початковий стан 1кмоль азоту визначається температурою 10 |
. Як |
зміниться ентропія газу, якщо його температура підніметься на 100 в процесах : ізохорному, ізобарному і адіабатному?
12. 10 м3 суміші при нормальних умовах з об’ємним складом: О2-20 , СО2- 30 , N2-20 ,при тиску 5 атм і температурі 37 , стикається політропно. При цьому тиск піднімається до 10 атм., а температура до 147 .Визначити показник політропи і зміну ентропії суміші. Значення k прийняти рівним 1,38.
13. 5 кг кисню ізотермічно розширюють до v2=3v1, а потім ізобарно стискують до початкового об’єму : початковий стан газу визначається тиском 12 бар і температурою 300 . Визначити параметри газу у всіх трьох точках, роботу, зміну внутрішньої енергії і ентропії.
14. Зобразити на p-v і T-S діаграмах наступні процеси: а) ізобарне стиснення газу в 2 рази; б) ізохорний нагрів з підвищенням температури в 2 рази; в) ізотермічне розширення; г) ізобарне розширення в 2 рази; д) адіабатне розширення.
При нанесені на діаграми процесів необхідно дотримуватись приблизно масштаб параметрів, які змінюються.
15. На p-v і T-S діаграмах зобразити області слідуючих процесів:
а) політропне розширення при 0 |
; |
б) політропне розширення при k |
; |
в) політропне стиснення при 1 |
. |
16. Показати області процесів з від’ємною теплоємністю і по діаграмах пояснити фізичне значення цього.
17. Зобразити області процесів в яких:
а) до газу підводиться теплота , а внутрішня енергія зменшується; б)підводиться теплота, а внутрішня енергія збільшується; в) відводиться теплота, а внутрішня енергія збільшується; г) відводиться теплота, а внутрішня енергія зменшується.
18. 4 кг вуглекислоти розширюється по ізобарі р=6бар зі зміною температури від 27 до 327 , а потім по адіабаті ще розширюється до тиску 2
24

бар. Визначити зміну внутрішньої енергії і ентальпії , роботу, зовнішню теплоту при кожному процесі і сумарне. R=189 , , , ,27.
19. До 10 кг повітря в ізохорному процесі підведено 1885 кДж теплоти, а потім при ізобарному стиснені об’єм зменшили в 2,5 рази. Початкова температура повітря 17 , а тиск 0,8 атм. Розрахувати процеси, які проходять з повітрям і привести їх на p-v діаграми.
20. 1 кг водню і 1 кг кисню розширюють від тиску 5 до 1 атм, початкова
температура обох газів однакова і дорівнює 227 |
. Порівняти |
адіабатну і |
ізотермну роботу розширення газів. Розрахувати цю роботу. |
|
|
21. Стратостат, заповнений гелієм в кількості |
10000м3 при |
15 і 760 |
мм.рт.ст. на землі , піднімається на висоту 22км. На цій висоті тиск повітря становить 0,0402 бар, а температура -56 . Визначити повну підйомну силу стратостата на землі і на вказаній висоті для двох випадків: 1) стратостат піднімається настільки швидко, що можна знехтувати теплообміном з навколишнім середовищем (адіабатне розширення газу) 2) газ при підйомі охолодився до -30 . Допускається, що газ із стратостата через клапан не виходить.
22. Газова турбіна працює на продуктах спалювання, які мають на виході з неї температуру 800 і тиск5атм; розширення турбіни проходить по політропі n= 1,3 до тиску 1атм. Визначити температуру газів на виході, зміну їх об’ємів в процесі і роботу 1 кг продуктів спалювання при розширені їх в турбіні.
R=294 .
23. Суміш із 4 кг кисню і 6 кг азоту адіабатно розширюється до v2=2v1 . Початкові параметри суміші: тиск 10бар, температура 127 . Визначити v1, v2, p2 і T2 , а також роботу розширення і зміну внутрішньої енергії.
24. Продукти спалювання бензину розширюються в ДВС по політропі n=1,27 від 30 до 3 атм. Початкова температура газів 2100 ; масовий склад продуктів спалювання 1 кг бензину слідуючий: СО2=3,125кг , Н2=1,305 кг, О2=0,34кг, N2=12,61кг. Визначити роботу розширення цих газів, якщо подається в циліндр 2 г бензину.
25
Розділ IV. Термодинамічні процеси
Основне рівняння для термодинамічних процесів уявляє собою математичну залежність між трьома величинами: зовнішня теплота (яка підводиться ззовні або відводиться від робочого тіла), зміна внутрішньої енергії і
зовнішня робота газу |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
dq= |
+ |
, |
|
|
|
|
(4.1) |
||||||||
або |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
q= |
+ , |
|
|
|
|
|
|
|
(4.2) |
||||||
де |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
(4.3) |
|
це зміна внутрішньої енергії, а |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
∫ |
, |
|
|
|
|
(4.4) |
|||
це зовнішня робота. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Рівняння політропного процесу має вигляд |
і залежність між |
||||||||||||||||
параметрами газу в процесі слідуючі: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
(4.5) |
|
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
(4.6) |
|
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
(4.7) |
|
Теплота, яка приймає участь в процесі при |
, визначається з |
||||||||||||||||
формули |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
(4.8) |
|
де |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
С= |
|
|
|
|
|
, |
|
|
|
|
|
(4.9) |
|||
|
|
|
|
|
|
|
|
||||||||||
це теплоємність, а |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
, |
|
|
|
|
|
(4.10) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
це показник політропи, де |
|
|
|
|
– розподілення енергії в процесі. |
||||||||||||
|
|
|
|
||||||||||||||
Робота 1 кг газу в політропному процесі виражається формулою |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
( |
|
) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(4.11) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Коли задавати визначені значення показника n , то одержимо часткові випадки політропного процесу:
26

а) ізохорний процес |
|
|
|
|
|
|
|
|
|
|
|
|
|
n= |
|
|
; |
|
|
|
(4.12) |
||||||
б) ізобарний процес |
|
|
|
|
|
|
|
|
|
|
|
|
|
n= |
|
|
; |
|
|
(4.13) |
|||||||
q= |
; |
|
|
|
|
|
|
(4.14) |
|||||
в) ізотермічний процес |
|
|
|
|
|
|
|
|
|
|
|
|
|
n= |
|
n |
|
|
n |
|
|
; |
(4.15) |
||||
|
|
|
|||||||||||
г) адіабатний процес |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
n |
|
|
|
|
|
[ |
( |
|
) ]. |
||||
|
|
|
|
||||||||||
4.1. Приклади розв’язування задач
Загальне зауваження. На діаграмі в координатах p-v зображені основні процеси, які проходять з газом.
У всіх задачах, де не вказані особливі умови, розрахунок потрібно вести для ідеального повітря, зі слідуючими характеристиками: тиск-абсолютний;
R=8.31 |
|
, |
, 5 |
|
, |
, |
2 . |
|
|
1.Від чого відводиться 100кДж; внутрішня енергія його збільшилась на 200 кДж. Що це за процес? Яка робота газу? Чому дорівнює теплоємність
q =-100кДж, 2 , 2, n=1,267, 3
Процес стиснення знаходиться нижче адіабати: теплота, яка одержана від роботи стиснення 300 кДж і розподіляється таким чином: частина іде на збільшення внутрішньої енергії (200кДж), а частина (100кДж) відводиться на
зовні, с=-0,357 . Підведення теплоти
27

2. На p-v діаграмі показати область процесів з від’ємною теплоємністю.
Всі процеси розташовані між ізотермою і адіабатою , оскільки в них, не дивлячись на підведення теплоти ззовні, внутрішня енергія зменшується (температура падає), а при відводі теплоти внутрішня енергія збільшується.
4.2.Задачі для самостійної роботи
1.В процесі газ віддає 200 кДж теплоти,із яких 80кДж взято із внутрішньої енергії. Визначити показник політропи і описати процес, яких проходить з газом.
2.В політропному процесі тиск газу зменшився з 10 до 2 атмосфери, а об’єм його збільшився в 4 рази. Визначити показник політропи і описати фізичні явища в цьому процесі.
3.Показник політропи дорівнює 2. Об’єм газу збільшився в 3 рази. Як змінились тиск і температура газу? Що проходить з газом в цьому процесі?
4.Показник політропи дорівнює 0,5. Газ стиснутий до р2=3р1. Як змінились температура і об’єм газу? Що відбувається з внутрішньою енергією газу? Яка його робота? Який вплив в процесі зовнішньої теплоти?
5.Показати на p-v діаграмі області процесів з від’ємною теплоємністю.
6.1 кг повітря політропно розширюється від початкового тиску 12 до 2 атм, при цьому об’єм його збільшився в 4 рази: початкова температура повітря дорівнює 127 . Визначити показник політропи, початковий і кінцевий об’єми, кінцеву температуру і роботу розширення.
7.5кг повітря стиснуто по політропі з показником n=2 від 1 до 6 атм, початкова температура дорівнює -23 . Визначити роботу стиснення, кінцеву температуру газу, початковий і кінцевий об’єми газу, зміну внутрішньої енергії і ентальпії та кількість зовнішньої теплоти.
8. В циліндрі дизеля повітря з початковими параметрами t1=47 і р=1атм стискається по політропі n=1,96. Стиснення відбувається до досягнення температури повітря 700 , яка дещо перевищує само загорання палива. Визначити кінцевий тиск повітря і необхідну ступінь стиснення : вичислити
роботу стиснення.
9.Порівняти витрати теплоти для нагрівання 5 кг азоту від 27 до 227 при v=const і p=const. Для ізобарного нагрівання визначити роботу розширення. Для азоту прийняти 2 .
28
10. Початковий стан 10 кг повітря визначається температурою 27 і тиском 1,2 бар. Повітря ізобарно нагрівається до 327 . Визначити роботу газу, зміну внутрішньої енергії і ентальпії, кількість підведеної теплоти.
11.10 кг повітря стискають до v2=0,5v1. Початковий стан повітря: t1=57 і р1=1бар. Розрахувати процеси стиснення при показниках політропи: 0; 0,6; 1; 1,2;1,4; 1,6. Показати ці процеси на p-v діаграмі.
12. Початковий стан повітря визначається температурою 127 і тиском 3 бар. Визначити роботу розширення 1кмоль повітря при тиску 1 бар в процесах з показником політропи: 0,5; 1; 1,2; 1,4; 1,6. Знайти зміну внутрішньої енергії і
ентальпії , кількість зовнішнього тепла задіяного в процесі. |
2 |
, |
|
. |
|
||||
13. Процес стиснення 10 кг повітря з t1=127 і |
р1=5бар |
проходить |
по |
|
політропі з показником n=-2; об’єм газу зменшився в 2 рази. Визначити зміну тиску і температури; пояснити фізичні явища, які відбуваються в цих процесах.
29
Література
1.Теплотехніка : підруч./Драганов Б.Х., Бессараб О.С., Долінський А.А. та ін..; за ред. Б.Х. Драганова. -2-ге вид. перероб. І доповн.– К.: ІНОКОС.2005.–400с.
2.Буляндра О.Ф. Теплотехнічна термодинаміка /О.Ф. Булянзра.– К.: Вища шк.,2001.–320с.
3.Андрющенко А.И. Основы термодинамики реальных процессов / А.И.
Андрющенко.–М.: Высшая шк.,1980.–350с.
4. Рабинович О.М. Сборник задач по технической термодинамике / О.М.
Рабинович .– М., «Машиностроение»,1973.–344с.
5. Задачник по технической термодинамике и теории тепломассобмена:
учеб. пособие для энергомашиностроит. спец. вузов/ Афанасьев В.Н., Исаев С.И.,
Кожинов И.А. и др.: под ред. В.И.Крутово и Г.Б. Перажицкого.–М.; Высшая шк.,1986.–383с.
6. Сборник задач по термодинамике и теплопередаче : учеб. пособие для авиационных вузов/ Болгарский А.В., Голдобсев В.И., Идиатуллин Н.С., Толкачев Д.Ф.– М.: Высшая шк.,1972.–304с.
30
