
Методичка БФХ / методичка-1
.docТермодинамические расчёты в биотехнологических процессах
Применение термодинамических закономерностей к биотехнологическим системах представляет теоретический и практический интерес. На основе стехиометрических закономерностей следует оставлять материальный баланс основной стадии процесса – ферментации или ферментативного превращения, а по материальному балансу строиться тепловой баланс. Эти расчёты используются далее для проектировании промышленных производств.
С теоретической точки зрения интересным представляется вопрос об энергетической эффективности потребления субстратов клетками микроорганизмов и оценка на этой основе целесообразности осуществления тех или иных процессов.
Стехиометрия и материальный балансы микробиологических производств
Любой процесс может быть описан стехиометрическим уравнением, связывающим массы исходных веществ и продуктов, основанным на законе сохранения масс. Стехиометрическое уравнение простой химической реакции имеет вид:
|
|
(1), |
где, νi– стехиометрический коэффициент i-го компонента в рассматриваемой реакции;
Mi – молекулярная масса.
Стехиометрические коэффициенты учитывают количество молей каждого из веществ, вступающих во взаимодействие или образующихся в его результате. Стехиометрические коэффициенты продуктов считают положительными, а вещества, вступающие во взаимодействие – отрицательными.
Стехиометрическое уравнение любого химического процесса представляют с собой равенство, в левой и правой частях которого массы различных веществ суммируются таким образом, что бы число грамм-атомов любого элемента слева или справа от знака равенство совпадало.
Стехиометрическое уравнение для общего случая микробиологических процессов, когда популяция микроорганизмов растёт за счёт потребления основного субстрата и вспомогательных веществ, выделяя при этом ряд продуктов имеет вид:
|
|
(2), |
где, Si – питательные вещества – субстраты; Pi – продукты.
Отличия данного уравнения от обычной для химии стехиометрической зависимости объясняется тем, что любые клетка осуществляют одновременно анаболитические и катаболитические процессы. Анаболитические процессы приводят к биосинтезу всех структыр клетки и некоторых важных продуктов (Экхоферментам), но многие из анаболитических реакций – эндэргонические. Это обстоятельство вынуждает клетку одновременно вести катаболитическиее процессы.
Анаболитический процесс можно представить в виде схемы:
|
|
(3), |
Катаболитический процесс:
|
|
(4), |
Для анаэробных процессов:
|
|
(5), |
При описании стехиометрических уравнений на первом этапе рассматривают катаболитические (4;5) и анаболитические (3) процессы, а по их сумме находят брутто-уравнение (2) микробиологического процесса.
Для составления стехиометрического уравнения при биосинтезе необходимо знать не только состав потребляемых исходных веществ, элементарный состав биомассы и состав образующихся в заданном режиме продуктов, ни и количественные характеристики, которые обычно представляют в виде расходных коэффициентов.
Расходные коэффициенты представляют собой отношение массы потреблённого субстрата ΔSi к приросту биомассы (на 1 гр потреб субстрата). На практике используют обратную величину, которую называют экономическим коэффициентом (Y) по данному исходному веществу:
![]() [г/г]
[г/г]
Δx – прирост абсолютной сухой биомассы (АСБ)
Экономический коэффициент показывает эффективность потребления питательной ценности субстрата.
Выход биомассы
Энергетический выход (теоретически возможный выход)
Состав биомассы:
АСВ – абсолютно сухой вес;
АСБ – абсолютно сухая биомасса
Элементарный состав абсолютно сухой биомассы микроорганизмов, определяется природой микроорганизмов и практически одинаков для всех дрожжей, всех бактерий.
АСБ дрожжей содержит по массе 46, 0 % углерода, 6,8 % водорода, 8,8 % азота, 33,1 % кислорода и 5,3 % золы. Элементарный анализ бактерий даёт среднее содержание по массе углерода 48,2 %, водорода 7,2 %, азота 9,7 %, кислорода 27,4 %, золы 7,5 %. Бактериальная масса содержит больше белка и нуклеиновых кислот.
Данные % массового соотношения на 1 г можно представить в виде брутто-формулы:
-
дрожжи
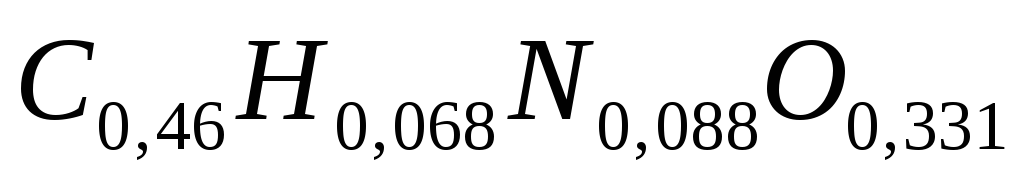
бактерии
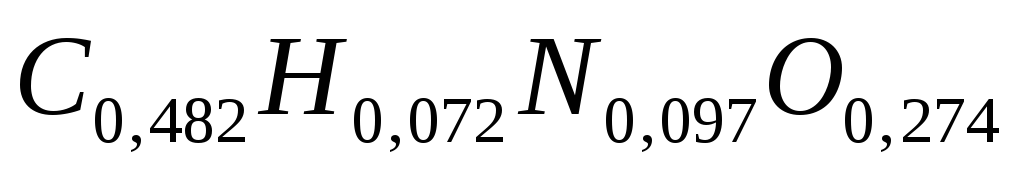
Данные брутто-формулы состава получаемой биомассы можно пересчитать из расчёта на 1 атом углерода:
-
дрожжи
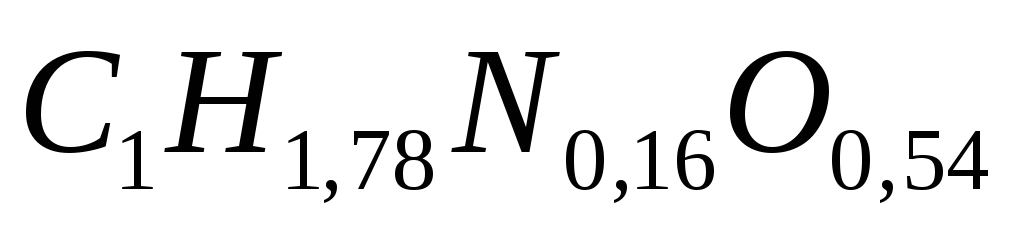
бактерии
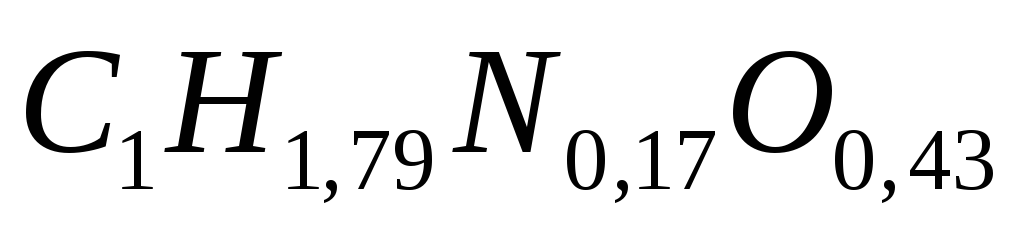
При написании стехиометрических уравнений используют выражение образующейся биомассы в массовом соотношении.
Для характеристики запаса энергии субстрата
Степень восстановленности (энергетическая ёмкость) η (на 1 моль вещества) запас электронов
![]()
η = 4·x+1·y-2·z-3·t
Доступные электроны. Степень восстановленности γ является величиной, несущей в себе связь балансов вещества и энергии. Что бы понять её смысл, запишем уравнение окисления органического вещества кислородом:
![]() (123454)
(123454)
, где γ = 4 + y - 2·z - 3·t
Здесь
![]()
![]() может
быть индивидуальным органическим
соединением либо их смесью, в том числе
биомассой клеток.
может
быть индивидуальным органическим
соединением либо их смесью, в том числе
биомассой клеток.
Аммиак в качестве продукта реакции выбран потому, что 1) он весьма часто является источником азота для роста, 2) азот в нём находится в электронной форме, близкой к той, которую он имеет в большей части макромолекул биомассы.
Если окисление происходит чисто химическим путём, то весь запас энергии органического вещества превращается в тепло. При биохимическом окислении с участием электрон-транспортных путёй часть энергии сохраняется в промежуточных носителях, а затем используется клеткой. Таким образом, процесс (123454) является способом оценки общего количества биологически доступной энергии, заключённой в органических веществах.
Согласно (123454), количество потреблённого
кислорода пропорционально γ, а выделившаяся
энергия пропорциональна кислороду (с
приблизительно постоянным коэффициентом),
то γ оценивает запас энергии вещества
![]() в расчёте на 1 грамм-атом его углерода.
в расчёте на 1 грамм-атом его углерода.
Схема (123454) не рассматривает детали процесса преобразования энергии в электрон-транспортных цепях, она предназначена лишь для оценки энергетического запаса субстрата окисления. При умножении числа доступных электронов на их энергетическую цену в органических веществах получается оценка запаса энергии в этом веществе, могущей быть использованной в аэробном метаболизме, достаточно близкая к реальной.
Максимально достижимый (теоретический) выход биомассы:
![]()
Наиболее часто в биохимии и динамике клеточных популяции используются два термодинамических потенциала – энтальпия H и свободная энергия Гиббса G, которые описывают, соответственно тепловыделение и химическое равновесии реакции при постоянных температуре и давлении.
В химии принята единая система отсчёта для значений этих величин. По соглашению, их нулевые значения приписываются простым веществам. Любое химическое соединение рассматривается как образованное из простых веществ в формальной реакции образования, и изменение термодинамического потенциала в ходе такой реакции считается потенциалом образования этого соединения.
Как простые вещества, так и образованное соединение должны быть в строго заданном стандартном состоянии – при температуре 25 °С (298,15 К), давлении 1 атм. Кристаллическое вещество должно быть в заданной кристаллической модификации. Рассматривается также водное стандартное состояние – раствор в воде при рН 0 и одномолярной концентрации растворённого вещества (моль/кг растворителя). Соответственно, потенциалы H и G, определённые таким образом, являются стандартными энтальпией H0 и свободной энергией G0 образования данного химического соединения. (ПРИЛОЖЕНИе)
(NH4OH не учитывают при расчётах)
ΔG считается только для катаболизма, ΔН только для брутто-процесса
Примеры решения задач.
Задача 1.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – н-С2Н5ОН, а состав получаемой биомассы – C0,460H0,068N0,088O0,331. Если известно, что при культивировании данного штамма микроорганизма на питательной среде, содержащей в качестве источника азота NH4OH, углерода – глюкозу экономический коэффициент составляет 0,4. При решении задачи в качестве допущения примите, что энергия диссипации при культивировании микроорганизмов не зависит от источника углерода, а определяется только видом микроорганизма. Для решения задачи воспользуйтесь справочными данными термодинамических величин.
Решение:
1. Составим уравнение анаболизма культивирования дрожжей на глюкозе.
C6H12O6 + NH4OH → C0,460H0,068N0,088O0,331 + O2 + H2O
Уравняем углерод с левой и правой стороны в уравнении реакции. Поскольку в приведенной формуле состава биомассы нижние индексы соответствуют массовым долям элементов в составе биомассы, а расчеты необходимо выполнять на 1 г АСБ (абсолютно сухой биомассы), то
в 1 г АСБ: m(С)=0,460 г,
m(Н)=0,068 г,
m(N)=0,088 г,
m(O)=0,331 г.
Определим коэффициент, который необходимо поставить перед глюкозой (расчеты производятся с точностью до пятого знака после запятой):
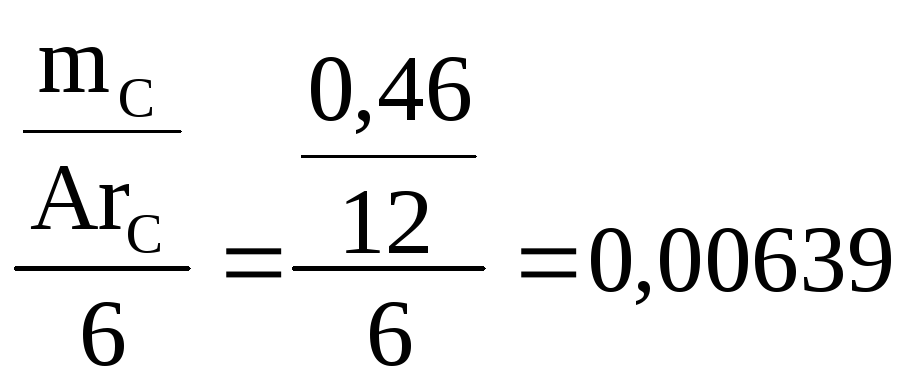 ,
где ArC
– относительная атомная масса углерода,
6 - количество атомов углерода в 1 моль
глюкозы. Таким образом
,
где ArC
– относительная атомная масса углерода,
6 - количество атомов углерода в 1 моль
глюкозы. Таким образом
0,00639 C6H12O6 + NH4OH → C0,460H0,068N0,088O0,331 + O2 + H2O.
Аналогично определяем коэффициент перед аммиаком:
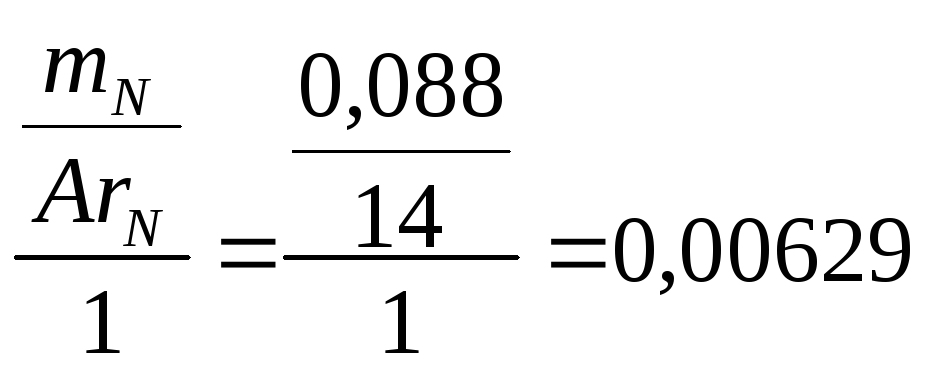 .
.
0,00639 C6H12O6 + 0,00629 NH4OH → C0,460H0,068N0,088O0,331 + O2 + H2O.
При уравнивании водорода учитываем водород во всех соединениях и определяем коэффициент перед водой.
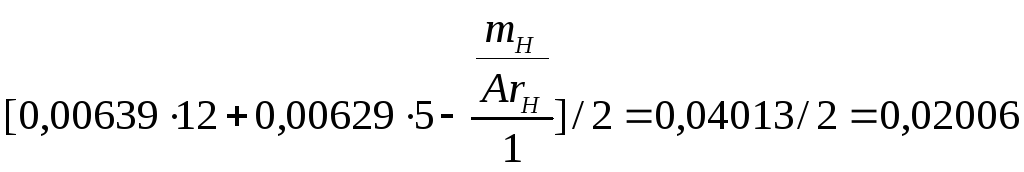 .
.
0,00639 C6H12O6 + 0,00629 NH4OH → C0,460H0,068N0,088O0,331 + O2 + 0,02006 H2O.
Определим коэффициент перед кислородом:
![]() .
.
Уравнение анаболизма:
0,00639 C6H12O6 + 0,00629 NH4OH → C0,460H0,068N0,088O0,331 + 0,00194 O2 + 0,02006 H2O
Составим уравнение катаболизма. Исходя из экономического коэффициента определим количество глюкозы, которое пошло на катаболизм.
![]() ,
тогда
,
тогда
![]() ,
а
,
а
![]() ,
следовательно
,
следовательно
![]() моль (180 – молярная масса глюкозы).
моль (180 – молярная масса глюкозы).
Уравнение катаболизма:
0,00750 C6H12O6 + 0,04500 О2 → 0,04500 CO2 + 0,04500 H2O.
Брутто-реакция:
0,01389 C6H12O6 + 0,00629 NH4OH + 0,04306 О2 → C0,460H0,068N0,088O0,331 +
+ 0,04500 CO2 + 0,06506 H2O.
Рассчитаем ∆Gбрутто-реакции (∆G(NH4OH) – принебрегаем в соответствии с правилами стехиометрических расчетов):
![]() Из
справочника:
Из
справочника:
ΔG0образ (СО2)газ= -394,37 кДж/моль,
ΔG0образ (Н2О)жид= -237,23 кДж/моль,
ΔG0образ (C6Н12О6)р-р= -916,67 кДж/моль. Тогда
![]()
![]()
2. Составим уравнение анаболизма культивирования дрожжей на этаноле (аналогично описанному ранее).
0,01917 C2H5OН + 0,00629 NH4OH + 0,03447 O2 → C0,460H0,068N0,088O0,331 +0,03924 H2O
Составим уравнение катаболизма, поскольку экономический коэффициент неизвестен, примем, что на реакцию будет израсходовано х моль этанола:
х C2H5OН + 2х О2 → 2х CO2 + 3х H2O.
Брутто-реакция:
(0,01917+2х) C2H5OН + 0,00629 NH4OH + (0,03447+2х) O2 →
→ C0,460H0,068N0,088O0,331 + 2х CO2 + (0,03924+3х) H2O
Рассчитаем ∆Gбрутто-реакции (∆G(NH4OH) – принебрегаем в соответствии с правилами стехиометрических расчетов):
![]() Из
справочника:
Из
справочника:
ΔG0образ (СО2)газ= -394,37 кДж/моль,
ΔG0образ (Н2О)жид= -237,23 кДж/моль,
ΔG0образ (C2H5ОН)= -174,15 кДж/моль
![]()
![]()
По условию задачи энергия диссипации при культивировании микроорганизмов не зависит от источника углерода, а определяется только видом микроорганизма. Это позволяет нам приравнять ∆G одной и другой брутто-реакций. Тогда
![]()
![]() ,
а следовательно х=0,01256.
,
а следовательно х=0,01256.
Уравнение катаболизма:
0,01256 C2H5OН + 0,02512 О2 → 0,02512 CO2 + 0,03768 H2O.
Брутто-реакция:
(0,04429 C2H5OН + 0,00629 NH4OH + 0,05959 O2 →
→ C0,460H0,068N0,088O0,331 + 0,02512 CO2 + 0,07692 H2O.
Ответ:
уравнение анаболизма: 0,01917 C2H5OН + 0,00629 NH4OH + 0,03447 O2 → C0,460H0,068N0,088O0,331 + 0,03924 H2O,
уравнение катаболизма: 0,01256 C2H5OН + 0,02512 О2 → 0,02512 CO2 +
+ 0,03768 H2O,
брутто-реакция: (0,04429 C2H5OН + 0,00629 NH4OH + 0,05959 O2 →
→ C0,460H0,068N0,088O0,331 + 0,02512 CO2 + 0,07692 H2O.
Задача 2
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, при анаэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – глюкозу, если известно, что Y= 0,05, а брожение осуществляется по спиртовому пути, состав получаемой биомассы – СН1,78N0,16О0,54.
Решение:
Составим уравнение анаболизма культивирования дрожжей на глюкозе.
C6H12O6 + NH4OH → СН1,78N0,16О0,54+ O2 + H2O
Уравняем углерод с левой и правой стороны в уравнении реакции. Поскольку состав биомассы приведен из расчета на один атом С, предварительно вычислим молярную массу АСБ.
М(АСБ)=112+1,781+0,1614+0,5416=24,66 г/моль.
Поскольку расчеты необходимо выполнять на 1 г АСБ (абсолютно сухой биомассы), то перед АСБ поставим коэффициент равный 1/М(АСБ)=1/24,66=0,04055.
C6H12O6 + NH4OH → 0,04055 СН1,78N0,16О0,54+ O2 + H2O
Определим коэффициент, который необходимо поставить перед глюкозой (расчеты производятся с точностью до пятого знака после запятой):
0,04055/6=0,00676, где 6 - количество атомов углерода в 1 моль глюкозы. Аналогично определяем коэффициент перед аммиаком. Таким образом
0,00676C6H12O6 + 0,00649 NH4OH → 0,04055 СН1,78N0,16О0,54+ O2 + H2O
При уравнивании водорода учитываем водород во всех соединениях и определяем коэффициент перед водой.
(0,0067612+0,006495-0,040551,78)/2=0,02070
0,00676C6H12O6 + 0,00649 NH4OH → 0,04055 СН1,78N0,16О0,54+ O2 +
+ 0,02070 H2O
Определим коэффициент перед кислородом:
(0,006766+0,006491-0,040550,54-0,020701)/2=0,00223.
Уравнение анаболизма:
0,00676 C6H12O6 + 0,00649 NH4OH → 0,04055 СН1,78N0,16О0,54+ 0,00223 O2 +
+ 0,02070 H2O.
Составим уравнение катаболизма. Исходя из экономического коэффициента определим количество глюкозы, которое пошло на катаболизм.
![]() ,
тогда
,
тогда
![]() ,
а
,
а
![]() ,
следовательно
,
следовательно
![]() моль (180 – молярная масса глюкозы).
моль (180 – молярная масса глюкозы).
Но поскольку в анаболизме кислород выделяется, а процесс, как указано в условии, анаэробный, то реакций катаболизма будет две. В первом уравнении кислород (0,00223 моль) будет расходоваться:
0,00037 C6H12O6 + 0,00223 О2 → 0,00223 CO2 + 0,00223 H2O.
Таким образом ∆Sкатаболизм, которое пойдет на образование спирта составит
0,10435-0,00037=0,10398 моль.
0,10398 C6H12O6 → 0,20796 С2Н5ОН + 0,20796 CO2
Суммарное уравнение катаболизма:
0,00037 C6H12O6 + 0,00223 О2 → 0,20796 С2Н5ОН + 0,21019 CO2 + 0,00223 H2O.
Брутто-реакция:
0,10435 C6H12O6 + 0,00649 NH4OH → 0,04055 СН1,78N0,16О0,54 +
+ 0,20796 С2Н5ОН + 0,21019 CO2 + 0,02293 H2O.
Ответ: уравнение анаболизма: 0,00676 C6H12O6 + 0,00649 NH4OH →
→ 0,04055 СН1,78N0,16О0,54+ 0,00223 O2 + 0,02070 H2O,
уравнение катаболизма: 0,00037 C6H12O6 + 0,00223 О2 → 0,20796 С2Н5ОН +
+ 0,21019 CO2 + 0,00223 H2O,
брутто-реакция: 0,10435 C6H12O6 + 0,00649 NH4OH →
→ 0,04055 СН1,78N0,16О0,54 + 0,20796 С2Н5ОН + 0,21019 CO2 + 0,02293 H2O.
Задачи
Задача 1.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔG0 и ΔН0 при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – пропанол, если известно, что Y=0,45, если состав получаемой биомассы из расчета на 1 атом С – СН1,78N0,16О0,54.
Задача 2.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔН0 при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – этанол, если известно, что брутто-реакция культивирования данного микроорганизма на глюкозе в анаэробных условиях может быть описана следующим уравнением:
0,04762 C6H12O6 + 0,00630 NH4OH → C0,460H0.068N0,088O0,331 + 0,08180 C2H5OH + 0,08376 CO2 + 0,02196 H2O.
ОБОСНУЙТЕ ПОДХОД К РЕШЕНИЮ ЗАДАЧИ.
Задача 3.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔG0 и ΔН0 при аэробном культивировании биомассы бактерий на питательной среде, содержащей в качестве источника азота NH4OH, углерода – бутанол, если известно, что Y=0,40, если состав получаемой биомассы из расчета на 1 атом С – СН1,66N0,14О0,48.
Задача 4.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, при спиртовом брожении дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – глюкозу, если известно, что Y=0,10, а состав получаемой биомассы из расчета на 1 атом С – СН1,78N0,16О0,54.
Задача 5.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔG0 и ΔН0 при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – пентанол, если известно, что Y=0,50, если состав получаемой биомассы из расчета на 1 атом С – СН1,78N0,16О0,54.
Задача 6.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔН0 при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – уксусную кислоту, если известно, что брутто-реакция культивирования данного микроорганизма на сахарозе в аэробных условиях может быть описана следующим уравнением:
0,01089 C6H12O6 + 0,00682 NH4OH + 0,02500 О2 → C0,460H0,068N0,088O0,331 + 0,02700 CO2 + 0,04700 H2O.
ОБОСНУЙТЕ ПОДХОД К РЕШЕНИЮ ЗАДАЧИ.
Задача 7.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔН0 при аэробном культивировании биомассы дрожжей на питательной среде, содержащей в качестве источника азота NH4OH, углерода – уксусную кислоту, если известно, что брутто-реакция культивирования данного микроорганизма на глюкозе в аэробных условиях может быть описана следующим уравнением:
0,01089 C6H12O6 + 0,00682 NH4OH + 0,02500 О2 → C0,460H0,068N0,088O0,331 + 0,02700 CO2 + 0,04700 H2O.
ОБОСНУЙТЕ ПОДХОД К РЕШЕНИЮ ЗАДАЧИ.
Задача 8.
Составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, при анаэробном культивировании биомассы бактерий на питательной среде, содержащей в качестве источника азота NH4OH, углерода – глюкозу, если известно, что Y=0,10, а брожение осуществляется по гетероферментативному пути (продукты – молочная и уксусная кислоты – С3Н6О3 и С2Н4О2), состав получаемой биомассы из расчета на 1 атом С – СН1,66N0,14О0,48.
Домашняя работа № 3: «Составление материального баланса
культивирования микроорганизмов»
Используя данные, соответствующие вашему варианту и приведенные в таблице, составьте уравнение реакции катаболизма, анаболизма, брутто-реакции, а также определите ΔG0 и ΔН0 при аэробном культивировании биомассы «А» на питательной среде, содержащей в качестве источника азота NH4OH, углерода – «Б», а состав получаемой биомассы – «В». Если известно, что при культивировании данного штамма микроорганизма на питательной среде, содержащей в качестве источника азота NH4OH, углерода – глюкозу экономический коэффициент составляет «Г». При решении задачи в качестве допущения примите, что энергия диссипации при культивировании микроорганизмов не зависит от источника углерода, а определяется только видом микроорганизма. Для решения задачи воспользуйтесь справочными данными термодинамических величин.
|
№ варианта |
«А» |
«Б» |
«В» |
«Г» |
|
1 |
Бактерий |
н-С1Н3ОН |
СН1,66N0,14О0,48 |
0,35 |
|
2 |
Бактерий |
н-С2Н5ОН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
3 |
Бактерий |
н-С3Н7ОН |
СН1,66N0,14О0,48 |
0,45 |
|
4 |
Дрожжей |
н-С4Н9ОН |
СН1,78N0,16О0,54 |
0,50 |
|
5 |
Бактерий |
н-С5Н11ОН |
СН1,66N0,14О0,48 |
0,55 |
|
6 |
Дрожжей |
н-С6Н13ОН |
C0,460H0,068N0,088O0,331 |
0,35 |
|
7 |
Бактерий |
н-С7Н15ОН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
8 |
Дрожжей |
н-С8Н17ОН |
СН1,78N0,16О0,54 |
0,45 |
|
9 |
Бактерий |
н-С9Н19ОН |
С0,488Н0,067N0,080О0,312 |
0,50 |
|
10 |
Дрожжей |
н-С10Н21ОН |
C0,460H0,068N0,088O0,331 |
0,55 |
|
11 |
Бактерий |
н-С11Н23ОН |
СН1,66N0,14О0,48 |
0,35 |
|
12 |
Бактерий |
н-С12Н25ОН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
13 |
Бактерий |
н-С13Н27ОН |
СН1,66N0,14О0,48 |
0,45 |
|
14 |
Дрожжей |
н-С14Н29ОН |
СН1,78N0,16О0,54 |
0,50 |
|
15 |
Бактерий |
н-С15Н31ОН |
СН1,66N0,14О0,48 |
0,55 |
|
16 |
Дрожжей |
н-С16Н33ОН |
C0,460H0,068N0,088O0,331 |
0,35 |
|
17 |
Бактерий |
н-С17Н35ОН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
18 |
Дрожжей |
н-С18Н37ОН |
СН1,78N0,16О0,54 |
0,45 |
|
19 |
Бактерий |
н-С19Н39ОН |
С0,488Н0,067N0,080О0,312 |
0,50 |
|
20 |
Дрожжей |
н-С20Н41ОН |
C0,460H0,068N0,088O0,331 |
0,55 |
|
21 |
Бактерий |
н-НСООН |
СН1,66N0,14О0,48 |
0,35 |
|
22 |
Бактерий |
н-СН3СООН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
23 |
Бактерий |
н-С2Н5СООН |
СН1,66N0,14О0,48 |
0,45 |
|
24 |
Дрожжей |
н-С3Н7СООН |
СН1,78N0,16О0,54 |
0,50 |
|
25 |
Бактерий |
н-С4Н9СООН |
СН1,66N0,14О0,48 |
0,55 |
|
26 |
Дрожжей |
н-С5Н11СООН |
C0,460H0,068N0,088O0,331 |
0,35 |
|
27 |
Бактерий |
н-С6Н13СООН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
28 |
Дрожжей |
н-С7Н15СООН |
СН1,78N0,16О0,54 |
0,45 |
|
29 |
Бактерий |
н-С8Н17СООН |
С0,488Н0,067N0,080О0,312 |
0,50 |
|
30 |
Дрожжей |
н-С9Н19СООН |
C0,460H0,068N0,088O0,331 |
0,55 |
|
31 |
Бактерий |
н-С10Н21СООН |
СН1,66N0,14О0,48 |
0,35 |
|
32 |
Бактерий |
н-С11Н23СООН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
33 |
Бактерий |
н-С12Н25СООН |
СН1,66N0,14О0,48 |
0,45 |
|
34 |
Дрожжей |
н-С13Н27СООН |
СН1,78N0,16О0,54 |
0,50 |
|
35 |
Бактерий |
н-С14Н29СООН |
СН1,66N0,14О0,48 |
0,55 |
|
36 |
Дрожжей |
н-С15Н31СООН |
C0,460H0,068N0,088O0,331 |
0,35 |
|
37 |
Бактерий |
н-С16Н33СООН |
С0,488Н0,067N0,080О0,312 |
0,40 |
|
38 |
Дрожжей |
н-С17Н35СООН |
СН1,78N0,16О0,54 |
0,45 |
|
39 |
Бактерий |
н-С18Н37СООН |
С0,488Н0,067N0,080О0,312 |
0,50 |
|
40 |
Дрожжей |
н-С19Н39СООН |
C0,460H0,068N0,088O0,331 |
0,55 |
