
- •Пожарная безопасность
- •§ 1.1. Аппараты с неподвижным уровнем жидкости
- •§ 1.2. Аппараты с подвижным уровнем жидкости
- •§ 1.3. Аппараты с газом
- •§ 1.4. Аппараты с пылями, порошками и волокнами
- •Глава 2. Выход горючих веществ наружу из нормально действующих аппаратов
- •§ 2.1. Аппараты с открытой поверхностью испарения
- •§ 2.2. Аппараты с дыхательными устройствами
- •§ 2.3. Аппараты периодического действия
- •§ 2.4. Выход пыли в помещение
- •Глава 3. Выход горючих веществ наружу из поврежденного технологического оборудования
- •§ 3.1. Характеристика аварийной ситуации
- •§ 3.2. Локальное и полное повреждение аппаратов
- •§ 3.3. Ограничение утечек горючих веществ
- •§ 3.4. Образование взрывоопасной смеси в помещении и на открытой площадке
- •Глава 4. Причины повреждения технологического оборудования
- •§ 4.1. Основы прочности и классификация причин повреждения оборудования
- •§ 4.2. Повреждения технологического оборудования в результате механических воздействий
- •§ 4.3. Повреждения технологического оборудования в результате температурного воздействия
- •§ 4.4. Повреждения технологического оборудования в результате химического воздействия
- •Защита от коррозии
- •Глава 5. Производственные источники зажигания
- •§ 5.1. Понятие источника зажигания
- •§ 5.2. Открытый огонь, раскаленные продукты горения и нагретые ими поверхности — производственные источники зажигания
- •§ 5.3. Тепловое проявление механической энергии как производственный источник зажигания
- •§ 5.4. Тепловое проявление химических реакций — производственный источник зажигания
- •§ 5.5. Тепловое проявление электрической энергии — производственный источник зажигания
- •Глава 6. Подготовка оборудования к ремонтным огневым работам
- •§ 6.1. Использование естественной вентиляции оборудования перед проведением ремонтных огневых работ
- •§ 6.2. Использование принудительной вентиляции оборудования перед проведением ремонтных огневых работ
- •§ 6.3. Пропаривание аппаратов перед проведением ремонтных огневых работ
- •§ 6.4. Промывка аппаратов водой и моющими растворами перед проведением ремонтных огневых работ
- •§ 6.5. Флегматизация среды в аппаратах инертными газами — способ подготовки их к проведению ремонтных огневых работ
- •§ 6.6. Заполнение аппаратов пеной при проведении ремонтных огневых работ
- •§ 6.7. Организация ремонтных огневых работ
- •Раздел второй. Предотвращение распространения пожара
- •Глава 7. Ограничение количества горючих веществ и материалов, обращающихся в технологическом процессе
- •§ 7.1. Выбор технологической схемы производства
- •§ 7.2. Режим эксплуатации технологического процесса производства
- •Производства,их удаление
- •§ 7.4. Замена горючих веществ, обращающихся в производстве, негорючими
- •§ 7.5. Аварийный слив жидкостей
- •§ 7.6. Аварийный выпуск горючих паров и газов
- •Глава 8. Огнезадерживающие устройства на производственных коммуникациях
- •§ 8.1. Сухие огнепреградители
- •Расчет огнепреградителя по методу я. Б. Зельдовича
- •§ 8.2. Жидкостные огнепреградители (гидрозатворы)
- •§ 8.3. Затворы из твердых измельченных материалов
- •§ 8.4. Автоматические заслонки и задвижки
- •§ 8.5. Защита трубопроводов от горючих отложений
- •§ 8.6. Изоляция производственных помещений от траншей и лотков с трубопроводами
- •Глава 9. Защита технологического оборудования и людей от воздействия опасных факторов пожара
- •§ 9.1. Опасные факторы пожара
- •§ 9.2. Защита людей и технологического оборудования от теплового воздействия пожара
- •§ 9.3. Защита технологического оборудования от разрушений при взрыве
- •§ 9.4. Защита людей и технологического оборудования от агрессивных сред
- •Пожарная профилактика основных
- •§ 10.2. Пожарная профилактика процессов измельчения твердых веществ
- •§ 10.3. Пожарная профилактика процессов механической обработки древесины и пластмасс
- •§ 10.4. Замена л вж и гж пожаробезопасными моющими средствами в технологических процессах обезжиривания и очистки поверхностей
- •Глава 11. Пожарная профилактика средств транспортировки и хранения веществ и материалов
- •§ 11.1. Пожарная профилактика средств перемещения горючих жидкостей
- •§ 11.2. Пожарная профилактика средств перемещения и сжатия газов
- •§ 11.3. Пожарная профилактика средств перемещения твердых веществ
- •§ 11.4. Пожарная профилактика технологических трубопроводов
- •§ 11.5. Пожарная профилактика хранения горючих веществ
- •Глава 12. Пожарная профилактика процессов нагревания и охлаждения веществ и материалов
- •§ 12.1. Пожарная профилактика процесса нагревания водяным паром
- •§ 12.2. Пожарная профилактика процесса нагревания горючих веществ пламенем и топочными газами
- •§ 12.3. Пожарная профилактика теплопроизводящих установок, используемых в сельском хозяйстве
- •§ 12.4. Пожарная профилактика процесса нагревания высокотемпературными теплоносителями
- •Глава 13. Пожарная профилактика процесса ректификации
- •§ 13.1. Понятие процесса ректификации
- •§ 13.2 Ректификационные колонны: их устройство и работа
- •§ 13.3. Принципиальная схема непрерывно действующей ректификационной установки
- •§ 13.4. Особенности пожарной опасности процесса ректификации
- •§ 13.5. Пожарная профилактика процесса ректификации
- •Пожаротушение и аварийное охлаждение ректификационной установки
- •Глава 14. Пожарная профилактика процессов сорбции и рекуперации
- •§ 14.1. Пожарная опасность процесса абсорбции
- •§ 14.2. Пожарная профилактика процессов адсорбции и рекуперации
- •Возможные пути распространения пожара
- •Глава 15. Пожарная профилактика процессов окраски и сушки веществ и материалов
- •§ 15.1. Пожарная опасность и профилактика процесса окраски
- •Окраска окунанием и обливанием
- •Окраска в электрическом поле высокого напряжения
- •§ 15.2. Пожарная опасность и профилактика процессов сушки
- •Глава 16. Пожарная профилактика процессов, протекающих в химических реакторах
- •§ 16.1. Назначение и классификация химических реакторов
- •§ 5. По конструктивному оформлению теплообменных устройств
- •§ 16.2. Пожарная опасность и противопожарная защита химических реакторов
- •Глава 17. Пожарная профилактика экзотермических и эндотермических химических процессов
- •§ 17.1. Пожарная профилактика экзотермических процессов
- •Процессы полимеризации и поликонденсации
- •§ 17.2. Пожарная профилактика эндотермических процессов
- •Дегидрирование
- •Пиролиз углеводородов
- •Глава 18. Изучение технологических процессов
- •§18.1. Информация о технологии производств, необходимая работнику пожарной охраны
- •§ 18.2. Источники информации о технологических процессах производств
- •§ 18.3. Методы изучения технологии производств
- •Глава 19. Исследование и оценка пожаровзрывоопасности технологических процессов производств
- •§ 19.1. Категории пожаровзрывоопасности производств согласно требованиям сНиПов
- •§ 19.2. Соответствие технологии производств системе стандартов безопасности труда
- •§ 19.3. Разработка пожарно-технической карты
- •Глава 20. Пожарно-техническая экспертиза технологических процессов на стадии проектирования производств
- •§ 20.1. Особенности пожарного надзора на стадии проектирования технологических процессов производств
- •§ 20.2. Использование норм проектирования по обеспечению пожарной безопасности технологических процессов производств
- •§ 20.3. Задачи и методика пожарно-технической экспертизы проектных материалов
- •§ 20.4. Основные решения пожарной безопасности, разрабатываемые на стадии проектирования производств
- •Глава 21. Пожарно-техническое обследование технологических процессов действующих производств
- •§ 21.1. Задачи и организация пожарно-технического обследования
- •§ 21.2. Бригадный метод пожарно-технического обследования
- •§ 21.3. Комплексное пожарно-техническое обследование предприятий отрасли
- •§21.4. Нормативно-технические документы пожарно-технического обследования
- •§ 21.5. Пожарно-техническая анкета как методический документ обследования
- •§ 21.6. Взаимодействие госпожнадзора с другими надзорными органами
- •Глава 22. Обучение рабочих и инженерно-технических работников основам пожарной безопасности технологических процессов производств
- •§ 22.1. Организация и формы обучения
- •§ 22.2. Учебные программы
- •§ 22.3. Методика и технические средства обучения
- •§ 22.4. Программированное обучение
- •Литература
- •Оглавление
Глава 17. Пожарная профилактика экзотермических и эндотермических химических процессов
Экзотермическая реакция — химическая реакция, протекающая с выделением теплоты (например горение, нейтрализация). Эндотермическая реакция — химическая реакция, протекающая с поглощением теплоты из внешней среды (например процессы восстановления металлов из руд).
§ 17.1. Пожарная профилактика экзотермических процессов
Примерами наиболее широко распространенных в промышленности экзотермических процессов являются окисление, хлорирование, гидрохлорирование, гидрирование, полимеризация, поликонденсация.
Процессы хлорирования и гидрохлорирования Реакции хлорирования и гидрохлорирования проводятся с целью введения атома хлора в органическое соединение. Они могут протекать как в жидкой, так и в паровой среде. Так, хлорированием этилена получают дихлорэтан:
CH2 = CH2 + Cl2->C1CH2—CH2C1 + Q, (17.1)
а гидрохлорированием ацетилена получают хлористый винил:
CH = CH + HC1→CH2 = CHC1 + Q. (17.2)
Условия осуществления процессов хлорирования и гидрохлорирования в промышленности весьма разнообразны. Они проводятся при обычных и повышенных температуре и давлении, без катализаторов и с применением их (либо инициаторов), в жидкой или парогазовой фазе.
В качестве исходных продуктов в промышленных процессах хлорирования и гидрохлорирования используют горючие углеводородные газы (метан, этан, этилен, пропилен, ацетилен и др.), легковоспламеняющиеся и горючие жидкости (бензол, толуол, фенол и др.). Конечные и промежуточные продукты в большинстве случаев являются также ЛВЖ и ГЖ (дихлорэтан, хлорбензол, дихлорэтилен и др.) и сжиженными газами (хлористый винил, хлористый метил и др.). Хлор, применяемый в этих процессах, является сильным окислителем, поддерживает горение многих органических веществ, образует взрывчатые смеси с органическими веществами, обладает токсичностью. Хлористый водород и хлор вызывают коррозию оборудования, особенно в присутствии влаги. В качестве хладагентов помимо воды и холодильных рассолов применяются горючие вещества, такие, как аммиак, этилен, водород и другие, что повышает пожарную опасность процессов хлорирования и гидрохлорирования.
Для некоторых газофазных процессов хлорирования (гидрохлорирования) необходим первоначальный подогрев реагентов до 200... 500° С. Используют для этого высокотемпературные теплоносители, в том числе органические, водяной пар, топочные газы, получаемые сжиганием жидкого или газообразного топлива, что обусловливает наличие открытых источников огня.
Газофазные процессы хлорирования (гидрохлорирования) проводят в реакторах вытеснения непрерывного действия трубчатого или камерного типа с изотермическим или адиабатическим режимом. На рис. 17.1 показана схема реактора вытеснения трубчатого
типа.
Пары органических веществ и углеводородные газы образуют с хлором взрывоопасные смеси, а скорость реакции хлорирования в значительной степени зависит от состава смеси. В определенном интервале состава хлоруглеводородной смеси скорость реакции резко возрастает и реакция становится неуправляемой, носит взрывной характер. Поэтому предусматривается надежная автоматическая система регулирования безопасного соотношения подачи хлора и углеводородов.

Рис. 17.1. Схема реактора вытеснения трубчатого типа: 1 — корпус; 2 — катализатор; 3 — теплоноситель (хладагент); 4 — исходные продукты; 5 — продукты реакции
Повышение температуры в реакционном объеме приводит к повышению скорости реакции, делает реакцию неуправляемой. Оно может произойти вследствие нарушения теплообмена (из-за прекращения или уменьшения подачи хладагента), загрязнения теплообменной поверхности, подачи хладагента с завышенной начальной температурой. Для поддержания заданной температуры в реакционном объеме предусматривается автоматическое регулирование подачи хладагента в систему охлаждения реактора.
При проведении процесса газофазного хлорирования могут иметь место реакции разложения продуктов хлорирования. Например,
С2Н5С1=С2Н4+НС1. (17.3)
При этом образуются газообразные продукты и пары, что может быть причиной повышения давления в реакторе.
В газофазных процессах может быть термическое разложение углеводородов с образованием сажи и смолистых продуктов, которые загрязняют поверхности твердого катализатора и увеличивают гидравлическое сопротивление системы. Сажу и смолистые вещества периодически выжигают.
В жидкофазных процессах легче поддерживать постоянство температуры, а также регулировать ее на заданном уровне, так как наличие в реакторах жидкостей создает благоприятные условия для теплоотвода. Поэтому хлорирование и гидрохлорирование органических веществ, неустойчивых при изменении температуры, осуществляют жидкофазным способом (например, это относится к винилацетилену).
Процессы гидрирования (гидрогенизации)
Гидрирование — это процесс непосредственного присоединения водорода к углеродсодержащим веществам. Например, гидрогенизацией окиси углерода получают метанол:
CO + 2H2=CH3OH + Q; (17.4)
гидрогенизацией бензола получают циклогенсан:
C6H6+3H2=C6H12+Q. (17.5)
Процессы гидрирования широко используются в промышленности при получении растворителей, синтетических смол, поверхностно-активных веществ, моторных топлив, технических смазок и т. д. В качестве исходного сырья применяют ароматические углеводороды, альдегиды и кетоны, нитросоединения, синтетические жирные кислоты и др.
Процессы гидрирования экзотермичны. Они проводятся при повышенных температурах (повышается активность катализаторов), при повышенных давлениях, а также при значительном избытке водорода, что позволяет увеличить выход продуктов реакции и поддерживать оптимальный температурный режим. Для каждого процесса гидрирования существует оптимальное время контакта реагирующих веществ с катализатором (от долей минуты до нескольких часов).
Процессы гидрирования происходят как в жидкой, так и в парогазовой фазах. Гидрирование высококипящих веществ производится жидкофазным способом, низкокипящих веществ — парофазным. В промышленных процессах гидрирования обращается большое количество ЛВЖ и ГЖ, которые используются в качестве сырья и получаются в итоге проведения процесса. Горючие жидкости нагреты выше температуры вспышки, а часто — выше температуры самовоспламенения и находятся под повышенным давлением. Для подогрева исходного сырья используются горючие высокотемпературные органические теплоносители. Технологическое оборудование, нагретое выше 200° С и находящееся под давлением газообразного водорода, подвергается активной водородной коррозии.
Для проведения процессов гидрирования применяются реакторы трубчатого или колонного типа с неподвижным слоем катализатора (рис. 17.2). Катализатор размещается в специальной катализаторной коробке. Холодный водород (или реакционная смесь) подается в кольцевое пространство между корпусом и катализаторной коробкой для снятия тепла. Кроме того, по высоте коробки в нескольких местах тоже вводится холодный водород.
Реактор гидрирования заполнен смесью паров ЛВЖ с водородом под давлением. Поскольку при нормальной работе в смеси нет окислителя, взрывоопасные концентрации внутри реактора не образуются.
Пожарная опасность реакторов гидрирования связана с возможностью появления неплотностей, повреждений и с выходом наружу водорода и паров ЛВЖ, с самовоспламенением их при контакте с воздухом. Повышенные давления в реакторах гидрирования могут возникать из-за:
нарушения температурного режима (перегревов исходного сырья, ухудшения теплоотвода из реакционной зоны). В реакторах газофазного гидрирования давление увеличивается пропорционально повышению температуры;
спекания и измельчения катализатора, что ведет к повышению гидравлического сопротивления слоя;
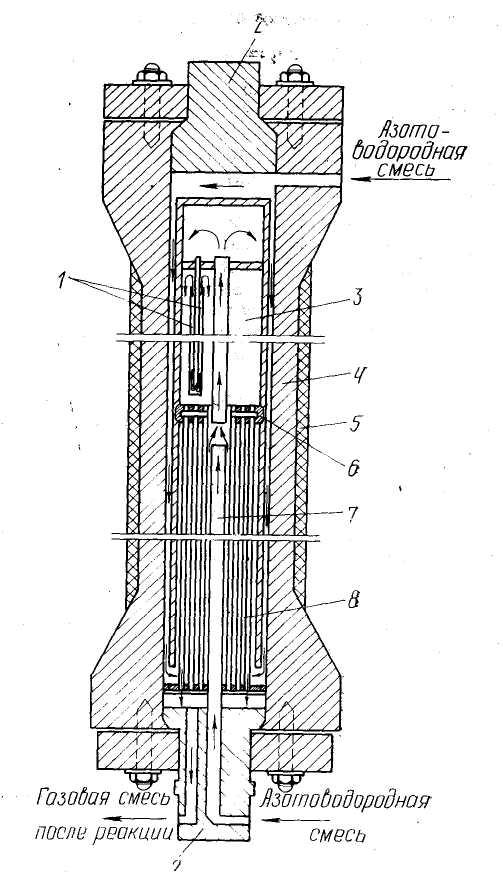
Рис. 17.2. Колонна для синтеза аммиака под средним давлением: / — теплообменник; 2 —крышки; 3 —катализаторная коробка; 4 — корпус колонны; 5 — изоляция; б— колосниковая решетка; 7 — центральная труба; 8 — теплообменные трубы
прогара труб, ведущего к аварии и пожару; попадания в реактор жидкого продукта и его вскипания. В парогазовых реакторах колонного типа с неподвижным катализатором теплоотвод осуществить труднее, чем в жидкофазных .реакторах, из-за низких коэффициентов теплоотдачи от газа к поверхности теплообмена. Для проведения реакций с большим тепло-дым эффектом применяются реакторы с промежуточным теплообменом: реактор делится на секции с промежуточным охлаждением (рис.. 17.3). При такой схеме слои катализатора чередуются с зонами теплообмена (теплообменниками). В реакционной зоне процесс идет адиабатически (без отвода тепла) и реакционные газы нагреваются. Затем в теплообменнике они охлаждаются и температура снова приближается к оптимальной и т. д. Чем больше ступеней контактирования и промежуточного охлаждения, тем ближе режим к оптимальному, тем безопаснее работа реактора.
Температурный режим в реакторе поддерживается за счет автоматического регулирования состава парогазовой смеси и подачи холодного газа (в зависимости от температуры в реакторе). Предусматривается также очистка свежего и циркуляционного водорода от механических примесей (во избежание загрязнения теплообменников), улавливание неиспарившейся перед реактором жидкости (с помощью сепараторов) и устройство компенсаторов температурных напряжений. Для предотвращения водородной и сероводородной коррозии реакторы изготовляются из специальных сталей или защищаются коррозионностойкими материалами. К специфическим источникам зажигания, которые могут возникнуть при проведении процессов гидрирования, относятся теплота химической реакции, вещества, нагретые до температуры, их самовоспламенения, статическое превышающей температуру электричество и самовозгорание сульфидов железа.

Рис. 17.3. Схема реактора с промежуточным теплообменом: 1...4—секции реактора с катализатором;
а...Ь — теплообменники
