
- •Що таке еквівалентна електрична провідність?
- •Охарактеризуйте особливості коагуляції золів сумішами електролітів.
- •Що таке діаграма плавкості?
- •Що таке кінетична стійкість дисперсної системи?
- •Які властивості розчинів називають колігативними?
- •Що таке активні молекули?
- •Як можна виміряти електродний потенціал?
- •В чому полягає сутність методів хроматографічного аналізу?
- •Що таке буферна система?
- •Що таке гальванічний елемент?
- •Як орієнтуються молекули поверхнево-активної речовини в адсорбційному шарі?
- •В чому полягає суть методу потенціометричного титрування?
- •Сформулюйте закон Кольрауша, наведіть математичний вираз закону.
- •В чому полягає спільність та відмінність у властивостях розчинів високомолекулярних сполук та істинних розчинів; розчинів вмс та колоїдних розчинів?
- •Дайте визначення понять: фаза, компонент, ступінь свободи системи.
- •В чому полягає сутність методу кондуктометричного титрування?
-
Що таке діаграма плавкості?
Виражають залежність температур кристалізації (плавлення) бінарних систем від їх складу.
В чому полягає принцип її побудови?
Для побудови діаграм плавкості використовують два основні способи реєстрації температурних змін, які відповідають фазовим переходам: 1) за кривими охолодження (або нагрівання), які виражають залежність температури суміші від часу охолодження (або нагрівання). При будь-якому фазовому перетворенні на цих кривих відзначаються зупинки або злами, температури яких наносять на діаграму для відповідних складів системи; 2) візуальний метод, в якому вимірюють температуру появи (або зникнення) кристалів у прозорому розчині.
Що таке крива охолодження?
Виражають залежність температури суміші від часу охолодження (або нагрівання).
Який вигляд матиме діаграма плавкості двокомпонентної системи з простою евтектикою?
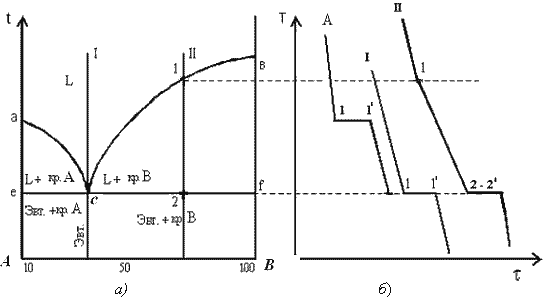
Застосуйте правило фаз Гіббса для аналізу системи.
З'ясуємо за допомогою правила фаз Гіббса максимально можливе число фаз та ступенів свободи в рівноважній однокомпонентній системі
(К = 1). Якщо число ступенів свободи С = 0, то Фмах = 3. Таким чином, індивідуальна речовина не може утворювати рівноважну систему, яка б складалася більше, ніж із трьох фаз. При наявності однієї фази така система має два ступеня свободи С=1-1+2=2, тобто система біваріантна.
Що таке "фізична несумісність " інгредієнтів лікарських препаратів?
Фізичні несумісності — це несумісності, за яких відбуваються зміни фізичного стану лікарських речовин у препараті. Розрізняють такі причини їх виникнення: нерозчинність або погіршення умов розчинності лікарської речовини; незмішуваність інгредієнтів; відволожування й розплавлення (евтектика) суміші твердих речовин; коагуляція колоїдних систем і розчинів ВМС; розшарування емульсій; адсорбція діючих речовин. На виникнення несумісностей впливають й інші чинники, напр. світло, температура, леткість інгредієнтів. Відволожування порошків залежить від вологості лікарських речовин і відносної вологості приміщення, температури повітря, характеру і тривалості перемішування, ступеня дисперсності, типу пакування.
Яку роль вона відіграє в фармацевтичній практиці?
Велику, так як не можливо приготувати ті чи інші ЛП
Як її можна передбачити, виходячи з діаграми?
Це непередбачувані хімічні реакції
-
Що таке кінетична стійкість дисперсної системи?
Кінетична (седиментаційна) стійкість – здатність дисперсних частинок перебувати у завислому стані і не седиментуватися, тобто не осідати.
Агрегативна стійкість?
Агрегатна стійкість – здатність часточок дисперсної фази зберігати ступінь дисперсності незмінним. В агрегатно стійких системах часточки дисперсної фази при зіткненні не злипаються і не утворюють агрегатів.
Що таке коагуляція?
злипання частинок колоїдів при їхньому зіткненні в процесі теплового (броунівського) руху, перемішування або напрямленого переміщення в зовнішньому силовому полі. У агрегатах (флокулах) первинні частинки пов'язані молекулярними силами безпосередньо або через прошарок навколишнього (дисперсійного) середовища.
Які фактори викликають коагуляцію золів?
введення електролітів, неелектролітів, заморожування, кип’ятіння, перемішування, дії сонячного світла
В чому полягає механізм впливу електролітів?
У процесі електролітної коагуляції часто спостерігається іонообмінна адсорбція: іони коагулянта з більшою валентністю або більшим адсорбційним потенціалом витісняють протиіони спочатку дифузного шару, а потім і адсорбційного шару. Обмін проходить в еквівалентній кількості, але заміна протиіонів приводить до того, що при достатній концентрації електролітів у дисперсному середовищі часточки гублять стійкість і при зіткненні злипаються.
Що таке поріг коагуляції?
Поріг коагуляції – це мінімальна концентрація електроліту при перевищенні якої спостерігається коагуляція.
Коагулююча здатність?
це об’єм золю, скоагульованого 1 моль електроліту.
Як впливає здатність іону до гідратації на його коагулюючу дію?
Це пояснюється тим, що ступінь гідратації іонів зменшується, наприклад, від L+1 до Cs+, а це полегшує його впровадження у подвійний іонний шар.
Що таке ліотропний ряд?
ряд іонiв, що розташованi в порядку пiдсилення чи послаблення їхнього впливу на властивостi розчинника (в'язкість, поверхневий натяг, розчинність i т. п.), а також на швидкiсть реакцiй у даному розчинниковi та iншi фiзико-хімiчнi процеси. Синонім — ряд Гофмейстера.
Як впливає заряд коагулюючого іону?
Коагулюючу дію має лише той іон електроліту, заряд якого протилежний заряду колоїдної частинки. Коагулююча здатність іона залежить від його заряду.
Сформулюйте правило Шульце - Гарді.
критична концентрація коагуляції для типових ліофільних золів дуже чутлива до валентності протийонів (йони з більшою валентністю знижують критичну концентрацію коагуляції). Коагуляцiйна здатнiсть електроліту є тим вищою, чим бiльший заряд йонiв з протилежним до заряду колоїдних частинок знаком.
Білет 3
