
- •ГЛАВА 5. АРИТМИИИ БЛОКАДЫ СЕРДЦА........................................…………...
- •ГЛАВА 6. МИОКАРДИТЫ. МИОКАРДИОПАТИИ……………………...………..
- •ГЛАВА 7.ПЕРИКАРДИТЫ. ………………….………………………..…................
- •ГЛАВА 3. АПЛАСТИЧЕСКАЯ АНЕМИЯ..................................................................
- •ГЛАВА 4. ОСТРЫЕ ЛЕЙКОЗЫ………………………………………………………
- •ГЛАВА 5.ХРОНИЧЕСКИЕ МИЕЛО- И ЛИМФОЛЕЙКОЗЫ……………………..
- •Патогенетические механизмы.
- •Классификация гипертонических кризов.
- •Неосложнённый гипертонический криз, несмотря на выраженную клиническую симптоматику, не сопровождается острым клинически значимым нарушением функции органов-мишеней.
- •Примечание.ВNP или NT – pro ВNP -N-концевой предсердный натрийуретический пептид и его предшественник (Национальные клинические рекомендации ВНОК, 2008).
- •Цели лечения острой сердечной недостаточности.
- •Цель неотложного лечения – быстрая стабилизация гемодинамики и уменьшение симптомов (одышки и/или слабости).
- •Диета. Необходимо поддерживать оптимальный баланс калорий и аминокислот, калия и магния в сыворотке крови.
- •Показания к ИВЛ с интубацией трахеи:
- •Медикаментозное лечение.
- •Морфин – показан при раннем лечении тяжелой ОСН, особенно при наличии боли, возбуждении и выраженной одышки. Вводят в/в болюсом 3 мг сразу после катетеризации вены, при необходимости повторно.
- •Примечание.Национальные клинические рекомендации ВНОК, 2008.
- •Ингибиторы ангиотензинпревращающего фермента(ИАПФ)– на начальных этапах лечения ОСН препараты этой группы недостаточно изучены.
- •Для борьбы с устойчивостью к диуретикам:
- •β-адреноблокаторы (БАБ) – лечениеβ-блокаторамипосле ликвидации симптомов ОСН (дозы титруют постепенно) вызывает улучшение клинической картины и прогноза у больных ИМ и ХСН. Дозы титруют постепенно.
- •Показания: сохраняющаяся АГ, ишемия микарда, тахикардия у больных без артериальной гипотонии и признаков периферической гипоперфузии и стандартных противопоказаний (метопролол, эсмолол, бисопролол, карведилол).
- •ГЛАВА 5. АРИТМИИИ БЛОКАДЫ СЕРДЦА.
- •Электрокардиостимуляция.
- •Кардиомиопатии.
- •ГЛАВА 7. ПЕРИКАРДИТЫ.
- •ГЛАВА 8. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА У ВЗРОСЛЫХ (ВПС).
- •ГЛАВА 3. АПЛАСТИЧЕСКАЯ АНЕМИЯ.
- •ГЛАВА 4. ОСТРЫЕ ЛЕЙКОЗЫ.
- •ГЛАВА 5. ХРОНИЧЕСКИЕ МИЕЛО - И ЛИМФОЛЕЙКОЗЫ.
- •Возможные этиологические факторы:
- •1. Малые дозы радиации.
- •2. Слабые электромагнитные излучения.
- •3. Гербициды, инсектициды и т.д.
- •4. Химические агенты – бензол.
- •Патогенетические аспекты ХМЛ.
- •Биологический эффект химерного генаBCR-ABL в гемопоэтических предшественниках:
- •Таблица 7-1
- •Стадии ММ
- •Клиническая картина.
- •Дифференциальный диагноз.
- •Лечение осложнений ММ.
- •Лечение и профилактика осложнений.
- •Лечение ХГН.
- •Терминальная почечная недостаточность.
- •Основные причины ТПН:
- •Лечение.
- •Таблица 4-1
- •Классификация амилоидоза
- •Клиническая картина и диагностика.
- •Лабораторные исследования.
- •Инструментальные исследования.
- •Таким образом, в основе развития ХЛС лежит постепенное формирование легочной артериальной гипертензии, которая обусловлена несколькими патогенетическими механизмами.
- •Клиника и диагностика ХЛС.
- •2) дыхательной недостаточности:
- •Плевральная пункция и исследование плевральной жидкости при диагностике плевритов и плевральных выпотов.
Князева Л. И., Князева Л. А., Горяйнов И. И.
Внутренние болезни
Учебник
Князева Л. И., Князева Л. А., Горяйнов И. И.
Внутренние болезни
Учебник для студентов медицинских вузов
Курск – 2013
2
УДК: 616.1/4 (075.8) ББК: 54.1я73
К54
УМО-754 25.08.08
«Рекомендуется Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебника для студентов медицинских вузов»
Князева Л. И., Князева Л. А., Горяйнов И. И. Внутренние болезни. Учебник для студентов медицинских вузов. Издание четвертое, дополненное и переработанное. - Курск, 2013.- с.
Рецензенты:
д.м.н., профессор кафедры факультетской терапии ГБОУ ВПО «Первый Московский государственный медицинский университет им. И.М.Сеченова» Минздрава России Т.В. Королева
д.м.н., профессор, зав. каф. пропедевтики внутренних болезней ГБОУ ВПО «Воронежская государственная медицинская академия им. Н.Н. Бурденко» Минздрава России А.В. Никитин
В данном учебнике представлены современные аспекты этиологии, патогенеза, клинических проявлений и диагностики заболеваний внутренних органов. Важным разделом четвертого издания учебника являются современные протоколы лечения внутренней патологии, основанные на принципах доказательной медицины, с учетом изменений
2012 г.
Несомненным достоинством данного учебника является анализ и систематизация новых методов диагностики и лечения основных заболеваний внутренних органов, представленных в виде алгоритмов, схем и таблиц.
Учебник будет полезен для студентов старших курсов медицинских вузов, поскольку содержит ответы на многие сложные вопросы, порождаемые клинической практикой.
ISBN 978-5-7487-1472-3 ББК: 54.1я73
Князева Л.И., Князева Л.А., Горяйнов И.И., КГМУ, 2013 ГБОУ ВПО КГМУ Минздрава России, 2013
3
СОДЕРЖАНИЕ РАЗДЕЛ I. РЕВМАТОЛОГИЯ
ГЛАВА 1.РЕВМАТОИДНЫЙ АРТРИТ………………………. ……………………
ГЛАВА 2. ОСТЕОАРТРОЗ……………………………………………………………
ГЛАВА 3. ПОДАГРА…………………………….……………………………………
ГЛАВА 4. СИСТЕМНАЯ КРАСНАЯ ВОЛЧАНКА.......................................………
ГЛАВА 5. СИСТЕМНАЯ СКЛЕРОДЕРМИЯ……………………….. ……………..
ГЛАВА 6. СЕРОНЕГАТИВНЫЕ СПОНДИЛОАРТРОПАТИИ……………………
ГЛАВА 7.ОСТРАЯ РЕВМАТИЧЕСКАЯ ЛИХОРАДКА. ХРОНИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА …………………………………………………………………...
ГЛАВА 8.РЕВМАТИЧЕСКИЕ ПОРОКИ СЕРДЦА………………………………...
ГЛАВА 9. СИСТЕМНЫЕ ВАСКУЛИТЫ....................................................................
ГЛАВА10.ИДИОПАТИЧЕСКИЕ ВОСПАЛИТЕЛЬНЫЕ МИОПАТИИ…….........
РАЗДЕЛ II. КАРДИОЛОГИЯ.
ГЛАВА 1. ИБС: СТАБИЛЬНАЯ СТЕНОКАРДИЯ………………………………….
ГЛАВА 2. ИБС: ОСТРЫЙ ИНФАРКТ МИОКАРДА…………………………….…
ГЛАВА 3. АРТЕРИАЛЬНЫЕ ГИПЕРТЕНЗИИ………………………….………….
ГЛАВА 4.ОСТРАЯ И ХРОНИЧЕСКАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ…………………………………………………………...……
ГЛАВА 5. АРИТМИИИ БЛОКАДЫ СЕРДЦА........................................…………...
ГЛАВА 6. МИОКАРДИТЫ. МИОКАРДИОПАТИИ……………………...………..
ГЛАВА 7.ПЕРИКАРДИТЫ. ………………….………………………..…................
ГЛАВА 8. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА У ВЗРОСЛЫХ…………………..
РАЗДЕЛ III. ГЕМАТОЛОГИЯ
ГЛАВА 1.ЖЕЛЕЗОДЕФИЦИТНЫЕ АНЕМИИ.........................................................
ГЛАВА 2. МЕГАЛОБЛАСТНЫЕ АНЕМИИ………………………………………...
ГЛАВА 3. АПЛАСТИЧЕСКАЯ АНЕМИЯ..................................................................
ГЛАВА 4. ОСТРЫЕ ЛЕЙКОЗЫ………………………………………………………
ГЛАВА 5.ХРОНИЧЕСКИЕ МИЕЛО- И ЛИМФОЛЕЙКОЗЫ……………………..
ГЛАВА 6. ИСТИННАЯ ПОЛИЦИТЕМИЯ…………………………………………..
ГЛАВА 7. МНОЖЕСТВЕННАЯ МИЕЛОМА……………………………………….
ГЛАВА 8. ГЕМОРРАГИЧЕСКИЕ ДИАТЕЗЫ……………………………………….
РАЗДЕЛ IV. НЕФРОЛОГИЯ
ГЛАВА 1.ОСТРЫЙ И ХРОНИЧЕСКИЙ ГЛОМЕРУЛОНЕФРИТЫ……………..
ГЛАВА 2. ХРОНИЧЕСКИЙ ТУБУЛОИНТЕРСТИЦИАЛЬНЫЙ НЕФРИТ………
ГЛАВА 3. ХРОНИЧЕСКАЯ БОЛЕЗНЬ ПОЧЕК.ТЕРМИНАЛЬНАЯ ПОЧЕЧНАЯ НЕДОСТАТОЧНОСТЬ............................................................................
ГЛАВА 4. АМИЛОИДОЗ. НЕФРОТИЧЕСКИЙ СИНДРОМ……………………….
РАЗДЕЛ V. ГАСТРОЭНТЕРОЛОГИЯ ГЛАВА 1.ЯЗВЕННАЯ БОЛЕЗНЬ ЖЕЛУДКА
И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ………………………………………..
ГЛАВА 2. ХРОНИЧЕСКИЙ ПАНКРЕАТИТ…………………………………...
ГЛАВА 3. СИНДРОМ РАЗДРАЖЁННОЙ КИШКИ……………………………..
4
ГЛАВА 4. ЯЗВЕННЫЙ КОЛИТ............................................................................
ГЛАВА 5. ГЕПАТИТЫ И ЦИРРОЗЫ ПЕЧЕНИ……………………………….
РАЗДЕЛ VI. ПУЛЬМОНОЛОГИЯ
ГЛАВА 1. ПНЕВМОНИИ…………………………………………………………..
ГЛАВА 2. ХРОНИЧЕСКАЯ ОБСТРУКТИВНАЯ БОЛЕЗНЬ ЛЕГКИХ…………
ГЛАВА 3. БРОНХИАЛЬНАЯ АСТМА.....................................................................
ГЛАВА 4. ХРОНИЧЕСКОЕ ЛЕГОЧНОЕ СЕРДЦЕ……………………………….
ГЛАВА 5. ПЛЕВРИТЫ…………………….………………………………………...
ГЛАВА 6. ИДИОПАТИЧЕСКИЕ ИНТЕРСТИЦИАЛЬНЫЕ ПНЕВМОНИИ……
ЛИТЕРАТУРА. …………………………..…………………………………
5
РАЗДЕЛ I. РЕВМАТОЛОГИЯ.
ГЛАВА 1. РЕВМАТОИДНЫЙ АРТРИТ.
Ревматоидный артрит (РА) – хроническое системное заболевание соединительной ткани с прогрессирующим поражением преимущественно периферических (синовиальных) суставов по типу эрозивнодеструктивного полиартрита, возможным развитием полиорганного поражения и тяжелых осложнений, таких как вторичный амилоидоз.
РА представляет собой наиболее распространенное аутоиммунное заболевание человека, которое регистрируют во всех климатогеографических зонах, во всех возратсных , расовых и этнических группах, поражая 0,5-2% взрослого населения Земли в наиболее работоспособном возрасте (35-55 лет). РА имеет общемедицинское и социальное значение, приводя к колоссальным экономическим потерям.
Факторы риска возникновения РА: женский пол, возраст 45 лет и старше, наследственная предрасположенность, наличие антигенов
HLADR4, DR1
Этиология РА неизвестна.
Существуют 2 теории возникновения и развития РА.
Вирусная теория: инфекционные агенты – вирус Эпштейна-Барра,
парвовирус В19, ретровирусы. |
предрасположенность – |
Генетическая теория. Генетическая |
|
носительство HLA-DR4, HLA-DR1 генов. |
|
Патогенез РА складывается из нескольких взаимодополняющих компонентов:
-участие Т-лимфоцитов;Bлимфоцитов.
-участие моноцитомакрофагальных клеток, которые продуцируют провоспалительные цитокины: (интерлейкин (ИЛ)-1, ИЛ-6, фактор некроза опухоли α)
-участие автономных неиммунных механизмов, определяющих опухолеподобный рост синовиальной ткани, приводящий к деструкции суставного хряща.
На ранней стадии РА:доминируют неспецифическое воспаление и синтез органоспецифичных аутоантител (ревматоидный фактор (РФ) и антитела к циклическому цитруллинированному пептиду (анти-ЦЦП)).
Развернутая стадия сопровождается нарушением ангиогенеза, активацией эндотелия, активной миграцией клеток в зону воспаления, активацией СД 4+ Т-клеток, гиперпродукцией провоспалительных
цитокинов, простагландинов, коллагеназ, металлопротеаз. |
|
|||
Поздняя |
стадия |
сопровождается |
нарушением |
апоптоза |
синовиальных клеток и прогрессирующей деструкцией суставов.
Главные патогенетические процессы, ведущие к деструкции сустава: деградация хряща, персистирующее аутоиммунное воспаление в полости сустава, пролиферация синовиальной ткани с разрастанием паннуса, и прогрессирующим развитием остеопороза.
6

Патоморфология.
Преобладают экссудативные и альтеративные процессы в синовиальной мембране, а именно отек, полнокровие и очаги фибриноидных изменений (рис. 1-1).
Рис. 1-1. Патоморфология ревматоидного артрита (по Насоновой В.А.,1997)
Рабочая классификация РА (принята на заседании пленума
Ассоциации ревматологов России 30.09.2007). |
|
||||
1. |
Основной диагноз: |
|
|
|
|
Ревматоидный |
артрит |
серопозитивный |
(положительный |
||
ревматоидный фактор в сыворотке крови). |
|
||||
Ревматоидный |
артрит |
серонегативный |
(отрицательный |
||
ревматоидный фактор в сыворотке крови. |
|
||||
Особые клинические |
формы |
ревматоидного артрита: |
|||
Синдром Фелти. |
|
|
|
|
|
Болезнь Стилла, развившаяся у взрослых. |
|
||||
Ревматоидный |
артрит |
вероятный. |
|
||
2. |
Клиническая стадия. |
|
|
||
1. |
Очень ранняя стадия: длительность болезни < 6 месяцев. |
||||
2.Ранняя стадия: длительность болезни 6 мес. - 1 год.
3.Развернутая стадия: длительность болезни > 1 года при наличии типичной симптоматики РА.
4.Поздняя стадия: длительность болезни 2 года и более + выраженная деструкция мелких (III-IV рентгенологическая стадия) и крупных суставов, наличие осложнений.
3.Активность болезни:
0= ремиссия (DAS 28 < 2,6).
1= низкая (DAS 28 = 2,6 - 3,2).
2= средняя (DAS 28 3,3 - 5,1).
7
3 = высокая (DAS 28 > 5,1).
4. Внесуставные (системные) проявления:
1. Ревматоидные узелки.
2. Кожный васкулит (язвенно-некротический васкулит, инфаркты ногтевого ложа, дигитальный артериит, ливедо-ангиит).
3.Васкулит других органов.
4.Нейропатия (мононеврит, полинейропатия).
5.Плеврит (сухой, выпотной), перикардит (сухой, выпотной).
6.Синдром Шегрена.
7.Поражение глаз (склерит, эписклерит, васкулит сетчатки).
5.Инструментальная характеристика.
Наличие или отсутствие эрозий (с использованием рентгенографии, возможно МРТ, УЗИ):
-неэрозивный; -эрозивный.
Рентгенологическая стадия (по Штейнброккеру, модификация): I- околосуставной остеопороз;
II-остеопороз + сужение суставной щели, могут быть единичные эрозии;
IIIпризнаки предыдущей стадии + множественные эрозии + подвывихи в суставах;
IV — признаки предыдущей стадии + костный анкилоз.
6.Дополнительная иммунологическая характеристикаантитела
кциклическому цитрулинированному пептиду (АЦЦП)
АЦЦП — присутствуют (+); АЦЦП — отсутствуют (-).
Функциональный класс (ФК):
I— полностью сохранены самообслуживание, непрофессиональная
ипрофессиональная деятельность;
II— сохранены: самообслуживание, профессиональная деятельность, ограничена непрофессиональная деятельность;
III — сохранено самообслуживание, ограничены непрофессиональная и профессиональная деятельность;
IV — ограничены самообслуживание, непрофессиональная и профессиональная деятельность;
8. Осложнения:
-вторичный системный амилоидоз;
-вторичный остеоартроз;
-остеопороз (системный);
-остеонекроз;
-туннельные синдромы (синдром карпального канала, синдромы сдавления локтевого, большеберцового нервов);
-подвывих в атланто-аксиальном суставе, в том числе с миелопатией, нестабильность шейного отдела позвоночника;
-атеросклеротическое поражение сосудов.
8
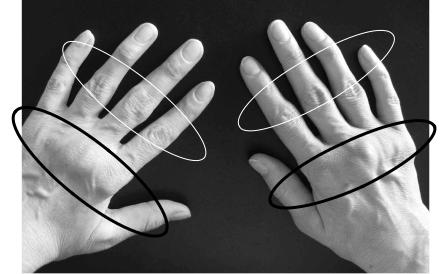
Ранний ревматоидный артрит.
Ранняя фаза ревматоидного артрита характеризуется появлением утренней скованности (всегда! свыше 30 мин.) в мелких суставах кистей (проксимальных межфаланговых и пястно-фаланговых) и стоп (проксимальных межфаланговых и плюснефаланговых) с развитием воспалительного отека периартикулярных тканей, возникновение болезненности вышеуказанных суставов при пальпации (положительный симптом поперечного сжатия кисти).
Процесс обычно симметричен и охватывает суставы обеих кистей (рис.1-2) и обеих стоп практически одновременно.
Рис.1-2. Ранний РА. Обращает на себя внимание симметричные артриты проксимальных межфаланговых (палец формы «веретена») и пястно-фаланговых суставов.
Если длительность подобной клинической симптоматики составляет не более 1 года, то речь идет о потенциально обратимой, клиникопатогенетической стадии болезни – раннем РА (РРА).
Признаки, позволяющие заподозрить РРА (по Р. Еmеry):
-> 3 припухших суставов;
-симметричное поражение пястно-фаланговых и плюснефаланговых суставов;
-положительный «тест поперечного сжатия» пястно-фаланговых
иплюсне-фаланговых суставов;
-утренняя скованность > 30 мин;
-СОЭ > 25 мм/час.
РРА сопровождается, чаще всего, такими системными проявлениями, как лихорадка, потеря массы тела, появлением ревматоидных узелков.
Уже на ранней стадии ревматоидного артрита будут характерны следующие изменения лабораторно-инструментальных показателей:
-СОЭ более 25 мм/ч;
-СРБ более 6 мг/мл;
9

-фибриноген более 5 г/л;
-наличие ревматоидного фактора, антител к циклическому цитруллиновому пептиду (АЦЦП), антител к виментину в сыворотке крови.
Примечание: при наличии таких признаков пациент должен быть
направлен на консультацию к ревматологу
Клиническая картина РА.
Поражение суставов.
Утренняя скованность — один из основных симптомов РА ее развитие связано с гиперпродукцией синовиальной жидкости содержащей высокие концентрации провоспалительных цитокинов (ИЛ-1, ИЛ-6, ФНО- α), способствующих поддержанию воспалительного процесса в суставах и дальнейшей деструкции хряща и кости. Утренняя скованность является диагностически значимой, если ее продолжительность составляет более одного часа.
С течением времени у пациентов формируется ревматоидная кисть: ульнарная девиация пястно-фаланговых суставов, обычно развивающаяся через 1—5 лет от начала болезни (рис.1-3); поражение пальцев кистей по типу «бутоньерки» (сгибание в проксимальных межфаланговых суставах) или «шеи лебедя» (переразгибание в проксимальных межфаланговых суставах) (рис.1-4); деформация кисти по типу «пуговичная петля» (рис.1-4, 1-5).
Рис. 1-3. Ульнарная девиация («плавник моржа»)
10

Рис. 1-4. «Шея лебедя».
Рис. 1-5. «Пуговичная петля»
Суставы стоп, как и кистей, вовлекаются в патологический процесс достаточно рано, что проявляется как типичной клинической симптоматикой, так и ранними изменениями на рентгенограммах. Более характерно поражение плюсне-фаланговых суставов II-IV пальцев с последующим развитием дефигурации и деформации стопы за счет множественных подвывихов и анкилозов.
Тазобедренный сустав при РА вовлекается в патологический процесс сравнительно редко. Его поражение проявляется болевым синдромом с иррадиацией в паховую или нижние отделы ягодичной области и ограничением внутренней ротации конечности. Наблюдается тенденция к фиксации бедра в положении полуфлексии. Развивающийся в некоторых случаях асептический некроз головки бедренной кости, с последующей протрузией вертлужной впадины, резко ограничивает движения в тазобедренном суставе. Адекватным лечением в таком случае является эндопротезирование сустава.
11
Воспаление коленных суставов характеризуется их припухлостью из-за развившегося синовита и болезненностью при выполнении активных
ипассивных движений. Развивается дефигурация суставов, при пальпации определяется баллотирование надколенника. За счет высокого внутрисуставного давления нередко образуются выпячивания заднего заворота суставной сумки в подколенную ямку (киста Бейкера). Для облегчения болей пациенты стараются держать нижние конечности в состоянии сгибания, что приводит с течением времени к появлению сгибательной контрактуры, а затем и анкилоза коленных суставов. Нередко формируется вальгусная (варусная) деформация коленных суставов.
Поражение суставов позвоночника, как правило сопровождается их анкилозированием в шейном отделе. Иногда наблюдаются подвывихи атлантоосевого сустава, еще реже — признаки компрессии спинного мозга или позвоночной артерии.
Височно-нижнечелюстные суставы особенно часто поражаются в детском возрасте, но могут вовлекаться в патологический процесс и у взрослых, что приводит к значительным трудностям при открывании рта.
Связочный аппарат и синовиальные сумки:тендосиновит в области лучезапястного сустава и кисти; бурсит, чаще в области локтевого сустава; синовиальная киста на задней стороне коленного сустава (киста Бейкера).
Внесуставные проявления РА.
Конституциональные симптомы.
Уже с первых недель заболевания у больных РА наблюдается снижение массы тела, достигающее 10-20 кг за 4-6 месяцев, иногда вплоть до развития кахексии. Характерно повышение температуры тела, сопровождающееся повышенной утомляемостью, адинамией, общим недомоганием. Лихорадка, появляющаяся уже в начальном периоде заболевания, беспокоит чаще во второй половине дня и вечером. Ее продолжительность колеблется от двух-трех недель до нескольких месяцев. Выраженность температурной реакции вариабельна — от субфебрильных цифр до 39-40°С при особых формах РА. Повышение температуры тела связывают с гиперпродукцией провоспалительных цитокинов (ИЛ-1; ИЛ-3; ИЛ-6; ФНО-α) и простагландинов моноцитамимакрофагами. При повышении температуры тела наблюдается тахикардия
илабильность пульса.
Для РА характерно поражение мышц, проявляющееся в начальной стадии заболевания миалгиями, затем развивается миозит с очагами некроза и генерализованная амиотрофия. Причины развития мышечной атрофии: мобилизация пораженных сегментов конечностей из-за выраженной болезненности, влияние провоспалительных цитокинов, вызывающих миолиз. Доказана прямая корреляционная зависимость между степенью мышечной атрофии, активностью и тяжестью ревматоидного воспаления. Сочетание атрофии межостных мышц, мышц тенара и гипотенара с припухлостью пястно-фаланговых, проксимальных
12

межфаланговых суставов, суставов запястья характеризуется как «ревматоидная кисть».
Поражение кожи при РА.
Поражение кожи при РА развивается на фоне высокой активности ревматоидного процесса и включают в себя капилляриты, геморрагический васкулит, дигитальный артериит, язву голени. Появление кожных изменений при РА связано с прогрессирующим течением ревматоидного васкулита и требует активной подавляющей терапии основного заболевания.
Ревматоидные узелки — безболезненные округлые плотные образования от 2-3 мм до 2-3 см в диаметре, которые выявляются в 2-30% случаев заболевания. Они располагаются преимущественно подкожно на разгибательной стороне суставов пальцев кистей (рис.1-6), локтевых суставов и предплечьях, возможна и другая локализация. Ревматоидные узелки не примыкают к глубинным слоям дермы, они безболезненные, подвижные, иногда спаянные с апоневрозом или костью.
Рис. 1-6. Ревматоидные узелки Их необходимо дифференцировать от подагрических тофусов,
остеофитов при остеоартрозе, ксантоматозных узелков.
Наличие ревматоидных узелков ассоциируется с высокими титрами ревматоидного фактора в сыворотке крови. Их размер со временем меняется, в период ремиссии они могут полностью исчезать. Появление ревматоидных узелков в начальной стадии РА является неблагоприятным прогностическим признаком.
Периферическая лимфоаденопатия диагностируется у 40-60%
больных РА. Наиболее часто поражаются передне- и заднешейные, подчелюстные, под- и надключичные, подмышечные и паховые лимфатические узлы, при этом выраженность лимфоаденопатии зависит от активности иммуновоспалительного процесса. Лимфатические узлы умеренной плотности, безболезненные, не спаянные с кожей, легко смещаемые, их размеры составляют от 1 до 3 см. При изменении характера лимфоаденопатии (увеличение в размерах лимфоузлов, изменение их плотности, генерализация процесса) необходимо проводить дифференциальную диагностику с системными заболеваниями крови, для которых характерно увеличение периферических лимфатических узлов
13
(неходжкинские лимфомы, лимфогранулематоз, хронический лимфолейкоз и др.).
Спленомегалиянаблюдается примерно у 25-30% больных с РА, при этом наиболее объективные данные можно получить при ультразвуковом исследовании селезенки.
Характерны следующие изменения в общем анализе крови: анемия,
тромбоцитоз, нейтропения.
Анемия у больных РА встречается достаточно часто (почти у 50% пациентов), при этом в большинстве случаев речь идет о так называемой «анемии хронического воспаления» (АХВ). Патогенез ее полиэтиологичный. Одной из причин развития АХВ у больных РА является ингибирование функциональной активности клетокпредшественников эритропоэза, в результате чего снижается их пролиферативный потенциал, нарушаются процессы дифференцировки и синтеза гема. Второй важный фактор в развитии анемии — нарушение обмена и утилизации железа. У больных РА выявляется снижение поглощения железа и уменьшение связывания трансферрина эритробластами, а также нарушение обмена железа, связанное с его задержкой в органах и клетках ретикуло-эндотелиальной системы и замедленным поступлением в костный мозг— так называемый «функциональный» дефицит железа.
Снижение продукции эндогенного эритропоэтина и недостаточная способность костного мозга к повышенной продукции эритроцитов также является одним из патогенетических факторов АХВ при РА. Еще одной причиной анемического синдрома при РА может быть укорочение периода жизни клеток эритроидного ряда.
Поражение легких при ревматоидном артрите:
диффузный интерстициальный фиброз легких;
плеврит (сухой или экссудативный, как правило, с незначительным количеством жидкости, благополучно купируется на фоне стандартной терапии);
альвеолит (может быть сегментарным, лобулярным и крайне редко тотальным);
облитерирующий бронхиолит (встречается казуистически редко);
гранулема (создает сложности при дифференциальной диагностике).
При наличии множественных легочных узелков следует проводить дифференциальный диагноз среди следующих нозологических форм:
1.Гранулематоз Вегенера.
2.Амилоидоз.
3.Саркоидоз.
4.Опухоли (папилломатоз, бронхолегочный рак, метастазы, неходжкинская лимфома).
5.Инфекции (туберкулез, грибковые инфекции, эмболии при сепсисе).
14
Поражение легких, связанное с ревматоидным артритом, требует проведения активной подавляющей терапии с использованием высоких доз глюкокортикоидов (45 – 60 мг в сутки peros, 250 мг внутривенно капельно) с последующей коррекцией соответственно динамике процесса.
Сердечно-сосудистая система:перикардит, коронарный артериит, гранулематозное поражение сердца (редко), раннее развитие атеросклероза.
Миокардит у больных РА характеризуется тахикардией, приглушенностью тонов, систолическим шумом на верхушке. При эхокардиографии имеют место снижение фракции выброса, ударного объема, увеличение минутного объема.
Поражение почек у больных РА встречаются в 10-25% случаев (гломерулонефрит, амилоидоз). При РА наиболее часто диагностируется мезангиально-пролиферативный (около 60% случаев), реже — мембранозный вариант гломерулонефрита; они сочетаются с высокой активностью иммуновоспалительного процесса и наиболее часто проявляются изолированным мочевым синдромом, в некоторых случаях возможно развитие нефротического синдрома. Прогрессирующее поражение почек может приводить к формированию терминальной почечной недостаточности и уремии.
У больных с длительностью РА более 7-10 лет возможно развитие амилоидоза почек, для которого характерны стойкая протеинурия (потеря белка составляет до 2-3 г/сут), цилиндрурия и периферические отеки. Диагноз верифицируется на основании гистологического исследования нефробиоптата. Это самый прогностически неблагоприятный вариант поражения почек, так как средняя продолжительность жизни таких больных составляет 2-4 года. Летальный исход наступает в результате формирования терминальной почечной недостаточности.
Поражение глаз: ирит, иридоциклит, эписклерит и склерит, склеромаляция, периферическая язвенная кератопатия.
Наиболее часто (около 3,5% случаев) диагностируется иридоциклит. Ирит более характерен для ювенильного РА, но может встречаться и у взрослых. Начало процесса, как правило, острое, затем он может принимать затяжное течение, нередко осложняется развитием синехий. Эписклерит сопровождается умеренными болями, сегментарным покраснением переднего отрезка глаза; при склерите возникают сильнейшие боли, развивается гиперемия склер, возможна потеря зрения. При сочетании РА с синдромом Шегрена развивается сухой кератоконъюнктивит. Следует иметь в виду, что метотрексат, являющийся основным базисным препаратом для лечения ревматоидного артрита, может способствовать росту ревматоидных узелков в глазном яблоке. Подобная ситуация требует немедленной смены терапии.
Поражение нервной системы: симметричная сенсорно-моторная нейропатия, шейный миелит.
15
В основе патогенеза периферической полинейропатии лежит патология vasanervorum. У больных развиваются парестезии, чувство жжения в области нижних и верхних конечностей, снижается тактильная и болевая чувствительность, появляются двигательные расстройства. При активном течении РА иногда наблюдаются симптомы полиневрита с сильными болями в конечностях, чувствительными или двигательными нарушениями, атрофией мышц.
Классификационные критерии ревматоидного артрита
(ACR/EULAR, 2010г)
Ревматоидный артрит может быть заподозрен, если: -имеется, как минимум 1 припухший сустав; -исключены другие заболевания индуцирующие синовиит; -сумма по всем разделам составляет от 6 до 10 баллов.
1 крупный сустав – 0 баллов
2-10 крупных суставов – 1 балл
1-3 мелких сустава – 2 балла
4-10 мелких суставов – 3 балла
>10 суставов ( как минимум 1 мелкий сустав должен быть в их числе) - 5 баллов
Длительность синовиита:
o менее 6 недель- 0 баллов o более 6 недель – 1 балл
Изменения одного из лабораторных показателей: o РФ отр. и/или АЦЦП отр. -0 баллов
o РФ + (слабопоожительный) и/или АЦЦП + - 2 балла
o РФ ++ (резко положительный) и/ или АЦЦП ++ - 3 балла
Изменения острофазовых показателей:
o СОЭ и/или СРБ в норме – 0 баллов
СОЭ и/или СРБ повышены – 1 балл (табл.1-1). При наличии у пациента свыше трех месяцев симптоматики ревматоидного артрита следует немедленно отправить больного к ревматологу для начала ранней агрессивной терапии, поскольку именно у пациентов с коротким анамнезом существует «окно возможности», то есть промежуток времени, когда проводимое лечение способно активно подавить иммунное воспаление и повлиять на течение и исход заболевания.
Таблица 1-1
Нормальные величины острофазовых показателей
|
|
Результат определения |
|||
Показатель |
Метод |
Негативный |
Слабополо- |
Резкополо- |
|
жительный |
жительный |
||||
|
|
||||
|
|
(-) |
(+) |
(++) |
|
|
|
|
|||
|
нефелометрия, |
≤ 15 МЕ/мл |
16-45 МЕ/мл |
> 45 МЕ/мл |
|
|
турбидиметрия |
||||
|
|
|
|
||
|
латекс-агглютинация |
≤ 1/40 |
>1/40 |
- |
|
16
|
иммуноферментный |
≤ 20 МЕ/мл |
|
21-60 МЕ/мл |
> 60 МЕ/мл |
||
|
(Orgentec). |
|
|||||
|
|
|
|
|
|
||
|
иммуноферментный |
≤ 5 ЕД/мл |
|
6-15 ЕД/мл |
>15 ЕД/мл |
||
|
(Axis-Shield, |
|
|||||
АЦЦП |
Euroimmun) |
|
|
|
|
|
|
|
иммунохемилюминис |
≤ 17 ЕД/мл |
|
18 -50ЕД/мл |
> 50ЕД/мл |
||
|
ценция (Roche) |
|
|
|
|
|
|
Показатель |
Метод |
|
Результат определения |
||||
Нормальный |
Повышенный |
||||||
|
|
||||||
СРБ |
нефелометрия, |
≤ 10 мг/л |
|
> 10 мг/л |
|||
тубидиметрия |
|
||||||
|
|
|
|
|
|
||
СОЭ |
по Вестергрену |
≤ 25 мм/ч |
|
> 25 мм/ч |
|||
Дифференциальный диагноз.
В дебюте РА поражение суставов (и некоторые другие клинические проявления) сходно с поражением суставов при других ревматических и неревматических заболеваниях.
Остеоартроз. Незначительная припухлость мягких тканей, вовлечение дистальных межфаланговых суставов, отсутствие выраженной утренней скованности, увеличение выраженности боли к концу дня.
Системная красная волчанка. Симметричное поражение мелких суставов кистей, лучезапястных и коленных суставов. Артрит недеформирующий (за исключением артрита Жакку); может быть отёк мягких тканей, но внутрисуставной выпот минимален; высокие титры АНФ (однако 30% больных РА имеют АНФ), редко — низкие титры РФ; на рентгенограммах — отсутствие костных эрозий.
Подагра. Диагноз устанавливают на основании выявления кристаллов в синовиальной жидкости или тофусах с характерным отрицательным двойным лучепреломлением при поляризационной микроскопии. При хронической форме может быть симметричное поражение мелких суставов кистей и стоп с наличием тофусов; возможны субкортикальные эрозии на рентгенограммах.
Псориатический артрит. Моноартрит, асимметричный олигоартрит, симметричный полиартрит с поражением дистальных межфаланговых суставов, мутилирующий артрит, связанный с развитием остеолиза по типу «карандаш в колпачке», поражения осевого скелета. Частое поражение дистальных межфаланговых суставов, веретенообразная припухлость пальцев, характерные для псориаза изменения кожи и ногтей.
Анкилозирующий спондилит. Асимметричный моно-, олигоартрит крупных суставов (тазобедренных, коленных, плечевых), позвоночного столба, крестцово-подвздошных сочленений; возможно вовлечение периферических суставов; экспрессия HLA-B27.
Реактивный артрит. Артрит олигоартикулярный и асимметричный, с преимущественным поражением нижних конечностей, экспрессия HLAB27. Вызывается инфицированием различными микроорганизмами
(Chlamydia, Escherichiacoli, Salmonella, Campylobacter, Yersiniaи др.);
17
синдром Рейтера: уретрит, конъюнктивит и артрит; наличие болей в пяточных областях с развитием энтезисов, кератодермии на ладонях и подошвах и циркулярного баланита.
Инфекционный эндокардит. Поражение крупных суставов; лихорадка с лейкоцитозом; сердечные шумы; обязательно бактериальное исследование крови у всех пациентов с лихорадкой и полиартритом.
Ревматическая лихорадка. Мигрирущий олигоартрит с преимущественным поражением крупных суставов, кардит, подкожные узелки, хорея, кольцевидная эритема, лихорадка. Специфические (в отношении стрептококков) серологические реакции.
Септический артрит. Обычно моноартикулярный, но может быть и олигоартикулярный; с преимущественным поражением крупных суставов; может быть мигрирующим. Метод верификации: посев крови на стерильность, аспирация жидкости из полости сустава с исследованием клеточного состава, окраской по Граму и культуральным исследованием; больные РА также могут иметь септический артрит.
Вирусные артриты. Характерна утренняя скованность с симметричным поражением суставов кистей и лучезапястных суставов, может выявляться РФ, вирусная экзантема. В большинстве случаев спонтанно проходит в течение 4-6 нед (за исключением артрита, связанного с парвовирусной инфекцией).
Системная склеродермия. Феномен Рейно и уплотнение кожи; редко может выявляться артрит, обычно артралгии, ограничение объёма движений, связанное с прикреплением кожи к подлежащей фасции.
Идиопатические воспалительные миопатии. Артрит с выраженным синовитом обнаруживается редко. Воспаление мышц, характеризующееся проксимальной мышечной слабостью, повышением уровня КФК и альдолазы, артралгиями и миалгиями, патологическими изменениями на электромиограмме.
Болезнь Лайма. На ранних стадиях мигрирующая эритема и сердечно-сосудистая патология, на поздних — интермиттирующий моноили олигоартрит (у 15% больных может быть хроническим и эрозивным), энцефалопатия и нейропатия; 5% здоровых людей имеют позитивные реакции на лайм-боррелиоз.
Ревматическая полимиалгия. Диффузная боль и утренняя скованность в осевых суставах и проксимальных группах мышц; припухлость суставов выявляется реже; выраженная СОЭ; возникает в возрасте старше 50 лет. Выраженный ответ на глюкокортикоидную терапию; в 10-15% сочетается с гигантоклеточным артериитом.
Амилоидоз. Периартикулярное отложение амилоида; может быть выпот в полость сустава. Окрашивание аспирированной суставной жидкости Конго красным.
Гемохроматоз. Увеличение костных структур 2-го и 3-го пястнофаланговых суставов; повышение уровня железа и ферритина в сыворотке со снижением трансферринсвязывающей способности; на рентгенограммах
18
может выявляться хондрокальциноз. Диагностируется с помощью биопсии печени.
Саркоидоз. Хроническое гранулематозное заболевание, в 10-15% сопровождающееся хроническим симметричным полиартритом.
Гипертрофическая остеоартропатия. Олигоартрит коленных,
голеностопных и лучезапястных суставов; периостальное новообразование кости; глубокая и ноющая боль, «барабанные палочки», связь с легочным заболеванием, боль в конечностях при определённом положении.
Семейная средиземноморская лихорадка. Рецидивирующие атаки острого синовита (моноили олигоартикулярного)крупных суставов, ассоциированные лихорадкой, плевритом и перитонитом.
Рецидивирующий полихондрит. Распространённое прогрессирующее воспаление и деструкция хрящевой и соединительной ткани; мигрирующий асимметричный и неэрозивный артрит мелких и крупных суставов; воспаление и деформация хряща ушной раковины.
Фибромиалгия. Распространённая мышечно-скелетная боль и скованность, парестезии, непродуктивный сон, усталость, множественные симметричные «триггерные» точки (для диагноза достаточно наличие 11 из 18); лабораторные исследования и исследование суставов — без патологии.
Особые формы РА. Синдром Фелти.
Назван по имени автора описавшего его в1924 году. Встречается у 1% больных ревматоидным артритом.
Включает в себя:
-хронический артрит;
-спленомегалию;
-лейкопению.
Суставной синдром:
-может развиваться после других проявлений заболевания, но чаще предшествует им.
Характеризуется тяжелым деструктивным полиартритом, хотя возможно и доброкачественное течение.
Внесуставные проявления:
-ревматоидные узелки;
-хронические язвы голени;
-полиневропатия;
-эписклерит;
-часто повышение температуры тела;
-амиотрофия.
При лабораторных исследованиях выявляются: анемия, лейкопения и нейтропения, увеличение СОЭ, высокие титры РФ.
Синдром Стилла у взрослых (ССВ).
19
Был описан Bywaters в 1971году. Чаще развивается в возрасте 16-35 лет (до 88% случаев). Триггерным фактором выступает носоглоточная инфекция.
ССВ характеризуется:
-высокой лихорадкой;
-миокардитом;
-перикардитом;
-лимфаденопатией;
-спленомегалией;
-кожной сыпью.
Диагностические критерии ССВ.
Основные:
-длительная лихорадка;
-артрит или стойкие артралгии;
-макулопапулезная сыпь;
-серонегативность по РФ;
-нейтрофильный лейкоцитоз;
-развитие болезни после 16 лет.
Дополнительные:
-лимфаденопатия;
-гепатоспленомегалия;
-полисерозит;
-носоглоточная инфекция.
Достоверным считается диагноз при наличии 4 основных признаков.
Лечение ревматоидного артрита.
Концепция TREAT to TARGET - «Лечение до достижения цели» - является главенствующей при принятии решенияо выборе тактики лечения у пациента с ревматоидным артритом.
1.Первичная цель лечения РАдостижение состояния клинической ремиссии (уровень доказательности А).
2.Клиническая ремиссия определяется, как отсутствие признаков значимой воспалительной активности.
3.Приемлемой альтернативной целью лечения является достижение низкой активности РА (уровень доказательности А), особенно при стабильном состоянии и длительно протекающем заболевании.
4.До тех пор пока не будет достигнута цель лечения , пересмотр терапии осуществляется не реже, чем 1 раз в 3 месяца.
5.Необходимо регулярно документировать данные об активности заболевания у пациентов с высокой/умеренной активностью – ежемесячно, стабильным течением и низкой активностью -1 раз в 3 месяца.
6.В ежедневной клинической практике необходимо использовать общепринятые методики оценки состояния суставов.
7.При принятии клинических решений следует учитывать изменения структурные и нарушения функции суставов.
20
8.Желаемая цель лечения должна поддерживаться на продолжении всего течения заболевания.
9.На тактику лечения могут влиять сопутствующие заболевания и прием других лекарственных препаратов.
10.Пациент должен быть информирован о цели лечения.
Цели терапии:
-уменьшение симптомов, включая недомогание, боли, отек, скованность суставов;
-предотвращение деструкции, нарушения функции и деформации суставов;
-сохранение качества жизни;
-достижение клинической ремиссии;
-увеличение продолжительности жизни.
«21 век ознаменовался сменой парадигмы в фармакотерапии РА» (академик РАМН Е.Л. Насонов).
В настоящее время к основным стратегиям терапии данного заболевания относятся:
1.«Ранняя» агрессивная терапия базисными противовоспалительными препаратами (БПВП) (уровень доказательности А);
2.Тщательный контроль эффективности лечения;
3.Использование инновационных подходов в лечении РА (генноинженерные биологические препараты) (уровень доказательности А).
Группы лекарственных препаратов, используемых в лечении
РА.
1.Симптоматическая терапия:
Нестероидные противовоспалительные препараты (НПВП):
А) неселективные (ингибирующие ЦОГ – 1 иЦОГ – 2 ) НПВП: Б) селективные ингибиторы ЦОГ-2; В) специфические ингибиторы ЦОГ-2
2.Глюкокортикоиды.
3.Базисные противоспалительные препараты (БПВП):
-синтетические БПВП;
-генно-инженерные биологические препараты (ГИБП).
НПВП.
Для уменьшения болей в суставах применяют НПВП, которые
оказывают хороший симптоматический (анальгетический) эффект, но не влияют на прогрессирование деструкции суставов, прогноз заболевания и могут вызывать тяжелые нежелательные реакции со стороны желудочнокишечного тракта и кардиоваскулярной системы (уровень доказательности А).
Неселективные НПВП
Ибупрофен 1200-2400 мг/сут в 4 приема. Кетопрофен 100-400 мг/сут в 3-4 приема. Флурбипрофен 100-300 мг/сут в 3-4 приема.
21
Диклофенак75 мг в/м – 1 раз в сутки Лорноксикам(8 мг) по 1 т. 1-2 раза в день; в/в или в/м в дозе 8-16 мг.
Селективные НПВП
Мелоксикам 7,5 - 15 мг/сут в 1 прием. НАЙЗ(нимесулид)(100 мг) по 1 т – 2 раза в день.
Специфические ингибиторы ЦОГ 2
Целекоксиб 100-200 мг/сут в 1-2 приема;эторикоксиб 60-120 мг/сут. Для профилактики НПВП-гастропатии необходимо назначить
ингибиторы протонной помпы – пантопрозол 20 мг - 1 раз в сутки. Глюкокортикоиды. Лечение ГК (низкие/средние дозы)
рекомендуются в комбинации с БПВП в качестве компонента комбинированной терапии РА, для купирования обострения до развития эффекта БПВП (bridge-терапия) или в виде монотерапии при неэффективности (или невозможности) назначения БПВП и ГИБП; прием ГК сопровождается развитием побочных эффектов, требующих тщательного мониторинга (уровень доказательности А). Применение ГК при РА должно быть ограничено строгими показаниями и осуществляться ревматологами.
Лечение низкими (< 15 мг/ сут) дозами ГКС позволяет быстро и адекватно контролировать ревматоидное воспаление.
Назначение ГКС показано больным при наличии системных проявлений (преднизолон, метилпреднизолон).
Пульс-терапия ГКС (метипред) позволяет достигнуть быстрого (в течение 24 часов), но кратковременного (3-12 нед) подавления активности воспалительного процесса, даже у больных, резистентных к предшествующей терапии.
Для профилактики и лечения остеопорозаБОНВИВА(ибандроновая кислота) (150 мг) 1 т. в месяц или БОНВИВА(3 мг/3мл) 1 в/в инъекция 1 раз в 3 месяца – длительно. ТЕВАНАТ(алендроновая кислота) - 70 мг раз в неделю.АЛЬФА Д3-ТЕВА (альфакальцидол) – 1 капс. в сутки (0,25 мкг, 0,5 мкг, 1 мкг) (уровень доказательности А).
Локальная терапия РА.
Занимает важное место в комплексе лечебных мероприятий. Подавляет местную активность процесса, положительно влияет на течение заболевания в целом.
С этой целью используют внутрисуставное введение ГКС, которое дает очень быстрый, но недостаточно стойкий эффект.
Для внутрисуставного введения применяют метипред, бетаметазон (20-40 мг в крупные, 10-20 мг в средние и 5-10 мг в мелкие суставы, 0,5-2 мл).
Базисная (болезнь-модифицирующая противовоспалительная) терапия РА.
К числу «базисных» относят разнообразные по химической структуре и фармакологическим свойствам лекарственные средства.
22
Их объединяет способность в большей или меньшей степени и за счет различных механизмов подавлять воспаление и/или патологическую активацию системы иммунитета и контролировать течение заболевания.
Терапия БПВП должна проводиться всем без исключения пациентам с РА и назначаться как можно раньше (в пределах 3-6 мес. от момента развития симптомов болезни) (уровень доказательности А).
Метотрексат (МТ) – препарат «первой линии» лечения РА с доказанной эффективностью и безопасностью (уровень доказательности A). У пациентов, впервые начавших лечение МТ, соотношение эффективности/безопасность/стоимость в пользу монотерапии МТ по сравнению с комбинированной терапией МТ и другими стандартными БПВП и монотерапией ГИБП (уровень доказательности А).
Лечение МТ следует начинать с дозы 10-15 мг/неделю с увеличением по 5 мг каждые 2-4 недели до 25-30 мг/неделя в зависимости от эффективности и переносимости (уровень доказательности В).
При недостаточной эффективности и переносимости (не тяжелые нежелательные реакции) перорального МТ, целесообразно назначение парентеральной (подкожной) формы препарата (уровень доказательности
B).
На фоне лечения МТ обязателен прием не менее 5 мг фолиевой кислоты в неделю (уровень доказательности A).
В начале лечения или при увеличении дозы МТ, определение АЛТ/АСТ, креатинина, общий анализ крови необходимо проводить каждые 1-1,5 месяца до достижения стабильной дозы МТ, затем – каждые 3 месяца; клиническую оценку нежелательных реакций и факторов риска следует проводить во время каждого визита пациентов (уровень доказательности С). Лечение МТ следует прервать при повышении концентрации АЛТ/АСТ > 3 верхней границы нормы (ВГН); возобновить лечение в более низкой дозе после нормализации показателей. При стойком увеличении уровня АСТ/АЛТ > 3 ВГН, следует скорректировать дозу МТ; при сохранении увеличения уровня АСТ/АЛТ > 3 ВГН после отмены МТ, следует провести соответствующие диагностические процедуры. (Уровень доказательности C)
Альтернативой является АРАВА (лефлуномид) – 3 дня по 100мг; далее по 20 мг/сут (уровень доказательности А). Высокая эффективность АРАВЫ и минимальные побочные эффекты позволяют использовать препарат для широкого круга пациентовс ревматоидным артритом. Оба цитотоксических препарата могут быть назначены только врачамиревматологами. Однако, мониторинг их эффективности осуществляет лечащий врач - терапевт.
Плаквенил (гидроксихлорохин) используется в качестве монотерапии при низкой активности РА и отсутствии факторов
23
неблагоприятности и длительности заболевания не более 1 года (уровень доказательности С).
Сульфасалазинприменяется в качестве монотерапии при любой длительности РА в отсутствие факторов неблагоприятного прогноза и незначительной активности заболевания (0,5 г/сутки внутрь с постепенным увеличением до 2-3 г/сут в 2 приема после еды).
Болезнь-контролирующая терапия.
Болезнь-контролирующая терапия с использованием генноинженерных биологических препаратов (ГИБП) позволяет достичь максимальной избирательности воздействия на иммунные патогенетические механизмы развития РА, устранить единственно значимое звено и разорвать патогенетическую цепь событий, существенно не влияя на функционирование других органов и систем.
Главным инструментом данного вида терапии являются моноклональные антитела, направленные против определенных иммунокомпетентных клеток и цитокинов, играющих ключевую роль в патогенезе РА. Благодаря использованию генно-инженерных биологических агентов стало реальностью индукция ремиссии у больных с тяжелым, неконтролируемым посредством БПВП, течением РА. Впервые появилась возможность считать реальнодостижимой целью лечения РА индукцию стойкой, а иногда и безмедикаментозной ремиссии у пациентов с прогностически неблагоприятными субтипами РА. Внедрение в клиническую практику биологических препаратов сделало возможным торможение суставной деструкции, обратное развитие эрозивных костных изменений, что способствует частичному восстановлению патологически измененных суставных структур даже при тяжелом и длительном течении РА.
Для лечения РА используются ГИБП, к которым относятся ингибиторы ФНО-α (инфликсимаб - ИНФ, адалимумаб – АДА, этанерцепт
– ЭТЦ, цертолизумаба пегол – ЦТЗ, голимумаб – ГЛМ), анти- В
клеточный препарат – ритуксимаб (РТМ), блокатор костимуляции Т – лимфоцитов – абатацепт (АБЦ) и блокатор рецепторов интерлейкина 6 – тоцилизумаб (ТЦЗ) (уровень доказательности А).
Для увеличения эффективности терапии, ГИБП целесообразно сочетать с применением МТ (уровень доказательности А).
У пациентов с непереносимостью МТ возможно проведение монотерапии ингибиторами ФНО-α (АДА, ЭТЦ, ЦЗП), блокатором ИЛ-6Р (ТЦЗ) или комбинированной терапии ГИБП и другими стандартными БПВП (уровень доказательности В).
Первыми биологическими препаратом, использованным в России для лечения РА стал препарат инфликсимаб (моноклональные химерные антитела к фактору некроза опухоли α (ФНО-α)). Благодаря блокирующему эффекту в отношении ФНО-α, инфликсимаб подавляет синтез основных медиаторов воспаления, участвующих в процессах деструкции хряща и кости (уровень доказательности А).
24
Инфликсимаб (Ремикейд) применяется в дозе 3 мг/кг, вводится в/в капельно, через инфузомат. Кратность введений определена общепринятой схемой согласно рекомендациям Европейской антиревматической лиги (ЕULAR) и Российскими национальными рекомендациями по ревматологии (НИИ ревматологии РАМН) и составляет 14 инфузий на курс лечения. Длительность курса лечения составляет 1 год. Затем тактика лечения может быть изменена врачом-экспертом (ревматологом).
Хумира - (адалимумаб) - 40 мг 2 раза в месяц в/кожно — это рекомбинантное моноклональное антитело, пептидная последовательность которого идентична человеческому.Хумира обладает специфичностью и высокой степенью родства к растворимому фактору некроза опухоли (ФНО-α), но не связывается с лимфотоксином (ФНО-β).Адалимумаб нейтрализует биологические эффекты ФНО, блокируя его взаимодействие с р55 и р75 рецепторами ФНО на поверхности клетки (уровень доказательности А).
Мабтера (ритуксимаб - РТМ) - химерные моноклональные антитела к CD 20 антигену В-лимфоцитов. РТМ целесообразно назначать пациентам РА, серопозитивных по РФ и/или АЦЦП, другими аутоиммунными нарушениями или имеющими противопоказания для назначения ингибиторов ФНО-α); для поддержания эффекта необходимо проведение повторных курсов РТМ через 6 месяцев после предыдущего курса (уровень доказательности В).
Применяется в виде в/в инфузий, осуществляемых через инфузомат. Курс лечения ритуксимабом составляет 2 инфузии с интервалом в 2 недели, повторный 2 курс лечения проводится через 6 месяцев.
Лечение ритуксимабом не только способствует развитию клиниколабораторной ремиссии, но и тормозит эрозирование суставов, сохраняет их функциональные способности и улучшает качество жизни больных.
АКТЕМРА – представляет собой гуманизированные моноклональные антитела подкласса JgG1, которые связываясь с мИЛ-6 Р и рИЛ-6 Р, ингибируют оба сигнальных пути ИЛ-6 зависимой клеточной активации (уровень доказательности А). Актемра первый и единственный препарат, обладающий способностью подавлять ИЛ-6 зависимые воспалительные реакции, разрешенный к применению при заболеваниях человека (академик РАМН Е.Л. Насонов / Применение тоцилизумаба (Актемры) при ревматоидном артрите 2009).
Использование тоцилизумаба в дозе 8 мг (0,4 мл) на 1 кг веса в/в, затем повторить через 4 нед. у пациентов с РА, способствует развитию стойкой клинико-лабораторной ремиссии у каждого второго пациента, получавшего курс лечения тоцилизумабом в течение 1 года.
АКТЕМРА (тоцилизумаб) занимает уникальное место в лечении РА. Применение Актемры позволяет достичь оптимального контроля над течением заболевания, способствует быстрому развитию клиниколабораторной ремиссии.
25
Вероятно, в будущем использование Актемры в терапии РА, позволит максимально индивидуализировать и значимо повысить эффективность лечения.
ОРЕНСИЯ (абатацепт) – растворимая гибридная белковая молекула, состоящая из внеклеточного домена CTLA4 человека и модифицированного Fc (CH2 и CH3 области) фрагмента IgG1. Абатацепт эффективно подавляет клинические проявления РА и улучшает физическую активность у больных с умеренно тяжелым/тяжелым РА при неадекватном эффекте метотрексата и ингибиторов ФНО- , у пациентов с ранним РА, не получавших метотрексат и имеющих факторы риска неблагоприятного прогноза. Абатацепт снижает риск трансформации недифференцированного артрита в РА. Лечение абатацептом проводят путем внутривенной инфузии в дозе 10 мг/кг (500 мг при массе тела больного менее 60 кг, 750 мг при массе 60-100 кг и 1000 мг при массе более 100 кг), через 2 и 4 недели, а затем ежемесячно (уровень доказательности А).
Лечение генно-инженерными биологическими препаратами
осуществляется исключительно при назначении их врачами-экспертами (ревматологами, имеющими соответствующий опыт), в условиях специализированных кабинетов (центров) генно-инженерной биологической терапии. В настоящее время на территории Российской Федерации таких центров 58.
Нефармакологические методы лечения.
Лечебная физкультура. Физиотерапия.
Ортопедические пособия - применяют ортезы – особые приспособления из термопластика, надеваемые на время сна и удерживающие сустав в правильном положении.
Хирургическое лечение.
Показания: резистентные к лекарственной терапии синовиты, тендосиновиты или бурситы, выраженный болевой синдром, значительное ограничение движений в суставе, тяжёлая деформация суставов.
Основные виды оперативного лечения: протезирование суставов,
синовэктомия, артродез.
26

ГЛАВА 2. ОСТЕОАРТРОЗ.
Остеоартроз– это гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими и клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц.
Факторы риска остеоартроза (ОА):
пожилой возраст;
избыточный вес;
наследственная предрасположенность;
гормональные нарушения;
остеопороз;
гипермобильность, а также другие заболевания (сахарныйдиабет, гипертензия и гиперурикемия);
механические факторы, такие как травма сустава (разрывы крестовидных и коллатеральных связок, переломы костей);
физические и спортивные нагрузки;
профессиональная деятельность (тяжелый физический труд).
Патогенетические механизмы остеоартроза.
При формировании ОА изменяется баланс между катаболическими и анаболическими процессами и, как результат, происходит разрушение суставного хряща и нарушение формирования новой хрящевой ткани
(рис.2-1).
Рис.2-1. Повреждение хондроцитов
Классификация ОА.
I.Идиопатический.
АЛокальный:
1.Кисти: узелки Гебердена и Бушара.
2.Вальгусный большой палец стопы.
27
3 Коленные суставы.
4.Тазобедренные суставы.
5.Позвоночник.
6.Другие суставы.
Б. Генерализованный (включает три группы суставов и
более).
II.Вторичный.
1.Травма: острая, хроническая (профессиональная,
спортивная).
2. Врожденные, приобретенные заболевания: болезнь КальвеПертеса, врожденный вывих тазобедренного сустава, смещенный эпифиз.
3.Заболевания обмена веществ.
-Охроноз.
-Гемохроматоз.
-Болезнь Уилсона - Коновалова.
-Болезнь Гоше.
4.Эндокринопатии.
-Акромегалия.
-Гиперпаратиреоз.
-Сахарный диабет.
-Ожирение.
-Гипотиреоз.
5. Заболевания с нарушением отложения кальция: -пирофосфатная артропатия -апатическая артропатия
6. Другие заболевания костей и суставов: трещины, аваскулярный некроз, инфекции, подагра, болезнь Педжета, остеопороз, остеохондроз.
7.Нейропатии: (болезнь Шарко).
8.Эндемические расстройства: (болезнь Кашина-Бека).
9.Другие состояния:обморожение, кессонная болезнь, гемоглобинопатия.
Клиническая картина. Общие признаки ОА.
Отсутствие внесуставного поражения.
Поражение суставов, выполняющих максимальную нагрузку. Медленное прогрессирование заболевания.
Связь заболевания с возрастом.
1.Клинические симптомы ОА обычно проявляются у людей среднего и пожилого возраста.
2.Утренняя скованность в суставах длится не более 30 минут.
3.Пациенты с ОА часто имеют ощущение неустойчивости в
суставе.
28

4. Пациенты с ОА ощущают крепитацию во время движения в пораженном суставе. Может наблюдаться развитие дефигурации (рис.4) сустава, появление умеренного синовита.
Диагностические параметры верификации диагноза ОА представлены в таблице 2-1.
Таблица 2-1
Диагностические параметры верификации диагноза ОА
(EULAR 2010)
Диагностические параметры верификации диагноза ОА |
Уровень |
|
|
|
доказа- |
|
|
тельности |
ОА характеризуется наличием механических болей в суставах и |
IIb |
|
ограничением подвижности в них. В основе патогенеза ОА лежит |
|
|
деструкция хряща, формирование остеофитов и вовлечение в |
|
|
патологический процесс периартикулярных тканей. |
|
|
|
|
|
Факторы риска ОА: ожирение, возраст старше 50 лет, женский пол, |
Ia-IIb |
|
травмы в анамнезе, интенсивная физическая нагрузка, генетическая |
|
|
предрасположенность |
|
|
|
|
|
Наличие типичных для ОА симптомов: усиление механических болей |
Ib-IIb |
|
в суставах к концу дня, уменьшающихся в покое, утренняя |
|
|
скованность не более 30 мин., наличие крепитации |
|
|
|
|
|
Наличие типичных для ОА деформаций: варусная деформация |
Ia-III |
|
голеней (genuvarum ) и вальгусная деформация первых |
|
|
плюснефаланговых суставов ( galusvalgus ) |
|
|
|
|
|
Типичные для ОА |
рентгенологические изменения : сужение |
Ib-IIb |
суставной щели, субхондральный остеосклероз, наличие остеофитов |
|
|
|
|
|
Отсутствие внесуставных проявлений |
Ia |
|
|
|
|
Боль и ограничение функции сустава – главные клинические проявления ОА.
Причины болей в суставах при ОА представлены на схеме.
Боли вначале возникают при больших нагрузках (длительная ходьба, подъем тяжестей, длительное вынужденное положение тела) и быстро
29
проходят в покое или при устранении причины перегрузки сустава. По мере прогрессирования ОА боли становятся более интенсивными, длительными, возникают при любых движениях, не исчезают в покое и могут беспокоить даже ночью.
Стартовые боли возникают при наличии реактивного синовита в начале ходьбы (нагрузки), затем быстро исчезают и возобновляются после продолжающейся физической нагрузки.
Рефлекторные боли возникают из-за реактивного синовита, который приводит к рефлекторному спазму близлежащих мышц и их гипоксии.
Отраженные боли связаны с вовлечением в воспалительнодегенеративный процесс капсулы сустава, что ведет к сдавлению нервных окончаний и появлению боли, усиливающейся при движении сустава (увеличивается растяжение капсулы). Они могут появляться и в области непораженного сустава, например, при поражении тазобедренного сустава боли могут ощущаться в коленном суставе (рефлекторная иррадиация болей).
«Блокадная боль» возникает при периодическом «заклинивании» сустава в результате ущемления секвестра хряща (суставная «мышь») между суставными поверхностями. Это обычно внезапная резкая боль, блокирующая движения в суставе, внезапно исчезающая при определенном положении эпифизов, создающих условия к соскальзыванию «мыши» с суставной поверхности.
Чаще всего причинами болей при ОА являются реактивный синовит, периартрит и спазм близлежащих мышц.
Объективные данные.
Болезненность сустава и периартикулярных тканей. При наличии синовита выявляются припухлость и повышение температуры кожи в области сустава. Иногда в полости сустава определяется небольшое количество жидкости по данным УЗИ. Синовит часто сопровождается тендобурситом, который проявляется ограниченной припухлостью, болезненностью при пальпации и энтезопатией. У больных нередко выявляется атрофия регионарных мышц.
Характерным для ОА является ограничение подвижности сустава и вынужденное положение конечности, однако полного отсутствия
движения в нем не наблюдается. |
В начальной |
стадии заболевания |
||
может отмечаться дефигурация |
сустава, |
связанная |
с |
|
синовиальным |
или периартикулярным отеком, а также наличием |
|||
внутрисуставноговыпота.При длительном течении заболевания выявляется отчетливая деформация суставов.
30

Рентгенологические признаки ОА (табл. 2-2).
1. Рентгенологические характеристики, определяющие стадию
ОА:
а) величина остеофитов; б) сужение суставной щели;
в) склероз субхондральной кости; г) маленькие ложные кисты со склеротическими стенками, обычно
расположенные в субхондральной кости; д) измененные размеры концов кости, в частности головки бедра.
Основные рентгенологические признаки ОА: сужение суставной щели, остеофитоз, субхондральный остеосклероз (рис. 2-2) .
Таблица 2-2
Рентгенографические критерии для определения ОА(Kellgren - Lawrence, 1975).
Стадия 0 |
нет ОА |
отсутствуют |
рентгенологические |
||
|
|
признаки. |
|
|
|
Стадия 1 |
сомнительный ОА |
мелкий |
остеофит, |
сомнительное |
|
|
|
значение. |
|
|
|
Стадия 2 |
минимальный ОА |
четкий |
остеофит, |
неизмененная |
|
|
|
суставная щель. |
|
|
|
Стадия 3 |
средний ОА |
умеренное сужение суставной щели, |
|||
|
|
множественные остеофиты. |
|||
Стадия 4 |
выраженный ОА |
значительное сужение суставной щели |
|||
|
|
(почти не прослеживается) со |
|||
|
|
склерозом |
субхондральной кости, |
||
|
|
грубые остеофиты |
|
|
|
Рис. 2-2. Остеоартроз коленных суставов (3 ст. по Келлегрену).
31

Лабораторных критериев для данного заболевания не существует. Для дифференциальной диагностики: клинический анализ крови, ревматоидный фактор, уровень мочевой кислоты.
Перед началом лечения: общий анализ крови, мочи, креатинин сыворотки, сывороточные аминотрансферазы с целью определения возможных противопоказаний для назначения противовоспалительной терапии.
Анализ синовиальной жидкости. В целях дифференциальной диагностики - только при наличии синовита. Для ОА характерен невоспалительный характер синовиальной жидкости: прозрачная, вязкая, с концентрацией лейкоцитов менее 2000/мм3.
Критерии диагностики.
Диагноз «ОА» ставят на основании клинических и рентгенологических критериев (Альтман и др., 1991) (табл. 2-3.).
Таблица 2-3
Диагностические критерии остеоартроза (по Altmanet., 1991)
Клинические критерии |
Клинические, |
лабораторные |
и |
|
рентгенологические критерии |
|
|
Коленные суставы |
|
|
|
1. Боль и |
1. Боль и |
|
|
2а. Крепитация |
2. Остеофиты или |
|
|
26. Утренняя скованность <30 мин |
За. СЖ, характерная для остеоартроза (или возраст |
||
2в. Возраст >38 лет или |
≥40 лет) |
|
|
За. Крепитация |
36. Утренняя скованность <30 мин |
|
|
36. Утренняя скованность ≤30 мин |
Зв. Крепитация |
|
|
Зв. Костные разрастания или |
|
|
|
4а. Отсутствие крепитации |
|
|
|
46. Костные разрастания |
|
|
|
Чувствительность — 89% |
Чувствительность — 94% |
|
|
Специфичность — 88% |
Специфичность — 88% |
|
|
Тазобедренные суставы |
|
|
|
1. Боль и |
1. Боль и не менее двух критериев из трёх |
|
|
2а. Внутренняя ротация <15° |
2а. СОЭ <20 мм/ч |
|
|
26. СОЭ <15 мм/ч |
26. Остеофиты |
|
|
(или сгибание в тазобедренном |
2в. Сужение суставной щели |
|
|
суставе >115°) или |
|
|
|
3а. Внутренняя ротация <15° |
|
|
|
3б. Утренняя скованность <60 мин |
|
|
|
3в. Возраст >50 лет |
|
|
|
3г. Боль при внутренней ротации |
|
|
|
Чувствительность — 86% |
Чувствительность — 89% |
|
|
Специфичность — 75% |
Специфичность — 91% |
|
|
Суставы кистей
1. Боль продолжительная или скованность
2. Костные разрастания двух и более суставов из 10 оцениваемых*
3. Менее двух припухших пястно-фаланговых суставов
4а. Костные разрастания, включающие 2 и более дистальных межфаланговых сустава (2-й и 3-й дистальные межфаланговые суставы могут приниматься во внимание в двух критериях: 2 и 4а) или
32

46. Деформация одного и более суставов из 10 оцениваемых*
Чувствительность — 93%
Специфичность — 91%
* 2-й и 3-й дистальные межфаланговые суставы; 2-й и 3-й проксимальные межфаланговые суставы; 1-й запястно-пястный сустав обеих кистей.
Лечение ОА.
33
Цели лечения:
•Обеспечить понимание больным своего заболевания и умение управлять им: изменение образа жизни, применение физических упражнений, поддерживающих функцию суставов, защита суставов.
•Уменьшить боль.
•Улучшить функциональное состояние суставов и предотвратить развитие деформации суставов и инвалидизации больного.
•Улучшить качество жизни больных.
•Предотвратить дальнейшее разрушение суставного хряща.
•Избежать побочных эффектов фармакотерапии и обострения сопутствующих заболеваний.
Нефармакологические методы.
1. Обучение больных должно быть обязательным компонентом всех
терапевтических программ при ОА, проводиться с учетом индивидуальных особенностей больного и включать рекомендации по изменению образа жизни, снижению веса и необходимости выполнения физических упражнений (уровень доказательности А, В).
2.Больным ОА с избыточным весом (ИМТ более 25 кг/м2) рекомендуется уменьшение веса (уровень доказательности В,С).
3.Больным ОА коленных суставов необходимы регулярные физические упражнения, направленные на укрепление силы четырехглавой мышцы бедра и увеличение объема движений, а также аэробные нагрузки (уровень доказательности А). При ОА тазобедренных суставов тоже требуется выполнение лечебной физкультуры, особенно силовых упражнений (уровень доказательности С).
4.При поражении медиального отдела коленного сустава, варусной деформации или нестабильности коленного сустава могут использоваться коленные ортезы (уровень доказательности В) и клиновидные ортопедические стельки (уровень доказательности С). Рекомендуется хождение с тростью в руке, противоположной поражённой нижней конечности (уровень доказательности С). При ОА 1–го запястно-пястного сустава применяются шинирование и ортезы (уровень доказательности В).
5.Физиотерапевтические методы. При ОА коленных суставов с признаками воспаления можно рекомендовать применение холодовых аппликаций (пакеты со льдом, массаж льдом) (уровень доказательности В). Для уменьшения боли при ОА коленных и суставов кистей рекомендуются тепловые процедуры (уровень доказательности В), чрезкожная электронейростимуляция (уровень доказательности А,В). У некоторых больных может использоваться акупунктура (уровень доказательности В).
Лекарственная терапия.
Главный симптом ОА - боль. Поэтому анальгетическая терапия, как эффективный контроль над болью, является важным направлением
влечении ОА.
34

Симптоматические лекарственные средства быстрого действия. Нестероидные противовоспалительные препараты (НПВП).
НПВП показаны при ОА в случае неэффективности парацетамола, а также при наличии признаков воспаления (уровень доказательности А). При сильной боли в суставах лечение следует начинать сразу с НПВП (уровень доказательности А). НПВП применяются в минимальной эффективной дозе назначаются на максимально короткие сроки (уровень доказательности А).
Неселективные НПВП.
Ибупрофен 1200-2400 мг/сут в 4 приема.
Аркетал (кетопрофен) 100-400 мг/сут в 3-4 приема. Флурбипрофен 100-300 мг/сут в 3-4 приема. НАКЛОФЕН (диклофенак)75 мг в/м – 1 раз в сутки
КСЕФОКАМ (лорноксикам) (8 мг) по 1 т. 1-2 раза в день; в/в или в/м в дозе 8-16 мг.
Селективные НПВП.
Мелоксикам 7,5 в/м - 15 мг/сут в 1 прием. НАЙЗ(нимесулид) (100 мг) по 1 т – 2 раза в день.
Специфические ингибиторы ЦОГ 2.
Целекоксиб 100-200 мг/сут в 1-2 приема;эторикоксиб 60-120 мг/сут. Для профилактики НПВП-гастропатии необходимо назначить
ингибиторы протонной помпы –пантопразол 40 мг - 1 раз в сутки.
Базисная терапия остеоартроза (уровень доказательности А)
представлена в таблице 2-4
|
|
Таблица 2-4 |
||
Базисная терапия остеоартроза |
||||
Препарат |
Суточная доза |
Длительность |
|
|
|
|
приема |
|
|
ХОНДРОКСИД |
750 мг 2 раза/сут |
1-2 года |
|
|
(Хондроитин сульфат) |
первые 3 нед., затем |
|
|
|
|
по 500 мг 2 раза в |
|
|
|
|
сутки |
|
|
|
СТОПАРТРОЗ |
1500 мг 1 раз в день |
1-2 года |
|
|
(Глюкозамина сульфат) |
|
|
|
|
|
|
|
|
|
хондроитин сульфат 400 |
2 капс. 3 раза в день |
1-2 года |
|
|
мг+глюкозамина сульфат |
|
|
|
|
500 мг, глюкозамин сульфат |
|
|
|
|
250 мг + ибупрофен 100 мг + |
2 капс. 3 раза в день |
1-2 года |
|
|
хондроитина сульфат 200 мг) |
|
|
|
|
Диацереин (диафлекс) |
50 мг. 2 раза в день |
не менее 4 мес. |
|
|
|
|
|
|
|
Пиаскледин |
1 капс. в сутки |
1-2 года |
|
|
35
АЛФЛУТОП - стерильный экстракт морских организмов, стимулирующий синтез гиалуроновой кислоты и тормозящий синтез гиалуронидазы.
Внутрисуставные инъекции алфлутопа эффективны, даже при наличии признаков синовита. Они выполняются курсами по 5 инъекций в каждый сустав, 1 инъекция в 3 дня, 2-3 раза в течение года.
Прекрасно переносится и сопоставимо по эффективности с внутрисуставным введением, в/м введениеалфлутопа ( 2 мл ) ежедневно в течение 10 дней.
Внутрисуставное введение глюкокортикоидов (ГЛК) показано при ОА коленных суставов с симптомами воспаления (уровень доказательности А). При ОА ГКС вводят в коленные суставы для уменьшения боли и симптомов воспаления. Рекомендуется использовать однократные инъекции метилпреднизолона (40 мг) или триамцинолона (20 мг или 40 мг). Не рекомендуется выполнять более 2–3 инъекций в год в один и тот же сустав.
Симптоматические лекарственные средства медленного действия.
Препараты-ортезы. Препараты, содержащие хондроитин сульфат и глюкозамин сульфат рекомендуются при ОА для уменьшения боли, улучшения функции суставов; эффект сохраняется в течение нескольких месяцев после их отмены, хорошо переносятся больными (уровень доказательности А).
Гиалуроновая кислота (демпфер и лумбрикант), применяется только для внутрисуставных инъекций); по 5 инъекций в каждый коленный сустав
(уровень доказательности А).
Хирургическое лечение: эндопротезирование суставов (уровень доказательности А).
Показания: ОА с выраженным болевым синдромом, не подающимся консервативному лечению; нарушение функции сустава (до развития значительной деформации, нестабильности сустава, контрактуры и мышечной атрофии).
Артроскопические манипуляции: лаваж коленных суставов, удаление «суставной мыши».
36
ГЛАВА 3. ПОДАГРА.
Подагра–системное тофусное заболевание, развивающееся в связи с воспалением в местах отложения кристаллов моноурата натрия (МУН)
улиц с гиперурикемией, обусловленным внешнесредовыми и/или генетическими факторами.
Термин “подагра” имеет греческое происхождение и составлен из слов “podus” - нога и “agrios” – жестокий.
Вкниге "Болезни древних людей" Рохлин Д.Г. описывает обнаруженные им плюсневые кости со следами подагры при раскопках богатых погребений в Новгороде ("...вот следствие постоянных пиров с объеданием и возлияниями"). В древности люди умоляли подагру о пощаде: "Будь милостива к нам, ты, всему миру известная и всех устрашающая подагра, пусть причиняемая тобою боль будет легкой и кратковременной, а не ужасной и невыносимой, пусть она не превращает нас в калек" (Лукиан).
Эпидемиология.
По экспертным оценкам подагрой страдает не менее 0,1-1% взрослого населения. Частота подагрического артрита в различных популяциях колеблется и составляет от 5 до 50 на 1000 мужчин и 1—9 на 1000 женщин, а число новых случаев в год - соответственно 1 —3 на 1000
умужчин и 0,2 на 1000 у женщин. Соотношение мужчин и женщин составляет 2-7:1.
Пик заболеваемости: 40—50 лет у мужчин, 60 лет и старше у женщин.
Этиология.
Подагра возникает вследствие различных по происхождению нарушений метаболизма мочевой кислоты (синтеза и/или выведения), приводящих к стойкому повышению её уровня в крови – гиперурикемии. Европейская лига по борьбе с ревматизмом рекомендует считать гиперурикемией уровень мочевой кислоты выше 360 ммоль/л.
Выделяют первичную и вторичную подагру (гиперурикемию).
Вторичной подагра признается тогда, когда она является лишь одним из синдромов другого заболевания, при котором по тем или иным причинам (врожденным или приобретенным) возникают нарушения метаболизма мочевой кислоты.
Источником мочевой кислоты являются пуриновые основания (аденин и гуанин) – составные части нуклеиновых кислот, а также пуриновые нуклеозиды, из которых образованы АТФ и подобные соединения. Метаболизм пуриновых оснований регулируется несколькими ферментами.
Среди больных первичной подагрой, причиной заболевания являются нарушения выведения мочевой кислоты почками.
Выведение уратов через почки включает четыре фазы: фильтрацию в клубочках, реабсорбцию в проксимальных канальцах, секрецию уратов,
37
постсекреторную реабсорбцию. У больных подагрой наблюдаются как изолированные дефекты различных фаз выведения мочевой кислоты (снижение секреции, повышение реабсорбции), так и комбинированных нарушений.
Стойкая многолетняя гиперурикемия является обязательным и главным условием развития подагры, максимальной выраженности достигает уже к 25 годам. Однако средний возраст начала подагры составляет только 47 лет, т.к. для развития первичной подагры, как правило, необходимо сочетание гиперурикемии с такими приобретенными факторами, как употребление в пищу большого количества продуктов, содержащих много пуринов; избыточная масса тела.
Известен афоризм: “Партнерами гиперурикемии являются друзья изобилия”.
Причины развития вторичной подагры обусловлены повышенным образованием уратов, замедлением выведения уратов почками или комбинацией этих нарушений.
Причины повышенного образования мочевой кислоты:
истинная полицитемия, вторичная полицитемия у больных с врожденными “синими” пороками сердца и с хроническими заболеваниями легких;
острые и хронические лейкозы, множественная миелома, лимфомы, карцинома почек и другие злокачественные опухоли;
гиперпаратиреоз;
псориаз (гиперурикемия связана с площадью поражения кожи);
гемоглобинопатии (серповидно-клеточная анемия, талассемия и др.), врожденная гемолитическая анемия, пернициозная анемия и другие мегалобластные анемии;
некоторые врожденные дефекты коагуляции (болезнь Виллебранда);
инфекционный мононуклеоз (гиперурикемия в первые 10 дней);
гипоксемия;
значительная перегрузка скелетных мышц;
избыточное употребление в пищу продуктов, богатых пуринами;
злоупотребление алкогольными напитками;
гликогеноз I, III, V и VII типа.
Причины замедления выведения мочевой кислоты почками:
терминальнаяпочечная недостаточность;
заболевания почек, не сопровождающиеся почечной недостаточностью, характеризующиеся преимущественно интерстициальными (канальцевыми) изменениями (поликистоз почек, анальгетическая нефропатия, гидронефроз);
кетоацидоз; ацидоз, обусловленный избытком молочной кислоты;
прием диуретических средств;
обезвоживание;
38
