
- •Учебно-методическое пособие для самоподготовки и самостоятельной работы студентов по курсу «техническая термодинамика и теплотехника»
- •Тема 1. Основные термодинамические параметры Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Рекомендуемая литература:
- •Определение основных термодинамических Параметров
- •Тема 2. Основные законы идеальных газов Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Краткие теоретические положения по теме:
- •Тема 3. Основные свойства газовых смесей Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Рекомендуемая литература:
- •Краткие теоретические положения по теме:
- •Тема 4. Реальные газы Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Краткие теоретические положения по теме:
- •Тема 5. Первый закон термодинамики Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Техническая термодинамика и теплотехника: учеб.Пособие для вузов/ л.Т. Бахшиева, б.П. Кондауров, а.А. Захаров, в.С. Салтыкова; под ред. А.А. Захаровой. – м.: «Академия», 2006 – с.48 – 52
- •Мазур л.С. Техническая термодинамика и теплотехника: Учебник. – м.: гэотар-мед, 2003. – с.16-18, 28-30
- •Тема 6. Теплоемкость газов
- •Рекомендуемая литература:
- •Тема 7. Основные газовые процессы Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Рекомендуемая литература:
- •Мазур л.С. Техническая термодинамика и теплотехника: Учебник. – м.: гэотар-мед, 2003. – с.18-28
- •Изотермическое сжатие воздуха
- •Экспериментальная часть
- •Обработка результатов измерений
- •Построение уравнения состояния воздуха
- •Тема 8. Теорема карно. Эксергия. Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Рекомендуемая литература:
- •Техническая термодинамика и теплотехника: учеб.Пособие для вузов/ л.Т. Бахшиева, б.П. Кондауров, а.А. Захаров, в.С. Салтыкова; под ред. А.А. Захаровой. – м.: «Академия», 2006 – с.145 -153
- •Мазур л.С. Техническая термодинамика и теплотехника: Учебник. – м.: гэотар-мед, 2003. – с.41-53, 63-66, 155-160 Краткие теоретические положения по теме:
- •Тема 9. Применение термодинамических таблиц и диаграмм для решения инженерных задач Вопросы для самостоятельного изучения:
- •Основные расчетные соотношения, законы, положения по теме:
- •Задачи для самостоятельного решения:
- •Краткие теоретические положения по теме:
- •Средства измерения температуры
- •Общие сведения о температурных шкалах
- •Термометры стеклянные жидкостные
- •Введение поправок к показаниям термометра.
- •Термоэлектрические измерители температуры (термопары)
- •Средства измерения давления
- •Жидкостные манометры
Тема 3. Основные свойства газовых смесей Вопросы для самостоятельного изучения:
-
Понятие «газовая смесь»
-
Парциальное давление. Закон Дальтона для идеальных газов
-
задание газовой смеси объемными и массовыми долями
-
Понятие парциального объема
-
Газовая постоянная смеси газов
-
Молекулярная масса смеси газов
Основные расчетные соотношения, законы, положения по теме:
-
Закон Дальтона:
Рсм
= Р1+Р2+..+Рn=
![]()
-
Массовая доля:
![]() ; w1+w2+…+wn
=
1
; w1+w2+…+wn
=
1
-
Объемная доля:
![]() ;
;
![]()
-
Парциальное давление:
![]()
-
Парциальный объем:
![]() ;
V1+V2+…+Vn=Vсм
;
V1+V2+…+Vn=Vсм
-
Газовая постоянная смеси:
![]()
-
Молекулярная масса смеси:
![]()
Задачи для самостоятельного решения:
-
Генераторный газ имеет следующий объемный состав: CH4 = 25%, CO = 27%, CO2 = 3%, N2=45%. Определить массовые доли, кажущуюся молекулярную массу, газовую постоянную, плотность и парциальные давления при 10 0С и 0,1 МПа.
-
Газовая смесь имеет следующий массовый состав: H2 = 5%, O2 = 15%, CO2 = 10%, N2 = 70%. До какого давления нужно сжать эту смесь, находящуюся при нормальных условиях, чтобы плотность ее составила 1,3 кг/м3?
Рекомендуемая литература:
-
Техническая термодинамика и теплотехника: учеб.пособие для вузов/ Л.Т. Бахшиева, Б.П. Кондауров, А.А. Захаров, В.С. Салтыкова; под ред. А.А. Захаровой. – М.: «Академия», 2006. – С.30 - 34
Краткие теоретические положения по теме:
В технике часто приходится иметь дело с газообразными веществами, близкими по свойствам к идеальным газам и представляющим механическую смесь отдельных газов (например, доменный газ отходящие газы котельных установок). Воздух также представляет собой газовую смесь, состоящую из азота, кислорода, углекислого газа, водяных паров, одноатомных газов. Поэтому для решения практических задач необходимо уметь определять основные параметры газовой смеси.
Под газовой смесью понимается смесь отдельных газов, не вступающих между собой ни в какие химические реакции. Каждый газ в смеси независимо от других газов полностью сохраняет все свои свойства и ведет себя так, как если бы он один занимал весь объем смеси. Молекулы газа создают давление на стенки сосуда, которое называется парциальным (частичным), то есть парциальное давление – это давление, которое имел бы каждый газ, входящий в состав смеси, если бы этот газ находился один в том же количестве, в том же объеме и при той же температуре. Газовая смесь идеальных газов подчиняется закону Дальтона: общее давление смеси газов равно сумме парциальных давлений отдельных газов, составляющих смесь:
![]() ,
,
где Р1, Р2 ,…Р n – парциальные давления.
Массовой долей называется отношение массы каждого газа к общей массе смеси:
![]()
где mn – масса каждого газа;
m – общая масса смеси.
Сумма массовых долей равна единице:
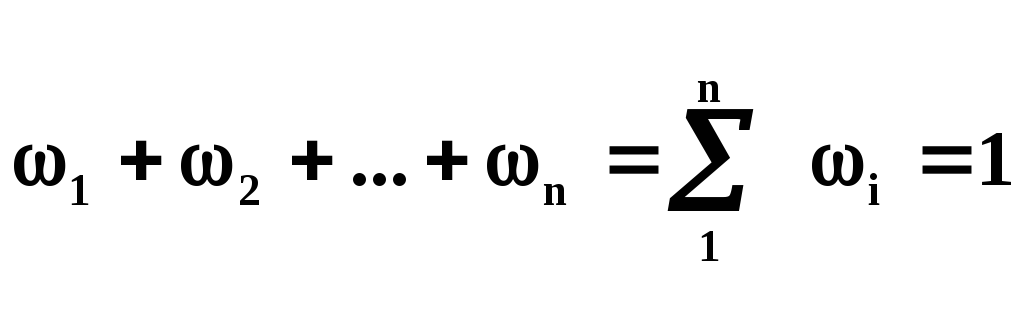
Объемной долей называется отношение парциального (приведенного) объема каждого газа к общему объему смеси газов:
![]()
Сумма объемных долей равна единице:
![]()
Парциальный объем каждого газа можно определить по закону Бойля – Мариотта. При постоянной температуре имеем:
![]() ,
,
причем
![]() ,
,
то есть сумма парциальных объемов газов, составляющих смесь, равна объему смеси газов.
Из записанных выше равенств вытекает:
![]()
Газовая смесь может быть задана массовыми, объемными и молярными долями. Задание смеси молярными долями равнозначно заданию ее объемными долями.
Действительно, из закона Авогадро:
![]() , тогда
, тогда
![]()
Соотношение между массовыми и объемными долями
Между удельными объемами, плотностями, молярными массами и удельными газовыми постоянными какого-либо газа и всей смеси в целом на основании закона Авогадро и уравнения Клайперона – Менделеева существует следующая зависимость:
![]()
можно записать также:
![]() ,
,
где ω – массовая доля;
φ – объемная доля.
![]()
![]()
Газовая постоянная смеси газов
Смесь газов подчиняется уравнению состояния:
![]()
Запишем уравнение состояния для всех компонентов смеси:
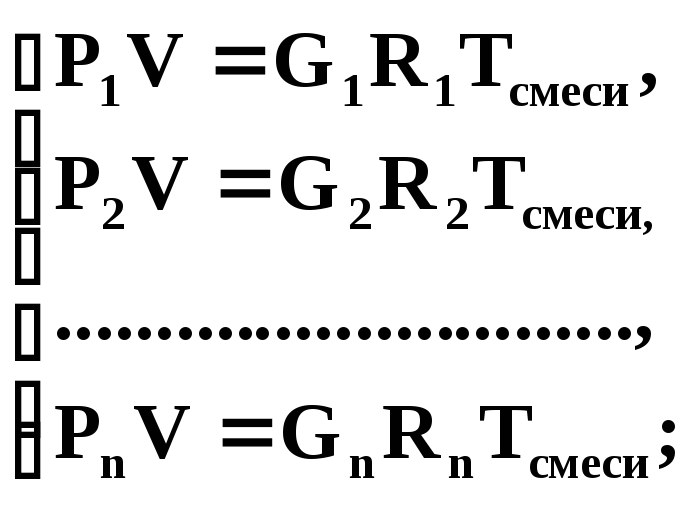
и сложим их
![]()
То есть можно записать:
![]() ,
тогда
,
тогда
![]() ;
;
где
![]() и,
следовательно:
и,
следовательно:
![]()
![]() (если газовая смесь
задается объемными долями)
(если газовая смесь
задается объемными долями)
![]()
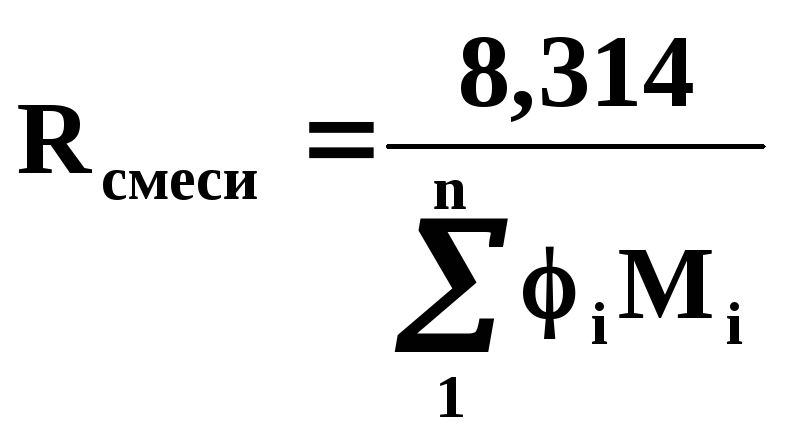
Вывод:
![]() ,
следовательно
,
следовательно
![]()
![]()
поделим это на
![]() :
:
![]()
![]()
