
- •Глава 6 водяной пар и его свойства
- •§6.1. Основные понятия и определения
- •§ 6.2. Термодинамическая фазовая рТ – диаграмма. Уравнение клапейрона - клаузиуса
- •§ 6.6. Основные параметры воды и водяного пара
- •§ 6.7. Процессы изменения состояния водяного пара в pν -,ts - и is -диаграммах
- •§ 6.8. Влажный воздух. Абсолютная влажность, влагосодержание и относительная влажность воздуха
- •§ 6.9. Теплоемкость и энтальпия влажного воздуха
- •Глава 7 термодинамика газового потока
- •§ 7.1. Уравнение энергии газового потока
- •§7.2. Располагаемая работа газового потока
- •§ 7.3. Основные закономерности соплового и диффузорного адиабатного течения газа
- •§ 7.4. Истечение идеального газа из суживающихся сопел
- •§ 7.5 Истечение идеального газа из комбинированного сопла лаваля
- •§ 7.6. Расчет истечения реальных газов и паров
- •7.7 Адиабатное дросселирование
- •§ 7.8. Дроссельный эффект (эффект джоуля-томсона)
- •§ 7.9. Газовые смеси
- •Глава 8 компрессорные машины
- •§ 8.1. Мощность привода и коэффициенты полезного действия компрессора
- •§ 8.2. Многоступенчатый компрессор
- •Глава 9 циклы поршневых двигателей внутреннего сгорания
- •§ 9.1. Краткие исторические сведения
- •§ 9.2. Классификация двс
- •§ 9.3. Циклы двс с подводом теплоты при постоянном объёме
- •§9.4. Циклы двс с подводом теплоты при постоянном давлении
- •§ 9.5. Циклы двс со смешанным подводом теплоты
- •Глава 10 циклы газотурбинных установок и реактивных двигателей
- •§ 10.1. Циклы гту с подводом теплоты при постоянном давлении
- •§10.2. Циклы гту с подводом теплоты при постоянном объеме
- •§ 10.3. Методы повышения термического кпд гту
- •§ 10.4. Циклы реактивных двигателей. Жидкостные реактивные двигатели
- •10.5. Воздушно-реактивные двигатели
- •§ 10.6. Пульсирующий воздушно-реактивный двигатель
- •§ 10.7. Компрессорные воздушно-реактивные двигатели
- •§ 10.8. Термодинамические методы сравнения циклов тепловых двигателей
- •Глава 11 циклы паросиловых установок мгд-генератор
- •§ 11.1. Цикл карно во влажном паре и его недостатки
- •§ 11.2. Основной цикл псу-цикл ренкина
- •§ 11.3. Полезная работа цикла ренкина. Работа питательного насоса
- •§ 11.4. Термический кпд цикла ренкина
- •§ 11.5. Влияние параметров пара на термический кпд цикла ренкина
- •§ 11.6. Промежуточный перегрев пара
- •§ 11.7. Регенеративный цикл паросиловой установки
- •§ 11.8. Бинарные (двойные) циклы
- •§ 11.9. Циклы парогазовых установок
- •§ 11.10. Циклы атомных электростанций
- •§ 11.11. Циклы электрических станций с магнитогидродинамическими генераторами
- •Глава 12 циклы холодильных машин
- •§12.1. Цикл воздушной холодильной установки
- •§ 12.2. Цикл паровой компрессорной холодильной установки
- •§ 12.3. Цикл холодильной установки абсорбционного типа
- •§ 12.4. Цикл пароэжекторной холодильной установки
- •§ 12.5. Тепловой насос
- •§ 12.6. Вихревая труба
- •§ 12.7. Термотрансформаторы
- •Глава 13 элементы химической термодинамики
- •§ 13.1. Классификация химических реакций
- •§13.2. Первый закон термодинамики в применении к химическим реакциям
- •§ 13.3. Тепловой эффект реакции
- •§ 13.4. Теплоты химических реакций
- •§ 13.5. Закон гесса
- •§13.6..Закон кирхгофа
- •§ 13.7. Применение второго закона термодинамики к химическим процессам
- •§ 13.8. Изохорно-изотермический и изобарно-изотермический потенциалы
- •§13.9. Максимальная работа реакции
- •§ 13.10. Уравнения максимальной работы (уравнения гиббса-гельмгольца)
- •13.11. Химический потенциал
- •§ 13.12. Условия равновесия в изолированных однородных (гомогенных) системах
- •§ 13.13. Условия равновесия в изолированных неоднородных (гетерогенных) системах и химических реакциях
- •§13.14. Равновесие в химических реакциях
- •§ 13.15. Закон действующих масс. Константы равновесия химических реакций
- •§ 13.16. Термическая диссоциация. Степень диссоциации
- •§ 13.17. Зависимость между константой равновесия и степенью диссоциации
- •§ 13.18. Зависимость между константой равновесия и максимальной работой. Уравнение изотермы химической реакции
- •§ 13.19. Влияние температуры реакции на химическое равновесие. Принцип ле-шателье
- •§ 13.20, Тепловая теорема нернста. Третье начало термодинамики
- •§ 13.21. Третье начало термодинамики в формулировке планка (постулат планка)
§ 13.17. Зависимость между константой равновесия и степенью диссоциации
Рассмотрим реакцию горения водорода, сопровождающуюся уменьшением числа молей
2
 Н20+02
2Н20.
Н20+02
2Н20.
Состав продуктов сгорания к моменту равновесия будет следующий: 2α молей водорода, а молей кислорода и 2(1-α) молей водяного пара. Используя известные формулы газовых смесей, находим парциальные давления компонентов
![]() ;
; ![]() ;
; ![]() .
.
Отсюда по формуле (13.44) находим
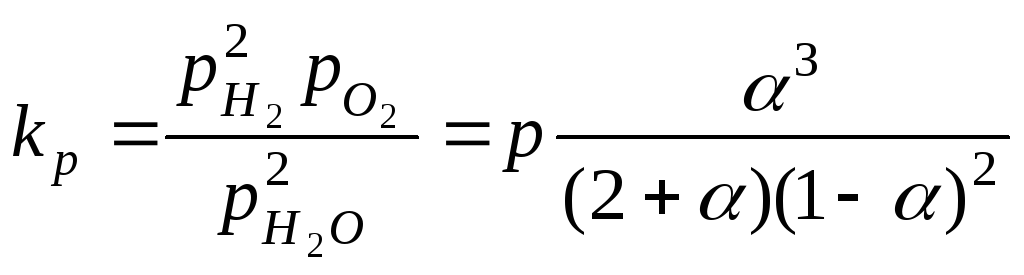 .
.
Из последней формулы следует, что степень диссоциации определяется давлением, при котором происходит диссоциация. Анализ формул зависимостей константы равновесия и степени диссоциации позволяет заключить, что константа равновесия представляет более удобную расчетную величину, чем степень диссоциации. Поэтому при расчетах состава продуктов сгорания обычно используют константу равновесия и для нее приводятся зависимости от температуры для различных реакций.
§ 13.18. Зависимость между константой равновесия и максимальной работой. Уравнение изотермы химической реакции
Скорость
и полнота химической реакции определяются
химическим сродством
реагирующих веществ. Степень химического
сродства зависит от величины
максимальной работы, которая для
изохорно-изотермической реакции
определяется разностью изохорных
потенциалов
![]() ,
а для
изобарно-изотермической
- разностью изобарных потенциалов
,
а для
изобарно-изотермической
- разностью изобарных потенциалов
![]() .
Чем
.
Чем
большее значение имеет максимальная работа реакции, тем больше химическое сродство реагентов. Тем полнее в этом случае проходит реакция и тем меньше остается к моменту равновесия исходных веществ и тем больше продуктов реакции.
Из анализа формулы (13.44) можно заключить, что константа равновесия с увеличением полноты реакции уменьшается. Отсюда следует, что константа равновесия связана с максимальной работой определенной зависимостью.
Уравнение, связывающее две эти величины, называется уравнением изотермы химической реакции.
Для вывода этого уравнения рассмотрим обратимую реакцию вида
a
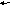 A+bB
cC+dD.
A+bB
cC+dD.
В
состоянии равновесия парциальные
давления делаются равновесными и равными
![]() Изменение
изобарно-изотермического потенциала
находится
по формуле (13.42). Подставляя в эту формулу
значения химических
потенциалов, определяемых уравнением
(13.40), получим
Изменение
изобарно-изотермического потенциала
находится
по формуле (13.42). Подставляя в эту формулу
значения химических
потенциалов, определяемых уравнением
(13.40), получим
![]() .
.
Учитывая (13.43), найдем
![]() . (13.46)
. (13.46)
Полученное уравнение называется уравнением изотермы химической реакции. Его вывод как для изобарно-изотермических, так и для изохорно-изотермических реакций одинаков. Анализ этого уравнения позволяет сделать следующие выводы:
1.
Если
![]() ,
то система находится в равновесии.
,
то система находится в равновесии.
2. Если
![]() ,
то
,
то
![]() .
Реакция в
данном случае
.
Реакция в
данном случае
может идти только слева направо, т.е. с образованием веществ С и D.
3.
Если
![]() ,
то реакция может идти только справа
налево, т.е. с образованием
веществ A
и В.
,
то реакция может идти только справа
налево, т.е. с образованием
веществ A
и В.
Уравнению изотермы химической реакции можно придать более простой вид, если отношение парциальных давлений принять равным единице, т.е.
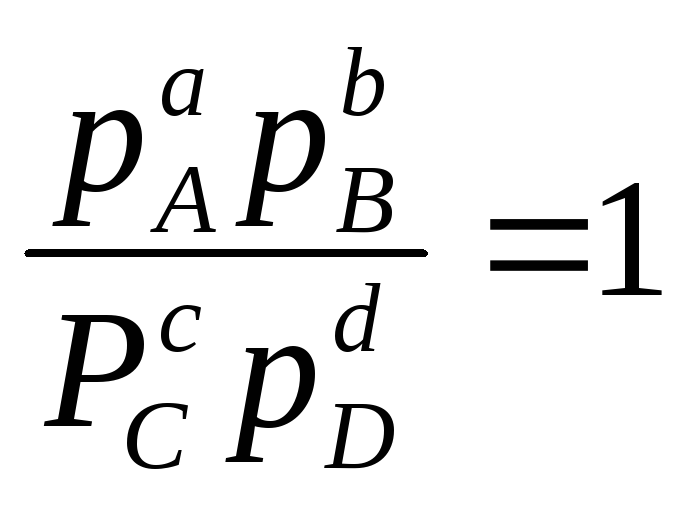
Тогда из (13.46) следует
![]() . (13.47)
. (13.47)
Или, учитывая, что R =8,3143 кДж/(моль.К) и переходя к десятичным логарифмам, получим
![]() . (13.48)
. (13.48)
