
- •Херсонский национальный технический университет к афедра экологии и бжд
- •1. Цель работы
- •2. Экспериментальная часть
- •2.1. Описание лабораторной установки
- •2.2 Порядок проведения работы на установке
- •3. Обработка результатов исследования
- •3.1. Определение содержания аммиака в аммиачно-воздушной смеси.
- •3.2. Определение содержания аммиака в промывной воде
- •3.3. Определение степени абсорбции аммиака
- •3.4. Определение движущей силы абсорбции
- •3.5. Определение коэффициента массопередачи
- •3.6. Определение коэффициента диффузии аммиака в газе
- •3.7. Определение коэффициента полезного действия полки
- •3.8. Материальный баланс установки
- •5. Техника безопасности
3. Обработка результатов исследования
3.1. Определение содержания аммиака в аммиачно-воздушной смеси.
Принцип метода. При отборе пробы аммиачно-воздушной смеси в эвакуационную колбу с водой аммиак поглощается с образованием гидроокиси аммония, содержание которой определяют титрованием полученного раствора серной кислотой:
NH3 + H2O = NH4OH
2NH4OH + H2SO4 = (NH4)2 SO4 + 2H2O
Реактивы:
Серная кислота 0,1 раствор;
Метиловый красный индикатор
Ход определения. В круглодонную колбу емкостью около 500 мл с пришлифованной пробкой-краном наливают 50 мл дистиллированной воды, приливают 2-3 капли метилового спирта и эвакуируют колбу при помощи водоструйного или масляного насоса до остаточного давления 50-60 мм рт.ст. После этого колбу проверяют на герметичность, опрокидывая ее краном вниз; при этом не должно наблюдаться проскакивание пузырьков через жидкость. Колбу тщательно вытирают, взвешивают на аналитических весах и присоединяют ее водную трубку к газообразной трубке. Пробу газа отбирают в течении 1-2 мин. После отбора пробы колбу вытирают, вторично взвешивают и встряхивают 5 мин для полного поглощения аммиака водой. Вынимают пробку и ополаскивают ее водой.
Расчет. Содержание аммиака в аммиачно-воздушной смеси (x) в весовых процентах рассчитывают по формуле:
![]() (1)
(1)
или в объемных процентах (y):
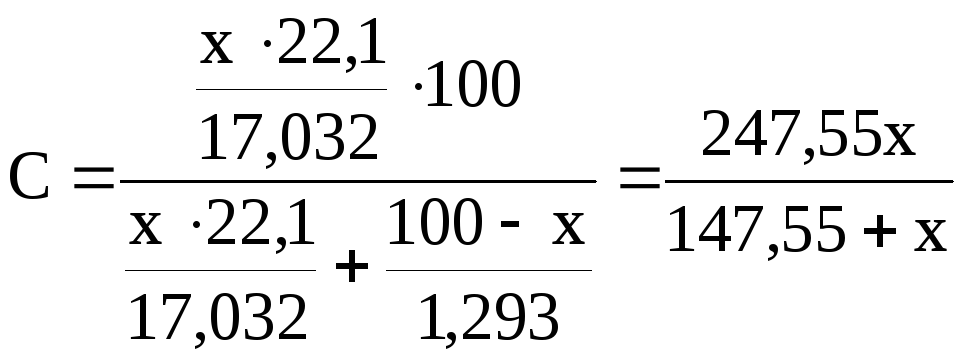 ,
(2)
,
(2)
где a- объем 0.1 н раствора H2SO4 израсходованного на титрование, мл;
К - поправочный коэффициент для приведения концентрации раствора H2SO4 к точно 0.1 н;
0,0017- количество NH3 соответствующее 1 мл 0,1 н раствора;
q- вес пробы аммиачно-воздушной смеси, г;
22,1- объем грамм-молекулы NH3 при нормальных условиях, л;
17,032- молекулярный вес NH3;
1,293- все одного литра воздуха при нормальных условиях, г.
Результаты анализа заносим в таблицу 2
Таблица 2
Результаты анализ аммиачно-воздушной смеси
|
№ |
Наименование измерения |
Вход |
Выход |
|
1 |
2 |
3 |
4 |
|
1 |
Вес колбы после откачки из нее воздуха, г; |
|
|
|
2 |
Вес колбы после взятия анализа, г; |
|
|
|
3 |
Вес аммиачно-воздушной смеси |
|
|
|
4 |
Количество 0,1 н H2SO4, пошедшей на титрование, мл; |
|
|
|
5 |
Концентрация аммиака в весовых % объёмных % |
|
|
3.2. Определение содержания аммиака в промывной воде
Содержание аммиака в промывной воде определяют третированием ее серной кислотой.
Титрометрический метод
Реактивы: Серная кислота 0,1 н раствор;
метиловый красный индикатор
Ход определения:
10 мл исследуемого раствора переносят в коническую колбу, добавляют 2 капли метилового красного и титруют 0,1 н раствором серной кислоты до перехода желтой окраски в розовую.
Расчет:
Содержание аммиака в г/л рассчитывают по формуле:
![]() ,
(3)
,
(3)
где a- объем 0.1 н раствора H2SO4 израсходованного на титрование, мл;
К- поправочный коэффициент для приведения концентрации раствора H2SO4 к точно 0.1 н;
V – объем исследуемого раствора, взятого для титрования, мл;
0,0017- количество NH3 соответствующее 1 мл 0,1 н раствора;
