
- •(Для студентов нехимических специальностей)
- •4) Валентных электронов
- •3) Уменьшается
- •1) Ковалентные полярные
- •1) Ковалентная полярная
- •Кислород
- •Увеличивается
- •Не изменяется
- •Уменьшается
- •Горении природного газа
- •1) Хрома (III) 2) хрома (II) 3) хрома (VI) 4) магния
- •Горение железа в хлоре
- •1) Стеклянный (ионселективный) 2) газовый 3) хлорсеребряный
- •3) Рентгенографии 4) хроматографии
- •3) Эмиссией
- •2) Радиоактивным
- •2) Фиолетовый
- •Энергией активации
- •1) Увеличится в 6 раз 2) уменьшится в 4 раза
- •3) Уменьшится в 2 раза 4) увеличится в 8 раз
- •4) Понизить температуру
- •1) Изотоническими
- •2) Уменьшается
- •3) Не изменяется
- •4) Увеличивается
- •Солей высших карбоновых кислот
- •Полимеризации
- •Кратные связи
- •1) Меньшей молекулярной массой
4) Понизить температуру
Общие свойства растворов
-
Осмотическое давление 0,15 м раствора глицерина при 250 равно …мПа
-
Осмотическое давление раствора этанола с молярной концентрацией 0,5 моль/л при 20 0С равно ….кПа
-
609
-
1217
-
2435
-
4970
-
Раствор, содержащий 11,6 г вещества в 400 г воды замерзает при температуре -0,940С. Криоскопическая константа для воды равна
КН2О
= 1,86
![]() .
Молярная масса растворенного вещества
равна…
.
Молярная масса растворенного вещества
равна…
г/моль.
1) 29 2) 58 3) 116 4) 87
-
Растворы, имеющие одинаковую величину осмотического давления называются
1) Изотоническими
2) изотермическими
3) гипотоническими
4) гипертоническими
-
Концентрация раствора глюкозы, кипящего при 100,78 0С
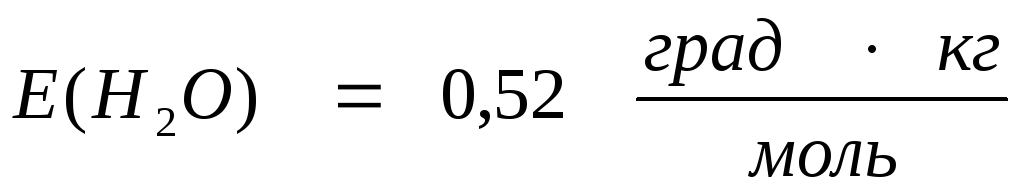 равна ….. моль/ кг
равна ….. моль/ кг
-
0,3
-
1,5
-
0,5
-
1
Окислительно-восстановительные реакции
-
Восстановителем в реакции
Fe +
HNO3(конц)
![]() Fe(NO3)3
+ NO2+
H2O
Fe(NO3)3
+ NO2+
H2O
является…
-
азотная кислота
-
железо
-
вода
-
оксид азота (IV)
-
Коэффициент перед молекулой восстановителя в уравнении реакции
KMnO4 + Na2SO3 + H2SO4 → MnSO4 + Na2SO4 + K2SO4 +H2O
равен…
1) 2 2) 3 3) 1 4) 5
-
Коэффициент перед молекулой восстановителя в уравнении реакции
KNO2 + H2SO4 + KJ → K2SO4 + NO + J2 +H2O
равен…
1) 1 2) 4 3) 3 4) 2
-
Сера проявляет окислительные свойства в реакции
1) S + O2 →
2) S + Fe →
3) S + HNO3 →
4) S + Cl2 →
-
Окислительные свойства оксида серы (IV) проявляются в реакции …
1) SO2 + H2S →
2) SO2 + KMnO4 + H2O →
3) SO2 + Ca(OH)2 →
4) SO2 + O2 →
-
Пропущенными веществами в системе химической реакции
Cl2 + … → KClO3 + … + H2O являются …
1) KH 2) KOCl 3) KOH 4) KCl
-
При разложении нитрата серебра образуются….
1) Ag +NO2 + O2→
2) Ag2O + N2O5 →
3) Ag + N2O3+O2 →
4) Ag2O + N2O5 O2→
-
Среди галогенов наиболее сильным окислителем является…
-
иод 2) фтор 3) бром 4) хлор
-
Формулы веществ, пропущенные в схеме химической реакции
Pb(NO3)2
![]() …
+NO2
+
…
…
+NO2
+
…
имеют вид…
1) N2 2) Pb 3) O2 4) PbO
-
Формулы веществ, пропущенные в схеме химической реакции
Al + …
![]() …
+
NH4NO3+
H2O…
…
+
NH4NO3+
H2O…
имеют вид…
1) Al2O3 2) Al(NO3)3 3) NO 4) H2O
-
Для защиты железных изделий от коррозии в качестве катодного покрытия используется…
1) олово
2) магний
3) бериллий
4) алюминий
81. При нарушении оловянного покрытия на железном изделии в кислоте на аноде будет протекать процесс
1) Fe0 – 2e → Fe+2
2) Sn0 – 2e → Sn+2
3) 2H+ – 2e → H20
4) Sn+2 + 2e → Sn0
Электролиз
-
Продуктами, выделяющимися на инертных электродах при электролизе водного раствора сульфата меди, являются…
1) Cu и Н2 2) H2 и O2 3) Cu и О2 4) Cu и H2S
-
Продуктами, выделяющимися на инертных электродах при электролизе водного раствора хлорида калия, являются…
1) Н2 и O2 2) К и Cl2 3) K и О2 4) Н2 и Cl2
-
Уравнение процесса, протекающего на катоде при электролизе водного раствора бромида меди, имеет вид …
-
Cu2+ + 2e = Сu0
-
2Br - - 2e = Br20
-
2H2O +2e = H2+ 2 OH-
-
2H+ + 2e = H2
ПАВ
-
При растворении в воде поверхностно-активного вещества величина поверхностного натяжения ...
1) сначала увеличится, а затем уменьшается
