
KMSF-Chast2-new
.pdf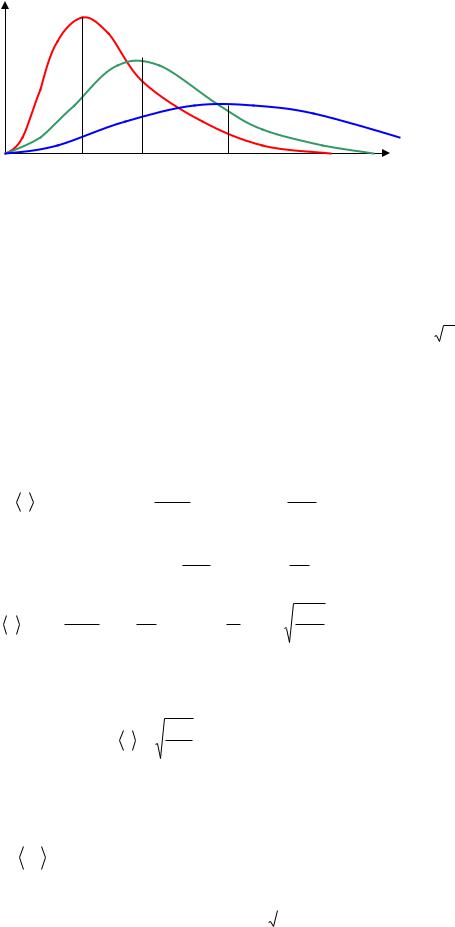
f(v)
T1 |
T1 < T2 < T3 |
T2
T3
v
Рис.2.3. Распределение Максвелла при разных температурах.
С ростом температуры диапазон скоростей все расширяется, а наиболее ве-
роятная скорость сдвигается в область больших
скоростей (
v |
вер |
|
~ |
T |
), при
этом наиболее вероятной скоростью обладают все меньшее число молекул(максимум становится меньше).
Характерные средние скорости:
1) Средняя скорость. По определению
|
|
|
v v dv 4 |
|
m |
|
3 / 2 |
|
|
|
mv |
2 |
|
|
|
|
|
|
3 |
|
|||||||
v |
|
|
|
v |
|
|
|
|
|
||||
|
2 kT |
|
|
exp |
|
|
dv |
||||||
|
|
0 |
|
0 |
|
|
|
2kT |
|||||
.
(2.25)
Произведем замену переменных:
ymv 2 2kT
и
vdv
kT m
dy
.
|
|
m |
|
3 / 2 |
|
||
v |
|
|
|
||||
4 |
|
|
|
|
|
||
|
2 kT |
|
|
0 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
e |
y |
ydy |
|
|||
|
|
||||||
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
v |
2T |
y exp y |
T |
dv 4 |
kT |
||||||||
m |
m |
2 m |
||||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
ye |
y |
|
e |
y |
dy e |
y |
1 |
|||||
|
|
|
||||||||||
|
|
0 |
|
|
0 |
|||||||
|
|
|
|
0 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||
|
8kT |
; |
|
|
|
|
|
|
||||
|
m |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
e |
y |
ydy. |
|
||
0 |
|
|
. |
|
|
(2.26)
2)Средняя квадратичная скорость. По определению, среднее значение квадрата скорости
|
|
|
|
|
|
|
m |
3 / 2 |
|
|
|
|
|
|
mv2 |
|
|
||
|
2 |
|
2 |
|
|
|
|
4 |
|
|
|
|
|
|
|||||
v |
|
v |
|
v dv 4 |
|
|
|
|
v |
|
|
e |
|
2kT |
dv |
(2.27) |
|||
|
|
|
|
|
|
|
|
||||||||||||
|
|
0 |
|
|
2 kT |
|
0 |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
x4 e x2 dx |
d |
|
e x2 dx |
|
3 |
|
|
|
|
||||||||
|
|
|
|
5 / 2 |
|
||||||||||||||
|
|
d |
2 |
|
8 |
|
|
|
|||||||||||
|
|
0 |
|
|
|
0 |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
31 |
|
|
|
|
|
|
|
|
|
|
|
|
В нашем случае |
|
|
m |
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
2kT |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
m |
|
3 / 2 |
3 |
|
2kT |
5 / 2 |
|
3kT |
|
|
|
v |
2 |
|
|
|
||||||||
|
|
|
4 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
2 kT |
|
8 |
|
m |
|
|
|
m |
|
И средняя квадратичная скорость равна
(2.28)
v |
|
|
v |
2 |
|
3kT |
|
|
|
|
|
|
|
|
ср.кв. |
|
|
|
|
m |
|
|
|
|
|
|
.
(2.29)
Отсюда можно получить среднюю кинетическую энергию, приходящуюся на молекулу:
K |
|
m |
v |
2 |
|
3 |
kT |
|
|
||||||
2 |
|
2 |
|||||
|
|
|
|
|
|
||
|
|
|
|
|
(2.30) |
||
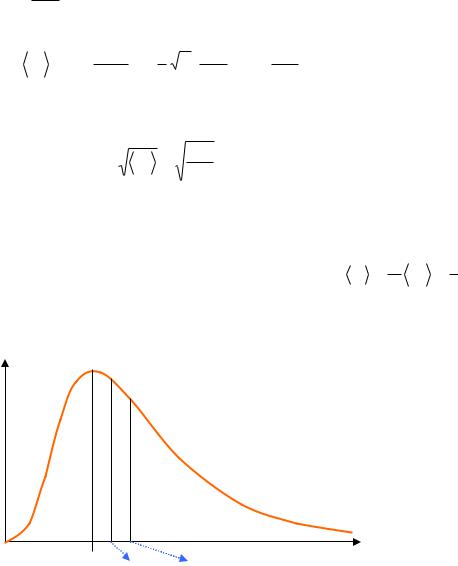
(v)
vвер |
vср |
v |
|
vср.кв. |
Рис.2.4. Характерные скорости распределения Максвелла.
На графике функции распределения v все характерные скорости расположены следующим образом:
vвер vср vср.кв. .
Из Рис.2.4. видно, что максимум функции распределения довольно широк. Это отражает большой разброс в абсолютных значениях скоростей молекулы, т.е. большие флуктуации её скорости. Одна молекула - подсистема, которая содержит малое число частиц, поэтому флуктуации велики;
3) Для подсистемы с N частицами её полная кинетическая энергия
32

|
|
|
|
|
|
|
|
|
mv |
2 |
|
mv |
|
|
K |
|
K |
|
K |
|
... |
|
|
||
K |
|
|
|
|
1 |
|
||||||
c |
1 |
2 |
3 |
2 |
|
2 |
||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||
2 2
|
mv |
|
2 |
||
|
2 3
...
Из этих N частиц доля молекул, имеющих скорости от от v до v + dv, в силу независимости будет равна
|
|
|
3 / 2 |
|
|
mv |
2 |
|
|
|
N |
|
m |
|
|
|
|
|
|
|
|
||
|
e |
|
|
|
4 v |
2 |
dv |
|
|||
dP K |
|
|
|
|
2kT |
|
|
||||
|
|
|
|
|
|
|
|
|
|
||
|
2kT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2.31)
Эта вероятность имеет очень резкий максимум как функция скорости v, при |
||||||||||
этом функция распределения по скоростям в системе |
dP K |
|
v . При |
|||||||
|
dv |
|
||||||||
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
mv |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
больших скоростях эта вероятность быстро спадает |
|
N |
|
|
|
, а при ма- |
||||
~ exp |
|
|
|
|||||||
|
|
|
|
|
|
2kT |
|
|||
|
|
|
|
|
|
|
|
|||
лых ведет себя как |
|
|
|
|
|
k |
|
|||
~ v |
2 N |
, таким образом в распределении получаем резкий |
||||||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
максимум.
dP Kdv N
N частиц
1 частица
v
Рис.2.5. Распределение Максвелла для N частиц.
Распределение Максвелла по проекциям скорости.
Когда проводится экспериментальная проверка распределения Максвелла, то регистрируются молекулы, летящие в одну сторону. Чтобы получить функцию распределения молекул по проекциям скорости перепишем распределение Максвелла в виде
33

|
m |
|
dP K |
|
|
|
2 kT |
|
3 / 2 |
|
2 |
2 |
2 |
) |
|
|
|
|
m(v |
v |
v |
|
|
|
||
|
|
x |
y |
z |
|
|
|
|
|
|
|
|
dv dv dv |
|
|||
|
e |
|
2kT |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x |
y |
z |
(2.32)
Эту вероятность |
|
||
dP K dP v |
dP v |
dP v |
z |
x |
y |
|
|
можно |
представить |
в |
виде |
произведения |
, где каждый из сомножителей представляет собой |
||||
распределение Максвелла для проекций скорости молекул. Очевидно,
|
|
1 / 2 |
|
|
mv |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
dP vx |
|
|
e |
|
x |
dvx . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 / 2 |
|
|
mv |
2 |
|
dP v |
|
|
|
|
|
|
|
|
|
m |
|
|
x |
|
|
||||||
Легко увидеть, что плотность вероятности |
vx |
|
|
|
e |
|
|
|
|
|
|
|||||||
|
|
|
2T |
|
|
x |
||||||||||||
|
|
|
|
|
|
|
|
2 T |
|
|
|
|
|
|
dv |
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
что
(2.33)
|
сим- |
|
метрично относительно начала координат и имеет максимум при vx = 0. Положительные и отрицательные значения vx имеют одинаковую вероятность, поэтому наиболее вероятная проекция и средняя проекция скорости равны нулю  vx
vx  0. Можно пояснить на простых картинках фазового объема разли-
0. Можно пояснить на простых картинках фазового объема разли-
чие в распределениях по абсолютным значениям скорости и по их проекциям, а также, почему наиболее вероятная проекция скорости равна нулю. Плотность числа точек наибольшая в центре системы координат скоростей, а
|
|
|
mv |
2 |
|
|
|
E K Ae |
|
|
|
||
затем падает по экспоненте - |
2T |
. Для абсолютных значений |
||||
|
||||||
|
|
|
|
|||
скорости фазовый объем растет с увеличением абсолютного значения скорости пропорционально ~ 4 v2dv. Поэтому при малых скоростях распределение растет из-за фазового объема, достигает максимума и затем падает из-за быстрого падения плотности частиц (хотя фазовый объем по-прежнему растет).
Если рассматривать фазовый объем в распределении по проекциям скорости, то этот фазовый объем постоянен для всех значений vx, и равен dvx. Следовательно, вероятность больше там, где больше плотность частиц.
Вычислим среднюю энергию, приходящуюся на одну степень свободы, т.е.
сосчитаем |
Ex |
- долю кинетической энергии, относящуюся к движению по |
оси x. По определению
Так как exp
|
|
m |
1 / 2 |
|
|
|
|
2 |
|
|
|
|
|
m |
|
|
|
mvx |
|
2 |
|||
Ex |
|
|
|
|
|
exp |
|
|
vx dvx . |
||
|
|
|
|
||||||||
|
|
2 kT |
|
2 |
|
|
|
2kT |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
x2 x2 dx |
d |
exp x2 |
dx |
d |
|
|
|
|
|
|
|
||
|
|
|
2 |
, то |
|||||||||
d |
d |
|
|
2 |
|
||||||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ex |
|
1 |
kT . |
(2.34) |
|
2 |
|||||
|
|
|
|
34

Итак, кинетическая энергия, приходящаяся на одну степень свободы, равна
“половинке” kT, причем
E |
|
|
E |
|
|
E |
|
|
1 |
kT . |
x |
y |
z |
2 |
|||||||
|
|
|
|
|
|
|
|
|
|
Тогда среднее значение пол-
ной энергии равно
E |
3 |
kT . |
(2.35) |
|
2 |
||||
|
|
|
§2.3. Распределение Больцмана и его свойства.
В начале |
настоящей главы мы писали для классической подсистемы |
E K U , |
и поскольку кинетическая энергия есть функция скоростей, а по- |
тенциальная энергия - функция координат, то вероятность для подсистемы иметь энергию Е равна dP E dP K dP U . В силу независимости событий (произведение вероятностей) иметь определенные значения кинетической и потенциальной энергий можно рассматривать отдельно вероятность распределения частиц во внешнем поле U x, y,z
dP U Be |
|
U x, y,z |
|
|
kT |
dxdydz, |
|||
|
||||
|
|
|
(2.36)
Так как |
dP U |
формулой
dP x, y, z
dN x, y, z N B
dN |
, то число молекул в объеме |
dV |
определяется |
|||
N |
||||||
|
U x, y, z |
|
|
|||
|
|
|
|
|||
exp |
|
dxdydz. Смысл множителя NB легко |
||||
|
||||||
|
|
kT |
|
|
||
понять, если рассмотреть число частиц в единице объема, т.е. плотность
|
|
dNx, y,z |
|
|
N Be |
|
U x, y,z |
|
|
||||||
(концентрацию) числа частиц |
|
|
|
. |
Очевидно, что |
||||||||||
dxdydz n x, y, z |
|
|
kT |
||||||||||||
|
|
|
|
|
|
|
|
||||||||
произведение NB равно плотности числа частиц 0 в точке, где U = 0. Тогда |
|||||||||||||||
n x, y, z n0 e |
|
U x, y, z |
|
|
|
|
|
|
|
|
|
||||
kT |
. |
|
|
|
|
|
|
(2.37) |
|||||||
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Эта формула носит название распределения Больцмана. |
|
|
|
||||||||||||
Если отсчет вести от точки, |
где U U 0 , |
то распределение Больцмана прини- |
|||||||||||||
мает вид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
n x, y, z n0 |
|
|
U x, y, z U 0 |
|
|
|
|
|
|
|
|||||
exp |
|
|
|
|
|
|
. |
|
|
|
|
|
(2.38) |
||
|
|
kT |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
Примеры использования распределения Больцмана:
1) Распределение частиц в сосуде по высоте в однородном поле тяжести
( g const , T const ). Для Земли поле тяжести однородно для небольших высот h << R3 (R3 - радиус Земли):
35
|
U r |
Mm |
|
Mm |
|
Mm |
|
Mm |
h |
, |
||||||
|
r |
R h |
R |
R |
2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
U h U 0 |
Mm |
h mgh . |
|
|
|
h |
||||||||
|
|
R |
2 |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Получаем |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
mgh |
|
|
|
mgh |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
gh |
|
|
|
||||||
n h n 0 exp |
|
n 0 exp |
|
|
n 0 exp |
|
. |
|
|
|||||||
|
kT |
|
|
|
kT |
|
|
|
|
|
RT |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
mg
Здесь - молярная масса газа, R - универсальная газовая постоянная. Воспользовавшись связью между концентрацией и давлением, получаем барометрическую формулу Больцмана
|
|
|
|
|
|
|
p p |
|
exp |
|
|
mgh |
|
0 |
|
kT |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2.39)
Концентрация частиц убывает с высотой, причем концентрация более тяжелых частиц убывает с высотой быстрее. Это создает подъемную силу для более легких объектов (воздушные шары). Для более высоких температур распределение с высотой становится более равномерным. При этом полное чис-
ло частиц сосуде N постоянно и равно
L |
|
|
|
S n0 |
exp |
0 |
|
mgh |
||
kT |
dh N |
|
|
||
k |
||
. Здесь S
площадь сечения сосуда, а L его полная высота;
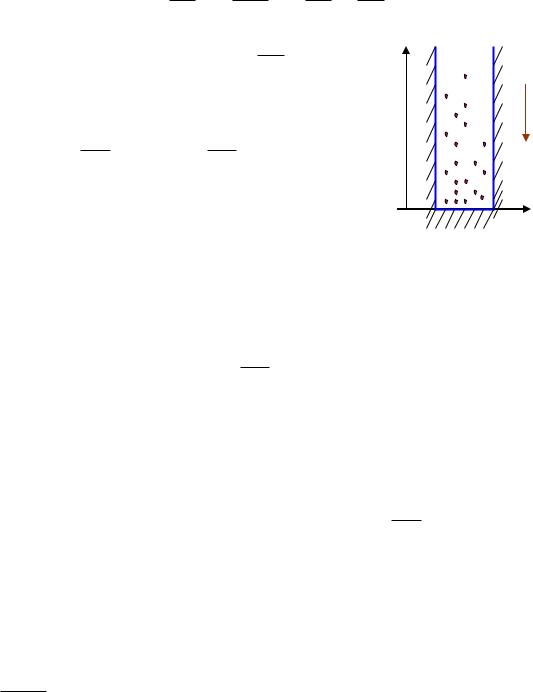
2) Распределение частиц во вращающемся сосуде. Имеем сосуд длины L,
который вращается с угловой скоростью вокруг одного из его оснований. Сила инерции, действующая на молекулу, находящуюся на расстоянии r от
основания, равна |
F m |
2 |
r |
, а потенциальная энергия молекулы равна |
|
m |
r |
|
U r |
2 |
|
2 |
2 |
|
|
|
|
|
|
. |
Распределение |
частиц |
описывается |
функцией |
n r n0 |
m 2 r 2 |
|
,которая показывает, что концентрация молекул растет с |
||
exp |
|
|
|||
2kT |
|||||
|
|
|
|
||
радиусом и достигает максимального значения у противоположного основания;
3) Средняя энергия, приходящаяся на колебательную степень свободы.
Распределение Максвелла-Больцмана (Гиббса) позволяет получить среднюю энергию, приходящуюся на колебательную степень свободы. Этим мы подтвердим теорему о равнораспределении энергии по степеням свободы и по-
36

лучим теплоемкость твердых тел при высоких температурах T (для которых применимо классическое описание).
Равновесное состояние кристалла - периодическое расположение атомов в пространстве. Однако, атомы не находятся в покое, а совершают малые тепловые колебания относительно положений равновесия. Пусть колебания совершаются вдоль оси 0x, тогда энергия такого осциллятора равна:
E |
mv 2 |
|
x |
2 |
|
x |
|
|
(2.40) |
||
2 |
2 |
|
|||
|
|
|
|
где m масса атома, упругая постоянная. Статистическое описание атомов с энергией Е можно вести с помощью распределения Максвелла-Больцмана, которое для одного осциллятора имеет вид
|
|
mv |
2 |
|
|
|
x |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
dP Aexp |
|
|
x |
exp |
|
|
|
dv |
dx |
||
|
|
|
|
||||||||
|
|
2T |
|
|
|
2T |
|
x |
|
||
|
|
|
|
|
|
|
|
||||
.
(2.41)
Во избежание путаницы здесь и далее вместо kT в знаменателе стоит T. Нормировочная постоянная A состоит из произведения двух постоянных (А = А1А2 ), которые равны соответственно:
|
|
m |
|
1 / 2 |
|
, |
|||
A |
|
|
||
1 |
|
2 T |
|
|
|
|
|||
A |
|
|
|
|
|
2 |
|
2 T |
|
|
1 / 2 |
|
|
|
|
|
|
.
(2.42)
Найдем стандартным образом среднюю энергию тела, колеблющегося вдоль оси x:
|
|
|
|
|
mv 2 |
x 2 |
|
|
|
|
|
|
|
|
mv 2 |
x 2 |
|
|
||||||||||
E |
|
A A |
|
|
x |
|
|
|
|
exp |
|
|
|
|
x |
|
|
dv |
dx |
|||||||||
x |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
1 2 |
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
x |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
m |
|
|
|
|
|
|
mv 2 |
|
|
|
|
|
|
|
|
|
x 2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
A A |
|
|
v 2 |
exp |
|
|
|
|
dv |
x |
|
|
|
|
exp |
|
dx |
|||||||||||
|
|
1 |
2 |
2 |
|
|
x |
|
|
|
2T |
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
mv 2 |
|
|
|
|
|
|
|
|
|
|
|
x 2 |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
A A |
|
|
exp |
|
|
dv |
x |
|
|
|
x 2 |
|
exp |
|
dx. |
||||||||||||
|
|
1 |
2 |
2 |
|
|
2T |
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Второй интеграл в первом слагаемом есть по сути нормировочный интеграл и равен (А2)-1. То же относится к первому интегралу во втором слагаемом, который равен (А1)-1. Другие интегралы равны:
|
|
|
|
|
|
|
|
mvx2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
32 |
|
|
|
|
|
|
|
|
|
|
x 2 |
|
|
|
|
|
|
|
|
32 |
|
|
|||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
2T |
|
|
||||||||||||||||||||
|
v |
|
exp |
|
|
|
|
dv |
|
|
|
|
|
|
|
|
|
|
|
, |
|
|
|
|
x |
|
exp |
|
|
|
|
dx |
|
|
|
|
|
|
|
. |
(2.43) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
x |
|
|
|
|
|
2T |
|
|
|
|
x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2T |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 m |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
||||||||||||||||
Подставляя (2.43) в выражение для средней энергии, получаем |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
m 12 |
|
|
|
|
2T 32 |
|
|
|
|
|
12 |
|
|
|
|
|
2T 32 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Ex |
m |
|
|
|
|
|
|
|
|
|
|
1 |
T |
1 |
T T (kT) |
|
(2.44) |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
2 |
2 |
|
|||||||||||||||||||||||||||||
|
|
2 |
2 T |
2 |
m |
|
|
|
2 T |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
37 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||

Итак, на одну колебательную степень свободы приходится энергия, равная в общепринятых единицах kT. Из расчета видно, что kТ/2 возникла из-за усреднения кинетической энергии колебательного движения, а kТ/2 - из-за потенциальной энергии колебательного движения. Здесь мы доказали теоре-
му о равномерном распределении энергии по степеням свободы. Согласно этой теореме на каждую колебательную степень свободы приходится энергия, равная kТ.
Глава 3. Квантовые статистические распределения.
§3.1. Статистическая сумма. Большой канонический ансамбль.
Известно, что все частицы в природе в зависимости |
от их спина |
делятся |
на фермионы и бозоны. Спин - это внутренний |
механический |
момент |
количества движения частицы не связанный с ее движением в пространстве. Частицы с полуцелым спином s = 1/2, 3/2, 5/2… называются фермионами, а частицы с целым значением s = 0, 1, 2, ... - бозонами. Так электрон, нейтрон, протон имеют s = 1/2 и являются фермионами. Бозонами являются фотон, векторные мезоны (s = 1) и гравитон (s = 2). В зависимости от спина, ядра атомов (и сами атомы) всех существующих в природе химических элементов тоже являются фермионами или бозонами. Различие между фермионами и бозонами заключается в возможности занимать одно и то же квантовое состояние нескольким тождественным частицам. Квантовые частицы неразличимы. Поэтому любые конфигурации, отличающимися только перестановками двух и более тождественных частиц считаются одинаковыми.
Многочастичные квантовые состояния системы удобно записывать в представлении чисел заполнения. Для этого введем полный набор одночастичных состояний { } с собственными энергиями { }, где индекс - номер состояния. Многочастичное состояние определяется указанием числа частицдля всех значений . Числа принимают значения:
=0,1,2,3, …. в случае статистики Бозе – Эйнштейна (Б-Э),
= 0,1 - в случае статистики Ферми – Дирака (Ф-Д).
Одно из центральных мест в квантовой статистике занимает понятие стати-
стической суммы (статсуммы)
|
|
= ∑ =1 − ≡ ∑ =1 − . |
(3.1) |
В этом выражении индекс n нумерует собственные функции |n> и собственные значения En всей системы. В квантовой статистике среднее значение оператора ̂ в соответствии с распределением Гиббса определяется выражением
38

|
|
|
|
̂ |
1 |
|
|
̂ |
− |
|
|
̂ |
|
|
|
|
|
|
= |
|
∑ |
|
| | |
≡ ∑ |
|
| | , |
(3.2) |
||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
1 |
|
− |
|
|
|
|
|
|
|
|
|
|
где |
|
– вероятность обнаружения системы в состоянии |n> . Если |
||||||||||||
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
статсумма известна, то с её помощью можно найти все термодинамические свойства системы.
Введём свободную энергию |
|
|
|
|
|
|
|
= − ln = − |
|
1 |
ln(∑ − ) |
(3.3) |
|||
|
|
||||||
|
|
|
|
|
|
|
|
и энтропию |
|
|
|
|
|
|
|
= − ∑ |
|
|
ln . |
(3.4) |
|||
|
|
|
|
|
|||
Определение энтропии (3.4) полностью соответствует определению, данному ранее в Главе 1. В условиях равновесия
= −( |
|
) . |
(3.5) |
|
|||
|
|
|
|
Использую нестационарную теорию возмущений легко показать, что при отклонении от равновесия энтропия с течением времени всегда возрастает
|
> 0. |
(3.6) |
|
|
|||
|
|
Рассмотрим полную энергию системы, находящейся в состоянии с номером
n: |
= |
= ∑ |
|
|
, |
где |
- энергии подсистем. Тогда |
( =1/kT ) |
полн |
|
|
|
|
|
|
|
= − 1 ln = − 1 ln ∑ − = − 1 ln ∑ 1 2, − ∑ =
−1 ln ∏ (∑ − ∑ ) = − 1 ∑ (ln ∑ − ∑ ) =
= ∑ (− |
1 |
ln ∑ |
|
|
− ∑ |
|
) ≡ |
(3.7) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Таким образом, свободная энергия всей системы есть сумма свободных энергий её подсистем.
При фиксированном числе частиц N в системе должно выполняться условие ∑ = , которое затрудняет вычисление статистической суммы. Данную проблему можно обойти, если ввести понятие химического потенциала для систем с переменным числом частиц. Ансамбль таких систем называется большим каноническим ансамблем. В этом ансамбле формально переходят к гамильтониану ̂ − ̂. Химический потенциал находится из условия
= ̂ и имеет смысл полной энергии, приходящейся на одну частицу.
В большом каноническом ансамбле статсумма равна
39

|
|
|
|
|
|
|
= ∑ 1,2,.. |
|
− ∑ ( − ) |
. |
|
(3.8) |
|||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
Свободная энергия = − |
|
|
ln |
называется термодинамическим потенциа- |
|||||||||||||||
|
|
||||||||||||||||||
лом. В случае, |
|
когда |
∑ |
|
|
|
= , |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= ∑ |
(∑ |
) |
{− [∑ ( |
− )]} = |
|||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
1, 2, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
= ∑ |
1, 2 , |
{− [∑ |
|
|
|
( − )]}. |
|
|
(3.9) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Однако, по определению,
̂ = 1 ∑ 1, 2. {− [∑ ( − )]},
|
̂ |
1 |
|
|
|
|
1 |
|
|
|
|
||||
|
|
|
|
|
|
||||||||||
так что |
= |
|
|
|
= |
|
|
|
ln |
|
= − |
|
. |
(3.10) |
|
Последнее уравнение позволяет найти зависимость от числа частиц .
Аналогичным образом можно получить:
|
|
|
|
|
|
|
|
|
|
|
|
|
̂ |
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
, |
|
= |
∑ . |
|
|
|
(3.11) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Внутренняя энергия системы |
|
|
|
|
|
|
|
|
|
||||||||||
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
( ) |
̂ |
|
|
= |
|
∑ |
1, |
2,.. |
(∑ |
|
|
|
) {− [∑ |
|
( |
− )]} = |
|
|
+ . |
(3.12) |
|||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
В качестве примера использования полученных выше формул рассмотрим одноатомный идеальный газ в трехмерном ящике с непроницаемыми стенками. Из квантовой механики известно, что энергия частиц равна
|
|
2 |
|
2 |
2 |
|
2 |
|
2 |
|
|
|
|
|
|
|
|
|
= |
|
|
( |
|
+ |
|
+ |
|
), |
где |
|
, |
|
, |
− размеры ящика, а − целые чис- |
|
2 |
|
|
|
||||||||||||||
|
|
|
2 |
2 |
2 |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
ла. Статистическую сумму запишем в виде Z=Zx Zy Zz. Отдельные сомножители легко вычисляются:
∞ |
|
|
2 2 |
2 |
|
∞ |
|
|
2 2 |
|
2 |
|
|
|
|
|
||||||
= ∑ exp (− |
|
|
|
|
) ∫ exp (− |
|
|
|
|
|
) |
|
= |
|
, |
|||||||
2 |
|
|
|
2 |
|
|
|
|||||||||||||||
|
|
|
2 |
|
0 |
|
|
|
2 |
|
|
|
1 |
|
||||||||
=0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
= |
|
, = |
|
|
, |
= 3 |
|
|
|
= 3 |
|
|
|
. |
|
|
||||||
1 |
1 |
|
3 |
|
|
|
|
3 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
2 |
|
|
|
|
2 |
|
|
|
2 |
|
|
|
2 |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
40 |
|
|
|
|
|
|
|
|
|
|
|
|
|
