
- •Скачек потенциала на границе металл / раствор.
- •Типы электродов.
- •Измерение электродвижущих сил.
- •Потенциометрическое титрование.
- •Краткое теоретическое обоснование
- •Порядок выполнения работы.
- •Обработка экспериментальных данных.
- •Приложение
- •1.Принцип действия иономера.
- •2.Инструкция к лабораторному блоку автоматического титрования бат-12-лм.
Измерение электродвижущих сил.
Компенсационный метод. Для измерения равновесной величины э. д. с. гальванического элемента необходимо, чтобы потенциалобразующий процесс совершался бесконечно медленно, следовательно, элемент должен работать при бесконечно малой силе тока. Это условие выполняется при измерении э. д. с. компенсационным методом, который основан на том, что исследуемый элемент последовательно включается против внешнего источника тока, так что ток от используемого гальванического элемента компенсируется встречным постоянным током от внешнего источника. Электродвижущую силу источника тока в свою очередь сравнивают с э. д. с. эталонного элемента, которая известна(см. рис.2).
В качестве эталона обычно применяют стандартный элемент, э. д. с. которого постоянна во времени и мало изменяется с температурой. В настоящее время для измерения э. д. с. применяют высокоомные потенциометры различных конструкции, содержащие все элементы компенсационной установки. Измерение э. д. с. компенсационным методом потенциометров дает весьма точные результаты при измерениях электродных потенциалов или опытном определении неизвестной э. д. с. Но этот метод неприменим, если внутреннее сопротивление элемента велико, например, у гальванических цепей со стеклянным электродом, в этом случае пользуются некомпенсационным методом.
Значения электродвижущей силы гальванического элемента определяют непосредственно на чувствительных вольтметрах постоянного тока с сопротивлением от 108 до 109 Ом и отсчетом до 1 мВ. Через такой вольтметр течет очень маленький ток, поэтому измеренная э. д. с. практически не отличается от измеренной на компенсационной установке.
Для измерений э. д. с. некомпенсационным методом применяют ламповые потенциометры, ламповые милливольтметры, рН-метры и ионометры различных конструкций. Шкалы приборов отградуированы в милливольтах или единицах рН. Метод используют для потенциометрического титрования и в ионометрии.
При измерениях э. д. с. электрохимических цепей некомпенсационным методом надо учитывать, что проходящий через элемент ток более 10-5 А вызывает концентрационную и химическую поляризацию и измеренная э. д. с. меньше равновесного значения.
Рис. 2 – Схема
компенсационной установки.
Работа №26
Потенциометрическое титрование.
Цель работы. Ознакомление с методикой потенциометрического титрования на примере определения концентраций сильной, слабой и смеси кислот.
Краткое теоретическое обоснование
Сущность потенциометрического титрования. Сущность метода состоит в том, что эквивалентную точку определяют не по изменению цвета индикатора, как это делается при обыкновенном методе титрования, а по изменению потенциала электрода.
Э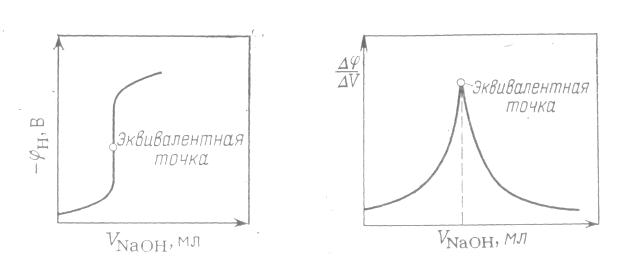 лектрод,
которым пользуются при потенциометрическом
титровании
для определения эквивалентной точки,
носит название индикаторного.
Индикаторный электрод, как правило,
должен быть
обратимым по отношению к ионам титруемого
вещества или
к ионам прибавляемого реагента (в
дальнейшем — просто реагента).
В зависимости от того, является ли
электрод обратимым
по отношению к ионам титруемого вещества
или по отношению
к ионам реагента, потенциал его по мере
титрования, согласно уравнению (15) будет
соответственно уменьшаться или
увеличиваться. В начале титрования
потенциал индикаторного электрода
изменяется медленно, но вблизи
эквивалентной точки
уже при добавлении незначительного
количества реагента
(1—2 капли) его потенциал изменяется
скачком. Этот скачок потенциала
Рис.3–Вид
кривой титрования HCI
едким натром.
Рис.4–Дифференциальная
кривая
лектрод,
которым пользуются при потенциометрическом
титровании
для определения эквивалентной точки,
носит название индикаторного.
Индикаторный электрод, как правило,
должен быть
обратимым по отношению к ионам титруемого
вещества или
к ионам прибавляемого реагента (в
дальнейшем — просто реагента).
В зависимости от того, является ли
электрод обратимым
по отношению к ионам титруемого вещества
или по отношению
к ионам реагента, потенциал его по мере
титрования, согласно уравнению (15) будет
соответственно уменьшаться или
увеличиваться. В начале титрования
потенциал индикаторного электрода
изменяется медленно, но вблизи
эквивалентной точки
уже при добавлении незначительного
количества реагента
(1—2 капли) его потенциал изменяется
скачком. Этот скачок потенциала
Рис.3–Вид
кривой титрования HCI
едким натром.
Рис.4–Дифференциальная
кривая
потенциометрического титрования HCI едким натром.
индикаторного
электрода и дает возможность определить
эквивалентную точку.
При
потенциометрическом титровании
практически удобнее (иногда
и необходимо) бывает следить не за
изменением потенциала
![]() ,
а за отношением изменения потенциала
к
,
а за отношением изменения потенциала
к
![]() соответствующему
изменению объема прибавленного реагента
соответствующему
изменению объема прибавленного реагента
![]() .
Это
объясняется тем, что отношение
.
Это
объясняется тем, что отношение
![]() изменяется вблизи эквивалентной
точки более резко, чем потенциал
,
что позволяет
точнее найти конечный момент титрования.
изменяется вблизи эквивалентной
точки более резко, чем потенциал
,
что позволяет
точнее найти конечный момент титрования.
Потенциометрическое титрование с успехом может быть использовано для количественного определения содержания в растворе кислот (метод нейтрализации), ионов галогенов (метод осаждения); ряда других ионов (метод комплексообразования).
Титрование кислот. При титровании кислот необходимо различать два случая:
титрование раствора сильной кислоты раствором сильного основания;
титрование раствора слабой кислоты раствором сильного основания.
В первом случае изменение концентрации ионов водорода происходит исключительно за счет реакции
Н3О + ОН– = 2Н2О (38)
При титровании сильной кислоты сильной щелочью эквивалентную точку определяют по точке перегиба кривой. Если по оси ординат откладывать отношение потенциала к соответствующему изменению объема ,а по оси абсцисс — объем реагента, то получается дифференциальная кривая, изображенная на рисунке.
При титровании слабых кислот скачок потенциала в эквивалентной точке выражен менее резко, чем в первом случае, что иногда затрудняет точное определение точки перегиба, следовательно, и конечного момента титрования.
На рисунке изображены кривые титрования растворов хлороводородной и уксусной кислот раствором сильного основания. Кривая титрования раствора уксусной кислоты вначале поднимается сравнительно круто (отрезок аб), отрезок бв — более пологий. Наконец, отрезок вг, отвечающий изменению потенциала в эквивалентной точке, значительно короче, чем аналогичный участок кривой титрования хлороводородной кислоты. Для очень слабых кислот отрезок вг на кривой титрования может исчезнуть совершенно, т. е. фактически в эквивалентной точке не будет наблюдаться заметного изменения потенциала.
Относительно быстрое изменение потенциала водородного электрода на участке аб объясняется тем, что концентрация ионов водорода, вследствие слабой диссоциации уксусной кислоты, быстро уменьшается при добавлении небольших количеств щелочи. Замедленное же изменение потенциала на участке бв обусловливается главным образом буферным действием соли, образующейся при реакции нейтрализации. Потенциал на участке вг определяется концентрацией ионов водорода в эквивалентной точке. Концентрация ионов водорода в этом случае может быть вычислена из уравнения
![]() ,
(39)
,
(39)
где Кдисс — константа диссоциации кислоты; Кв — ионное произведение воды; С — концентрация соли в эквивалентной точке.
При нейтрализации слабой кислоты сильным основанием в эквивалентной точке раствор будет уже не нейтральным, а щелочным, вследствие гидролиза образовавшейся соли.
Т итрование
смеси кислот.
При титровании смеси сильной и слабой
кислот удается потенциометрически
определить содержание
каждой из кислот в отдельности,
не производя предварительного
разделения их. При
титровании смеси сильной и
слабой кислот сначала будет
итрование
смеси кислот.
При титровании смеси сильной и слабой
кислот удается потенциометрически
определить содержание
каждой из кислот в отдельности,
не производя предварительного
разделения их. При
титровании смеси сильной и
слабой кислот сначала будет
Рис.5–Вид кривых титрования Рис.6–Вид кривой титрования смеси кислот
HCI и СН3СООН едким натром. HCI и СН3СООН едким натром.
нейтрализоваться первая. При потенциометрическом титровании таких кислот получают два скачка потенциала индикаторного электрода, а следовательно, и две точки перегиба на кривой титрования.
На рисунке изображена кривая титрования раствора смеси хлороводородной и уксусной кислот едким натром. Точки а1 и а2 на кривой являются точками перегиба. Первая соответствует полному оттитрованию хлороводородной кислоты в смеси, а вторая — уксусной кислоты. Пунктирная линия показывает изменение потенциала в эквивалентной точке, которое наблюдалось бы при нейтрализации раствора одной хлороводородной кислоты, имеющей такую же концентрацию, как и в смеси.
Приборы и реактивы. рН-метр (иономер), БАТ-12-ЛМ, магнитная мешалка, индикаторный электрод (стеклянный), хлорсеребряный электрод, бюретка емкостью 25 мл, стакан для титрования емкостью 100 мл, растворы кислот (уксусной, соляной и смеси этих кислот), раствор едкого натрия.
