
- •1. Переваривание и всасывание нуклеопротеидов
- •2. Метаболизм пуриновых и пиримидиновых нуклеотидов
- •Катаболизм пуриновых нуклеотидов
- •Реакции распада мочевой кислоты. От нуклеотидов к основаниям.
- •Катаболизм пиримидиновых нуклеотидов
- •Продукты распада нуклеотидов могут повторно использоваться (реутилизацироваться)
- •De novo синтез пуриновых и пиримидиновых рибонуклеотидов
- •De Novo синтез пуриновых нуклеотидов.
- •Регуляция синтеза пуриновых нуклеотидов de novo
- •Cинтез пиримидиновых нуклеотидов de novo
- •Рибонуклеотидредуктаза и биосинтез дезоксирибонуклеотидов
- •Регуляция активности рибонуклеотид редуктазы
- •Биосинтез тимидиловых дезоксирибонуклеотидов
- •Обмен дезоксиуридиловых нуклеотидов
- •Наиболее частые проявления нарушений обмена пуринов - гиперурикемия и подагра
- •Нарушение обмена пиримидиновых нуклеотидов также приводит к болезням.
- •Биосинтез днк – один из важнейших процессов передачи генетической информации последующим поколениям и ее хранения.
- •Ретровирусы внесли изменения в центральную догму молекулярной биологии.
- •Выход из состояния пролиферативного покоя требует специальных регуляторов.
- •У эукариот свой набор днк полимераз
- •Механизм синтеза рнк во многом напоминает синтез днк
- •Транскриптон (оперон) - единица транскрипции.
- •Промоторы имеют сходное строение
- •У эукариот – 3 рнк- полимеразы
- •Транскриптон (оперон) - единица транскрипции.
- •Промоторы имеют сходное строение
- •У эукариот – 3 рнк- полимеразы
- •В транскрипции у прокариот важная роль принадлежит -фактору
- •У эукариот молекула рнк модифицируется после транскрипции.
- •Кэпирование и полиаденилирование иРнКопределяют дальнейшие особенности функций иРнк
- •Сплайсинг – способ создания многообразия белков
- •1.Мультимедийная презентация
Регуляция синтеза пуриновых нуклеотидов de novo
В регуляции синтеза пуриновых нуклеотидов можно выделить несколько уровней. Управление синтезом в целом происходит на этапе фосфорибозиламидотрансферазы Как видно из рис. 9-18, основную роль в регуляции на этом уровне играет ингибирующее
влияние мононуклеотидов по механизму обратной связи и -или концентрация ФРПФ (см выше) . . Мононуклеотиды (АМФ и ГМФ). Второй уровень регуляции связан с контролем за поддержанием соответствующего равновесия между ATФ и ГТФ. АТФ, являясь источником энергии для синтеза ГМФ, стимулирует образование ГМФ. В свою очередь ГТФ, как источник энергии для синтеза АМФ, стимулирует образование АМФ
Кроме того, каждый их нуклеотидов тормозит свое образование по принципу обратной связи, действуя на ферменты своего синтеза. ГМФ тормозит преобразование ИМФ в КсMФ, а AMФ тормозит преобразование ИМФ в аденилсукцинат.
Т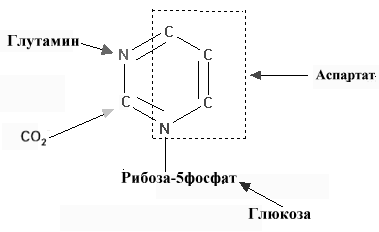 акое
многоуровневое и согласованное действие
регуляторов позволяет поддерживать
соотношение мононуклеотидов на уровне,
обеспечивающем потребности в них в
клетке
акое
многоуровневое и согласованное действие
регуляторов позволяет поддерживать
соотношение мононуклеотидов на уровне,
обеспечивающем потребности в них в
клетке
Cинтез пиримидиновых нуклеотидов de novo
Структура пиримидинового кольца проще, и путь биосинтеза пиримидинов короче, чем у пуринов. Амидный азот глутамина и диоксид углерода обеспечивает атомы 2 и 3 кольца пиримидина после преобразования их в карбамоилфосфат. Другие четыре атома кольца происходят из аспартата. Так же как и в случае с пуриновыми нуклеотидами, углеводная часть поставляется ФРПФ.
Карбамоилфосфат. Образование пиримидиновых нуклеотидов начинается с синтеза карбамоил фосфата, который протекает в цитозоле тканей, способных к образованию пиримидинов (наиболее высокая активность синтеза в селезенке, тимусе, ЖКТ и яичках).
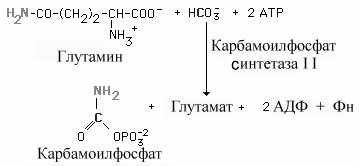 Карбамоил
фосфат, как упоминалось в главе об обмене
аминокислот, используется также в
синтезе мочевины.
Карбамоил
фосфат, как упоминалось в главе об обмене
аминокислот, используется также в
синтезе мочевины.
Его образование в клетках катализируется двумя разными карбамоилфосфат синтетазами - I и II.Основные различия между ними приведены в таблице 9-3.
Сравнительная характеристика карбомоилфосфат синтетаз I и II |
||
|
Карбамоил фосфат синтетаза I |
Карбамоил фосфат синтетаза II |
Распределение в тканях |
Преимущественно печень |
Во всех тканях |
Клеточная локализация |
Митохондрия |
Цитозоль |
Метаболический путь |
Синтез мочевины |
Биосинтез пиримидинов |
Источник азота |
Ионы аммония |
Аминогруппа глутамина |
Карбамоилфосфат синтетаза II (КФС II) предпочитает амид глутамина свободному аммиаку и не требует N-ацетилглутамата в качестве косубстрата. У человекаn КФСII, аспартат-транскарбамоилазная, и дигидрооротазная активности - это части одного мультифункционального белка.
Образование оротовой кислоты. Ключевая реакция. Первая уникальная для биосинтеза пиримидинов реакция – это реакция конденсации карбамоилфосфата и аспартата с образованием карбамоиласпартата, катализируемая аспартаттранскарбамоилазой (реакция
2 ).
Затем дигидрооротаза катализирует
отщепление Н2О
с образованием кольцевой структуры
(реакция
-3). Дегидрогеназа дигидрооротата,
используя НАД+
в качестве кофермента, формирует
оротовую кислоту - основного предшественника
пиримидиновых
).
Затем дигидрооротаза катализирует
отщепление Н2О
с образованием кольцевой структуры
(реакция
-3). Дегидрогеназа дигидрооротата,
используя НАД+
в качестве кофермента, формирует
оротовую кислоту - основного предшественника
пиримидиновых
. Реакции синтеза пиримидиновых нуклеотидов
оснований (реакция 4).
Образование нуклеотидов. Образование мононуклеотида происходит в реакции 5 путем присоединения к оротовой кислоте остатка рибоза-5-фосфата. Донором моносахарида служит ФРПФ. Первый пиримидиновый мононуклеотид - оротидинмонофосфат (ОМР). Эта реакция катализируется оротат-фосфорибозилтрансферазой — ферментом, аналогичным гипоксантин-гуанин— фосфорибозилрансферазе и аденин-фосфорибозил трансферазе, которые участвуют в фосфорибозилировании пуриновых колец при их реутилизации.
Первый главный пиримидиновый рибонуклеотид - уридиловая кислота (уридинмонофосфат, УМФ) образуется путем декарбоксилирования оротидилата (реакция б). Дигидрооротатдегидрогеназа — митохондриальный фермент. Все остальные ферменты, участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному янием аминоимидазолилрибозилфосфатсинтетазы
участвующие в синтезе пиримидинов de novo, локализуются в цитозоле. УМФ подвергается двукратному фосфорилированию и образующийся УТФ аминируется с участием глутамина и АТФ и образованием ЦТФ (реакция 9).
Регуляция синтеза пиримидиновых нуклеотидов Ключевым ферментом синтеза пиримидиновых нуклеотидов у человека является цитоплазматическая КФС II. УТФ тормозит активность этого фермента, конкурируя с ATФ. ФРПФ является активатором этого фермента. Имеются и другие участки регуляции (например, OMФ декарбоксилаза ингибируется УМФ и ЦМФ). Однако при нормальных условиях эти участки имеют ограниченное значение. У бактерий ключевым регуляторным ферментом является аспартат транскарбомоилаза. У них имеется только одна карбомоилфосфат синтетаза, так как они не имеют митохондрий. Карбомоилфосфат, таким образом, находится на развилке метаболических путей, которая ведет или к образованию пиримидиновых нуклеотидов или к синтезу аргинина.
Суммарная сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов приводится в следующей таблице.
Таблица 9-5. Сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов |
||
|
Путь синтеза пуринов |
Путь синтеза пиримидинов |
Последовательность синтеза |
1.Образование N-гликозидной связи 2.Сборка кольцевой структуры |
1.Сборка кольцевой структуры 2.Образование N-гликозидной связи |
Ключевая реакция |
Образование фосфорибозилами на(фосфорибозиамидотрансфераза) |
Образование карбамоилфос фата (Аспартат транскарба моилаза) |
Локализация в клетке |
Цитозоль |
Митохондрии и цитозоль |
Ферментгная орнганизация |
Отдельные ферменты и полифункциональные (3) |
Отдельные ферменты и полифункциональные (2) |
Регуляция |
Торможение ИМФ,АМФ и ГМФ вна нескольких уровнях |
Торможение УТФ карбамоилфосфатсинтетазы II |
