
- •Обмен аминокислот. Дезаминирование и трансаминирование аминокислот. Обезвреживание аммиака. Образование и выведение мочевины.
- •Основные вопросы лекции:
- •Белки – высокомолекулярные органические полимеры, построенные из аминокислот, связанных между собой
- •Ежесуточно в организме человека обновляется 1 - 2% всех белков (300 г/сут)
- •Обновление белков организма
- •Пул (фонд) свободных аминокислот
- •Азотистый баланс
- •Факторы, влияющие на интенсивность азотистого обмена
- •Поступление белков с пищей
- •Качественный состав белка зависит от состава аминокислот.
- •Биологическая ценность белка определяется его аминокислотным составом.
- •Недостаточность белка в рационе. Квашиоркор -
- •Недостаточность аминокислот.
- •Протеолиз – распад белков до аминокислот.
- •Переваривание белков в ЖКТ
- •Образование и функции соляной кислоты
- •Изменения концентрации Hcl в желудочном соке
- •Ферменты желудочного сока
- •Ферменты желудочного сока.
- •Переваривание белков в тонком кишечнике осуществляется ферментами панкреатического происхождения.
- •Активация трипсина.
- •Ферменты кишечного сока синтезируются клетками тонкого
- •Защита клеток ЖКТ от действия протеаз.
- •Транспорт аминокислот в клетки.
- •Нарушение переваривания белков и транспорта аминокислот.
- •Гниение аминокислот в кишечнике. Обезвреживание и выведение продуктов гниения.
- •Применение протеолитических ферментов и их ингибиторов.
- •Катаболизм аминокислот.
- •Общие пути катаболизма аминокислот.
- •Дезаминирование аминокислот. Поток азота в ходе катаболизма аминокислот.
- •Катаболизм аминокислот начинается с удаления аминогруппы.
- •Анаэробное прямое окислительное дезаминирование
- •Непрямое дезаминирование. Дезаминирование через стадию трансаминирования -
- •Химизм процесса трансаминирования
- •В наиболее значимых реакциях трансаминирования участвуют аспартатаминотрансфераза (АСТ)
- •Клинико-диагностическое значение определения активности аминотрансфераз крови.
- •Локализация аминотрансфераз в клетке
- •Изменение активности АЛТ, АСТ в крови при заболеваниях печени и миокарда.
- •Аминокислоты могут давать энергию. Гликогенные и кетогенные аминокислоты.
- •Глюкозо - аланиновый цикл
- •В клетках постоянно образуется аммиак.
- •Пути обезвреживание аммиака в организме.
- •Токсичность аммиака.
- •Восстановительное аминирование α-кетоглутарата с образованием глутаминовой кислоты..
- •Синтез глутамина - одним из важных способов утилизации аммиака в нервной и мышечной
- •С током крови ГЛУ (н) транспортируется в почки, где происходит гидролиз ГЛУ(н) под
- •Печень – единственный орган, клетки которого содержат все ферменты биосинтеза мочевины.
- •Синтез карбамоилфосфата – ключевая реакция синтеза мочевины.
- •Цитруллин – аминокислота, которая не кодируется генетически
- •Аспартат – источник NH2–группы.
- •Аргинин синтезируется при распаде аргининосукцината.
- •Орнитин – аминокислота, которая не кодируется генетически.
- •Синтез мочевины – регулируемый процесс.
- •Гипераммониемия
- •Энзимопатии орнитинового цикла.
- •Определение концентрации мочевины
- •Определение концентрации мочевины
- •Определение концентрации мочевины в биологических жидкостях при
- •Определение концентрации мочевины в биологических жидкостях.
- •Благодарю за внимание!

Биологическая ценность белка определяется его аминокислотным составом.
Чем ближе аминокислотный состав
пищевого белка к аминокислотному составу
нашего организма, |
тем |
выше его ценность |
|
Белки животного происхождения более ценные!
Эталонный белок –белок куриного яйца.

Недостаточность белка в рационе. Квашиоркор -
форма белковой недостаточности, развивающаяся при однообразном питании продуктами растительного происхождения
смалым содержанием белка.
Встречается среди населения стран тропического и субтропического пояса Африки,
Латинской Америки и |
Юго- |
Восточной Азии. |
|
Этим заболеванием страдают преимущественно дети в возрасте 1 - 5 лет.
Проявления: отставание в росте, поражение печени, кожи, атония мышц и т.п.
Недостаточность аминокислот.
Развивается при |
Аминокислота |
Проявление недостаточности |
|
- полном голодании |
Лизин |
Головокружение, тошнота, |
|
- частичном голодании |
|||
|
чувствительность к шуму |
||
- получении только |
|
||
Аргинин |
Атрофия семенников, |
||
растительных белков |
|||
|
гипоспермия |
||
|
|
||
|
Метионин |
Жировая |
|
|
|
инфильтрация печени |

Протеолиз – распад белков до аминокислот.
Протеолитические ферменты, осуществляющие гидролиз пептидной связи, объединяют термином пептидазы.
Экзопептидазы - отщепляют по одной аминокислоте с N или С конца полипептидной цепи;
Эндопептидазы – воздействуют на связи внутри полипептидной цепи
(протеиназы или протеазы).
Для усвоения организмом пищевых белков необходимо их полное расщепление до аминокислот в желудочно-кишечном тракте
(всасываются только аминокислоты, т.к. лишены антигенных свойств)
ВЖКТ происходит тотальный протеолиз, благодаря
-набору ферментов
-оптимуму рН
-регуляции последовательности процессов.
Переваривание белков в ЖКТ
Ротовая полость: |
не |
содержит ферментов |
|
переваривания белков, |
здесь |
осуществляется механическое дробление белковой пищи.
Желудок:
Основная пищеварительная функция желудка заключается в том, что в нём начинается
переваривание белка.
Желудочный сок –
секрет желез слизистой оболочки желудка:
Объем /сут |
1,5 - 2 л |
Hcl |
300 - 400 моль |
Ферменты |
0,5 - 1,15 г |
Белки (муцин) |
7 г |
Бикарбонаты, |
|
Nacl, фосфат |
45 ммоль/л |
|
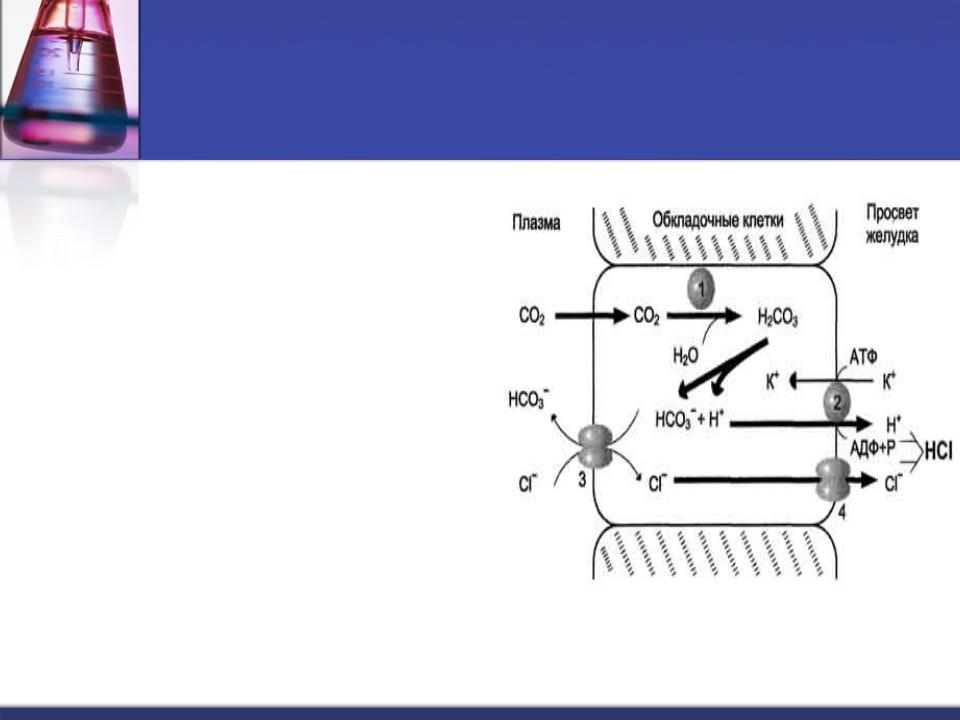
Образование и функции соляной кислоты
Образование Hcl идет в обкладочных клетках желудка.
Образование Hcl требует затраты АТФ.
Важную роль в синтезе Hcl играет фермент карбоангидраза.
Функции Hcl:
активация пепсиногена,
создание оптимума рН,
денатурация белков,
бактерицидное действие.
Изменения концентрации Hcl в желудочном соке
Проявление
изменения концентрации Hcl
Гиперацидное состояние |
Гипоацидное состояние |
Гипохлоргидрия |
|
Гиперхлоргидрия |
Ахлоргидрия |
|
Ахилия |
Причиной кислотозависимых заболеваний может стать:
разбалансировка функционирования механизмов кислотопродукции
недостаточная эффективность сфинктеров,
неправильные питание или образ жизни и др.

Ферменты желудочного сока
Пепсин
Образуется из профермента пепсиногена путем
частичного протеолиза. Оптимум рН 1-2. Пепсин - эндопептидаза, осуществляет гидролиз
пептидных связей внутри белковой молекулы,
образованных аминокислотами: ГЛУ, АСП,ТИР,ФЕН.

Ферменты желудочного сока.
Гастриксин – эндопептидаза, оптимум
рН 3,2-3,5. Образуется из пепсиногена, гидролизует внутренние пептидные связи с образованием коротких пептидов.
Реннин (сычужный фермент) – эндопептидаза,
оптимум рН 4,5;
вызывает створаживание молока в присутствии Са2+. Есть только у детей
грудного возраста. В желудке взрослых людей реннина нет, молоко створаживается под действием НСl, пепсина.
Пепсин, реннин и гастриксин имеют сходство по первичной структуре, что указывает на их происхождение от общего
гена-предшественника.
Переваривание белков в тонком кишечнике осуществляется ферментами панкреатического происхождения.
В поджелудочной железе синтезируются проферменты
(неактивная форма) ряда протеаз: трипсиноген химотрипсиноген проэластаза прокарбоксипептидазы А и В.
В кишечнике они превращаются в активные ферменты путем частичного протеолиза:
трипсин
химотрипсин
эластаза карбоксипептидазы А и В.
