
- •1.Введение
- •2.Исходное сырье
- •3.Характеристика целевого продукта
- •3.1 Физические свойства
- •3.2 Химические свойства метилового спирта
- •4.Физико-химическое обоснование основных процессов производства целевого продукта и экологической безопасности производства
- •4.1 Основные реакции:
- •4.2 Приведем некоторые побочные реакции:
- •4.3 Температура:
- •4.4 Катализатор:
- •5.Описание технологической схемы процесса
- •5.1 Процесс при 32мПа:
- •5.3 Функциональная схема производства метанола
- •5.4 Структурная блок-схема
- •6.Расчет материального баланса хтс
- •6.1 Условно-постоянная информация для расчета
- •6.2 Исходные данные для расчёта. Вариант №4.
- •6.3 Балансовая математическая модель
- •6.4 Соответствие переменных потокам
- •6.5 Матрица
- •6.6 Материальный баланс хтс производства метилового спирта в расчёте на 1500 кг
- •8.Список использованной литературы
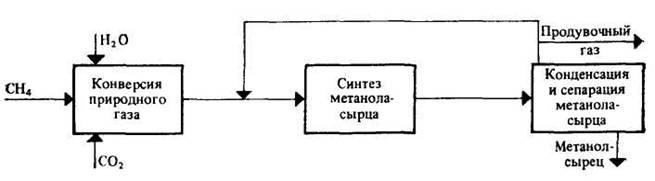
5.3 Функциональная схема производства метанола
Технологический процесс получения метанола из оксида углерода и водорода включает ряд операций, обязательных для любой технологической схемы синтеза. Газ предварительно очищается от карбонила железа, сернистых соединений, подогревается до температуры начала реакции и поступает в реактор синтеза метанола. По выходе из зоны катализа из газов выделяется образовавшийся метанол, что достигается охлаждением смеси, которая затем сжимается до давления синтеза и возвращается в процесс.
5.4 Структурная блок-схема
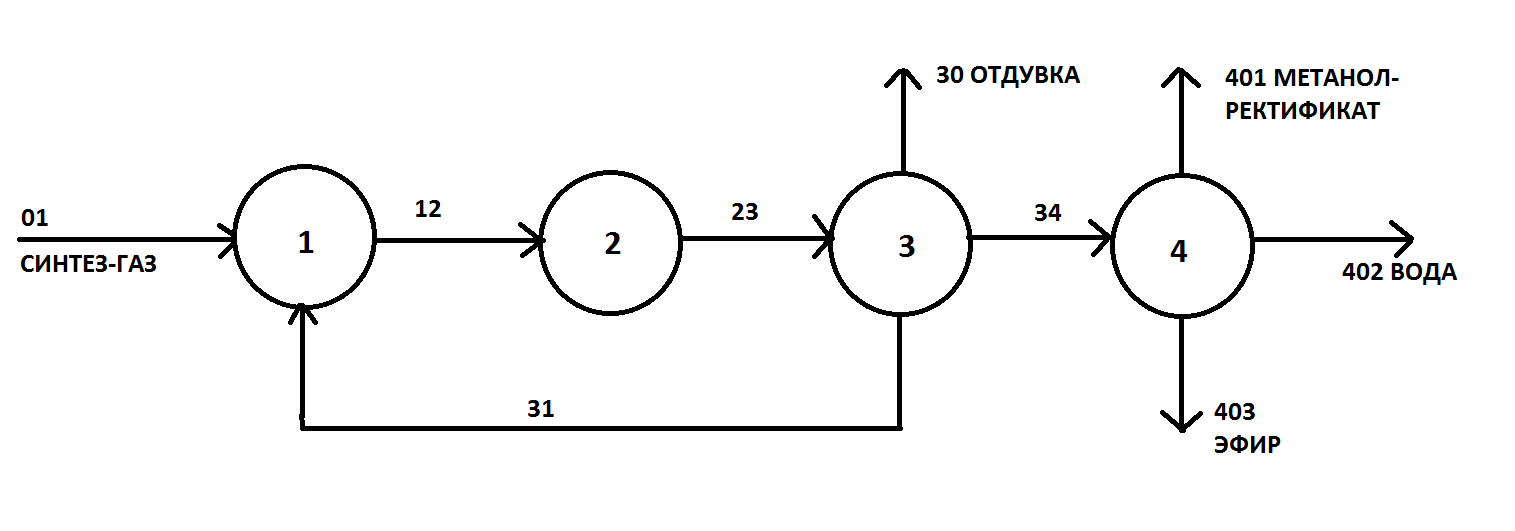
Потоки: 01 - свежий газ; 12 - Смесь газов; 23,34 – смесь продуктов; 31 – циркуляционный газ; 30 – отдувочный газ; 401 – метанол-ректификат; 402 – вода; 403 – эфир. Блоки: 1 – смешение; 2 – синтез; 3 – конденсация и сепарация; 4 – ректификация.
6.Расчет материального баланса хтс
6.1 Условно-постоянная информация для расчета
Производство метанола основано на реакции:
СО +
2Н2 ![]() СН3ОН
СН3ОН
Одновременно протекают побочные реакции:
СО + 3Н2 = СН4 + Н2О
2СО + 4Н2 = (СН3)2О + Н2О
6.2 Исходные данные для расчёта. Вариант №4.
|
№ |
Содержание информации |
Условное обозначение |
Единица измерения |
Принятое значение |
||
|
1 |
Содержание СО в циркуляционном газе |
ɣ31CO |
Мольные доли |
0,12 |
||
|
2 |
Содержание Н2 в циркуляционном газе |
ɣ31H2 |
Мольные доли |
0.74 |
||
|
3 |
Содержание инертных примесей в циркуляционном газе |
ɣ31CH4 |
Мольные доли |
0,14 |
||
|
4 |
Содержание инертных примесей в свежем газе |
ɣ01СH4 |
Мольные доли |
0,04 |
||
|
5 |
Общая конверсия СО |
X |
Мольные доли |
0.2 |
||
|
6 |
Доля СО, превратившегося в СН3OH |
φCH3OHCO |
Доли |
0,95 |
||
|
7 |
Доля СО, превратившегося в (СН3)2О |
φ(CH3)2OCO |
Доли |
0,03 |
||
|
8 |
Доля СО, превратившегося в СН4 |
φCH4CO |
Доли |
0,02 |
||
|
9 |
Базис расчета |
П |
Кг СН4ОН ректификата |
1500 |
||
6.3 Балансовая математическая модель
1) N01CO+N31ɣ31CO=N12CO
2) N01H2+ N31ɣ31H2= N12H2
3) N12CO(1-X)= N31ɣ31CO+ N30ɣ31CO
4) N12H2=2N12COX(ɣ403(CH3)2O+φCH3OHCO)+ N31ɣ31H2+ N30ɣ31H2+3 N12COXφCH4CO
5) (ПCH3OH ɷCH3OH)/MCH3OH = N12COXφCH3OHCO
6) N30ɣ31CH4 = (( N01H2+ N01CO)/(1- ɣ01СH4)) ɣ01СH4+ N12COXφCH4CO
7)
N403
=
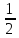 N12COXφ(CH3)2OCO
N12COXφ(CH3)2OCO
8)G402
=
N12COXφCH4CO
MH2O
+
 N12COXφ(CH3)2OCOMH2O
– П(1-ɷCH3OH)
N12COXφ(CH3)2OCOMH2O
– П(1-ɷCH3OH)
6.4 Соответствие переменных потокам
|
Наименование потока |
Условное обозначение |
Обозначение переменной |
Размерность |
Значение по расчёту |
|
Количество СО в исходном газе |
N01CO |
X1 |
кмоль |
57,343 |
|
Поток циркуляционного газа |
N31 |
X2 |
кмоль |
1567,780 |
|
Количество СО после смешения |
N12CO |
X3 |
кмоль |
245,477 |
|
Количество Н2 в исходном газе |
N01H2 |
X4 |
кмоль |
150,036 |
|
Количество Н2 после смешения |
N12H2 |
X5 |
кмоль |
1310,192 |
|
Отдувка |
N30 |
X6 |
кмоль |
68,734 |
|
Количество (СН3)2О на выходе из ректификационной колонны |
N403 |
X7 |
кмоль |
0,736 |
|
Количество воды на выходе из ректификационной колонны |
G402 |
X8 |
кг |
23,430 |
