
- •29) Средняя кинетическая энергия молекул идеального газа.
- •34) Среди равновесных процессов, происходящих с термодинамическими системами, выделяются изопроцессы, при которых один из основных параметров состояния сохраняется постоянным.
- •37) Явление переноса в термодинамически неравновесных системах
- •Статистическое толкование энтропии.
- •50) Барометрическая формула. Закон Больцмана для распределения частиц во внешнем потенциальном поле.
Статистическое толкование энтропии.
Рассматривая Вселенную как изолированную систему и распространяя на неё второй закон термодинамики, Р. Клаузиус пришёл к выводу о неизбежности «тепловой смерти» Вселенной, при которой в необозримом будущем в ней будет достигнуто состояние термодинамического равновесия и всякие процессы прекратятся. Этот вывод вызвал много споров, которые не прекращаются до сих пор. Из сказанного в предыдущем разделе следует, что к Вселенной в целом как изолированной системе (F = 0) второе начало термодинамики неприменимо по определению. В силу этого предсказанная Р. Клаузиусом «тепловая смерть» вследствие непрерывного возрастания энтропии ей не угрожает. Понятие энтропии приложимо исключительно к открытым (неизолированным) термодинамическим системам.
Напомним, что ни классическая, ни современная термодинамика не отрицают применимости второго начала к изолированным системам и в силу этого принципиально не могут противостоять упомянутому выше утверждению Клаузиуса достаточно решительно. Они опираются на статистическое истолкование второго закона с помощью формулы Больцмана: S = k ln P, где P — термодинамическая вероятность состояния системы. При этом второй закон термодинамики формулируется следующим образом: природа стремится от состояния менее вероятного к состоянию более вероятному.
Таким образом, являясь статистическим законом, второй закон классической термодинамики выражает закономерности хаотического движения большого числа частиц, входящих в состав изолированной системы. Для систем с относительно малым или бесконечным числом частиц второй закон термодинамики неприменим: в первом случае из-за возможных значительных флуктуаций, во втором — из-за равновероятности всех микросостояний.
Как видим, формулировка второго закона термодинамики, данная Больцманом, содержит в себе указание на относительность (нефундаментальность) этого закона и на недопустимость распространения его, на всю Вселенную в целом. В масштабах последней «на отдельных её участках вполне вероятны весьма мощные флуктуации энтропии. На этих участках естественными и самопроизвольными будут те процессы, которые сопровождаются не ростом, а уменьшением энтропии».
«Решив» таким образом, проблему тепловой смерти Вселенной, классическая и современная термодинамика одновременно предоставили карт-бланш изобретателям вечных двигателей второго рода. В самом деле, равновесную окружающую среду вполне правомерно представить как систему с бесконечным числом частиц (молекул) и на этом основании игнорировать второй закон термодинамики. С другой стороны, двигатель в масштабах окружающей среды представляет собой систему с относительно малым числом частиц, для которой второй закон термодинамики также неприменим. Возможность отбора теплоты от окружающей среды для выполнения работы оказалась, таким образом, вполне легитимной. Тем более, что для отопления помещений посредством тепловых насосов отбор теплоты от окружающей среды широко практикуется.
42)
43) ВАН-ДЕР-ВААЛЬСА УРАВНЕНИЕ - уравнение состояния реального газа. Предложено И. Д. Ван-дер-Ваальсом (J. D. van der Waals) в 1873. Для газа, содержащего N молекул, В. у. имеет вид:
![]()
где
V - объём, р - давление, T -
абс. темп-pa газа, а и b - постоянные,
учитывающие притяжение и отталкивание
молекул. Член
![]() наз.
внутр. давлением, постоянная b равна
учетверённому объёму молекулы газа,
если в качестве модели молекулы принять
слабо притягивающиеся упругие сферы.
наз.
внутр. давлением, постоянная b равна
учетверённому объёму молекулы газа,
если в качестве модели молекулы принять
слабо притягивающиеся упругие сферы.
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул, которая определяет внутреннюю энергию идеального газа и потенциальную энергию межмолекулярного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к возникновению внутреннего давления на газ
![]()
44) Фазой называется термодинамически равновесное состояние вещества, отличающееся по физическим свойствам от других возможных равновесных состояний того же вещества. Если, например, в закрытом сосуде находится вода, то эта система является двухфазной: жидкая фаза — вода; газообразная фаза — смесь воздуха с водяными парами. Если в воду бросить кусочки льда, то эта система станет трехфазной, в которой лед является твердой фазой. Часто понятие «фаза» употребляется в смысле агрегатного состояния, однако надо учитывать, что оно шире, чем понятие «агрегатное состояние». В пределах одного агрегатного состояния вещество может находиться в нескольких фазах, отличающихся по своим свойствам, составу и строению (лед, например, встречается в пяти различных модификациях — фазах). Переход вещества из одной фазы в другую — фазовый переход — всегда связан с качественными изменениями свойств вещества. Примером фазового перехода могут служить изменения агрегатного состояния вещества или переходы, связанные с изменениями в составе, строении и свойствах вещества (например, переход кристаллического вещества из одной модификации в другую).
Различают фазовые переходы двух родов. Фазовый переход I рода (например, плавление, кристаллизация и т. д.) сопровождается поглощением или выделением теплоты, называемой теплотой фазового перехода. Фазовые переходы I рода характеризуются постоянством температуры, изменениями энтропии и объема. Объяснение этому можно дать следующим образом. Например, при плавлении телу нужно сообщить некоторое количество теплоты, чтобы вызвать разрушение кристаллической решетки. Подводимая при плавлении теплота идет не на нагрев тела, а на разрыв межатомных связей, поэтому плавление протекает при постоянной температуре. В подобных переходах — из более упорядоченного кристаллического состояния в менее упорядоченное жидкое состояние — степень беспорядка увеличивается, т. е., согласно второму началу термодинамики, этот процесс связан с возрастанием энтропии системы. Если переход происходит в обратном направлении (кристаллизация), то система теплоту выделяет.
Фазовые переходы, не связанные с поглощением или выделением теплоты и изменением объема, называются фазовыми переходами II рода. Эти переходы характеризуются постоянством объема и энтропии, но скачкообразным изменением теплоемкости. Общая трактовка фазовых переходов II рода предложена академиком Л. Д. Ландау (1908—1968). Согласно этой трактовке, фазовые переходы II рода связаны с изменением симметрии: выше точки перехода система, как правило, обладает более высокой симметрией, чем ниже точки перехода. Примерами фазовых переходов II рода являются: переход ферромагнитных веществ (железа, никеля) при определенных давлении в температуре в парамагнитное состояние; переход металлов и некоторых сплавов при температуре, близкой к 0 К, в сверхпроводящее состояние, характеризуемое скачкообразным уменьшением электрического сопротивления до нуля; превращение обыкновенного жидкого гелия (гелия I) при Т=2,9 К в другую жидкую модификацию (гелий II), обладающую свойствами сверхтекучести.
45) Капиллярность (поверхностное натяжение) – это свойство жидкости изменять положение ее поверхности, вызванное натяжением и силой взаимодействия между нею и стенками трубок или мелкими порами грунта. Поверхностное натяжение зависит от температуры, уменьшаясь с ее ростом.
Смачивание явление, возникающее при соприкосновении жидкости с поверхностью твёрдого тела или другие жидкости. Оно выражается, в частности, в растекании жидкости по твёрдой поверхности, находящейся в контакте с газом (паром) или другой жидкостью, пропитывании пористых тел и порошков, искривлении поверхности жидкости у поверхности твёрдого тела.
46) Жидкостями называются тела, которые имеют определенный объем, но не имеют упругости формы. Жидкости отличаются сильным межмолекулярным взаимодействием и, вследствие этого, малой сжимаемостью. Малая сжимаемость жидкостей объясняется тем, что небольшое уменьшение расстояния между молекулами на малых взаимных расстояниях приводит к появлению больших сил межмолекулярного отталкивания. Коэффициент сжимаемости для жидкостей изменяется в пределах от 2*10-6 до 2*10-4 атм-1. 2. Обычные жидкости изотропны, за исключением жидких кристаллов, анизотропность которых в отношении ряда физических свойств связана с преобладанием у них в различных микрообъемах определенной ориентации молекул. 3. В жидкостях наблюдается ближний порядок - упорядоченное относительное расположение (или взаимная ориентация в жидких кристаллах) соседних частиц жидкости внутри малых ее объемов. Структура жидкости и ее физические свойства описываются набором функций распределения положений групп ее частиц. Наибольшее значение имеет радиальная функция распределения, характеризующая радиальное распределение частиц вокруг одной из них (центральной). Плотностью радиального распределения называется число центров частиц, попадающих внутрь шарового слоя, ограниченного радиусами r и r + dr, где r - расстояние от центральной частицы 4. Молекулы жидкости совершают тепловые колебания около положений равновесия со средней частотой 1/t0, близкой к частотам колебаний атомов в кристаллах, и амплитудой, определяемой «свободным объемом», предоставленным молекуле ее соседями. По истечении времени t >> t0 эти положения равновесия смещаются на расстояния порядка 10-8 см. Среднее (по совокупности большого числа молекул) время t, называемое временем релаксации, является характерным временем, связанным с перемещением частиц жидкости на расстояния порядка 10-8 см.
47) Кристаллическими веществами называют вещества, которые обладают трехмерной кристаллической решеткой. Это значит, что атомы в таких веществах расположены друг относительно друга в определенной закономерности, которую называют кристаллической решеткой. Вещества, имеющие кристаллическую решетку, – твердые. Такие вещества называют кристаллами.
авенство молярных теплоемкостей имеет место и в случае одноатомных твердых тел, к числу которых относятся металлы. У твердых тел не различают ср и cv, а говорят просто об удельной теплоемкости с. Как было в 1819 г. установлено П. Л. Дюлонгом и А. Т. Пти, молярная теплоемкость твердых одноатомных тел примерно одинакова и равна 3R=25 Дж/(моль•К), где R — газовая постоянная.
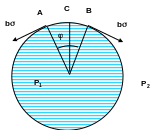
48) Давление под изогнутой поверхностью. Формула Лапласа На стороны малого участка АВ действуют силы bs. Их равнодействующая направлена по радиусу и равна:
f=2bssin(j/2)»bsj
т.к. j=|АВ|/R ® f=sS/R
окончательно получаем:
Р1-Р2=f/S=s/R
Капиллярные явления Искривление поверхности жидкости у краев сосуда особенно отчетливо видно в узких трубках, где искривляется вся свободная поверхность жидкости. В трубках с узким сечением эта поверхность представляет собой часть сферы, ее называют мениском
49) Закон Максвелла для распределения молекул идеального газа по скоростям и энергиям.
Закон распределения молекул идеального газа по скоростям (закон Максвелла) определяет вероятное количество dN молекул из полного их числа N (число Авогадро) в данной массе газа, которые имеют при данной температуре Т скорости, заключенные в интервале от V до V + dV: dN/N=F(V)dV F(V) - функция распределения вероятности молекул газа по скоростям определяется по формуле; F(V)=4π(M/2πRT)3/2 V2 exp(MV2/2RT) где V - модуль скорости молекул, м/с; - абсолютная температура, градусы Кельвина, К; М - молярная масса, кг/моль, численно равная молекулярной массе; R = 8,3144 Дж/(моль•К) - универсальная газовая постоянная в системе СИ
