
Лабораторная работа n1 Изучение, исследование и моделирование процесса
термической диффузии.
1. Цель работы.
Изучение основных положений термической диффузии в полупроводниках, методов реализации термических процессов перераспределения примесей в объеме твердого тела, технологии диффузного легирования кремния, основных методов расчета диффузных структур и контроля их параметров.
2.Теоретическая часть.
Ряд технологических процессов в производстве полупроводниковых приборов и интегральных схем (ИС) основан на непосредственном соприкосновении различных фаз и переходе при этом соответствующих компонентов из одной фазы в другую или перемещении компонентов в пределах одной фазы. Во всех этих процессах происходит перемещение компонента из одной фазы в другую или внутри одной фазы, которое называется диффузией. Диффузия протекает в результате стремления системы достигнуть физико-химического равновесия, т.е. до тех пор, пока химические потенциалы компонентов фазы μ во всех частях ее станут равными (для однородной системы).
При производстве современных изделий электронной техники (ИЭТ), в том числе электронно-оптических изделий, диффузия является одним из методов введения в объем твердого тела примесных атомов, определяющих тип проводимости и уровень легирования диффузионного слоя. С другой стороны термическая диффузия используется как базовый процесс перераспределения примесей из поверхностных слоев твердого тела в объем, с целью получения заданных профилей распределения примесных атомов и глубины залегания легированных слоев. При этом предполагается, что примесные атомы введены в приповерхностные слои твердого тела (полупроводника) методом ионной имплантации или радиационно-стимулированной диффузии.
Таким образом, диффузией называют перенос вещества, обусловленный хаотическим тепловым движением атомов, возникающий при наличии градиента концентрации данного вещества, и направленный в сторону убывания этой концентрации в той среде, где происходит диффузия.
Математическое описание диффузионных процессов было впервые предложено в 1855 г. А. Фиком в виде двух законов, основанных на уравнениях теплопроводности.
Первый закон Фика характеризует скорость проникновения атомов одного вещества в другое при постоянном во времени потоке этих атомов и неизменном градиенте их концентрации:
![]() ,
(1)
,
(1)
где F – вектор плотности
потока атомов вещества,
![]() С
– вектор градиента концентрации
диффундирующих атомов; D
– коэффициент пропорциональности, или
коэффициент диффузии. Коэффициент
диффузии (см2/с) является мерой
скорости, с которой система способна
при заданных условиях выровнять разность
концентраций.
С
– вектор градиента концентрации
диффундирующих атомов; D
– коэффициент пропорциональности, или
коэффициент диффузии. Коэффициент
диффузии (см2/с) является мерой
скорости, с которой система способна
при заданных условиях выровнять разность
концентраций.
Если глубина диффузии значительно меньше поперечных размеров площади, на которой она происходит, то принимают, что диффузия идет в одном направлении. Одномерное уравнение Фика имеет вид:
![]() ,
(2)
,
(2)
где F(x) –
плотность тока, или число атомов вещества,
переносимых в единицу времени через
единичную площадь;
![]() – градиент концентрации диффундирующей
примеси в направлении диффузии.
– градиент концентрации диффундирующей
примеси в направлении диффузии.
Второй закон Фика определяет скорость накопления растворенной примеси в любой плоскости, перпендикулярной направлению диффузии. Для одномерного случая оно имеет вид:
![]() ,
(3)
,
(3)
где
![]() - изменение концентрации диффундирующего
вещества со временем. Если коэффициент
D считать постоянным (что
справедливо в большинстве практических
случаев диффузии в полупроводниках),
то уравнение (3) имеет вид:
- изменение концентрации диффундирующего
вещества со временем. Если коэффициент
D считать постоянным (что
справедливо в большинстве практических
случаев диффузии в полупроводниках),
то уравнение (3) имеет вид:
![]() .
(4)
.
(4)
Одной из основных величин в уравнении Фика является коэффициент диффузии D. Оно зависит от температуры, энергии связи примесных атомов в решетке полупроводника, плотности вакансий в кристалле, постоянной решетки и других. Влияние этих параметров на величину D описывается соотношением Аррениуса:
![]() ,
(5)
,
(5)
где D0 – константа диффузии, которая в диапазоне 900 – 1200 оС не зависит от температуры (физический смысл величины D0 связан с частотой атомных скачков или с величиной собственных колебаний решетки ≈1013 Гц и величиной скачка атома в примеси), k – постоянная Больцмана, Т – абсолютная температура, Eакт – энергия активации процесса диффузии. Eакт – энергия, необходимая для удаления атома из кристаллической решетки твердого тела. Фактически это энергия элементарного «прыжка» (перемещения) примесного или собственного атома.
В таблице приведены коэффициенты диффузии некоторых элементов в кремнии.
Таблица
Химический элемент |
Множитель D0, см2/с |
D при 1200 оС, см2/с |
∆Е, |
B Al P As Au Cu Fe |
10,0 8,0 10,5 0,32 1,1∙10-3 - 62,0 |
2,8∙10-12 1,5∙10-11 2,8∙10-12 2,7∙10-13 1∙10-6 1∙10-5 1∙10-6 |
340,0 357,0 357,2 345,2 109,0 20,1 108,6 |
Каковы же механизмы перемещения атомов одного вещества в другом? Для полупроводников, в частности Si и Ge они определяются наличием двух видов точечных дефектов – дефектов по Шоттки и дефектов по Френкелю.
Число дефектов резко возрастает с ростом температуры:
![]() ,
(6)
,
(6)
где Eакт – энергия образования вакансий, эВ. При нормальной температуре количество вакансий в кремнии мало и составляет 106 - 107 см2, а при температуре 1000-1200 оС уже 1015 - 1016 см2.
В соответствии с основными видами дефектов различают два основополагающих вида диффузии для реальных кристаллов – междоузельный и вакансионный. Ознакомится с этими механизмами можно с помощью компьютерных программ раздела «Диффузия».
Для некоторых примесных атомов Si для вакансионного механизма Eакт ≈ 3-4 эВ, а для механизма прямого перемещения атомов по междоузлиям Eакт ≈ 0,6-1,2 эВ.
Для практических реализаций диффузионных процессов особый интерес представляют два случая диффузии:
1 – диффузия из бесконечного источника, когда в поверхностные слои твердого тела вводятся примесные атомы, концентрация которых на поверхности остается постоянной в течение всего процесса диффузии. Этот случай характерен для первой стадии диффузии, называемой в производстве ИЭТ «загонкой». Упрощенно, на стадии «загонка», в поверхностные слои вводятся примесные атомы на глубину 0,15-0,8 мкм в зависимости от предельной растворимости примеси в твердом теле при данной температуре.
В этом случае решение второго уравнения диффузии (4) дает следующее соотношение:
 ,
(7)
,
(7)
где С0 – исходная концентрация источника диффузии, z – любой аргумент
![]() ,
,
Интеграл в этом соотношении обычно называется функцией ошибок, следовательно, выражение (7) можно записать в виде:
![]() ,
,
или
![]() ,
(8)
,
(8)
где erfc z известна под названием функции ошибок.
Значения функции
![]() и
табулированы.
и
табулированы.
Количество вещества, проникшее в твердое тело за время диффузии t от начала процесса диффузии из бесконечного источника определяется выражением:
![]() .
(9)
.
(9)
Рассмотренный пример (7) реализуется при проведении глубокой (например, разделительной) диффузии и иногда при диффузии для создания областей эмиттера. Формула (8) позволяет при наличии данных о коэффициенте диффузии определять распределение концентрации вдоль оси X для различных моментов времени. Это распределение представлено на рис. 1. В случае, когда диффузант распространяется в одном направлении (x>0), реализуется только правая ветвь кривой на рис. 1.
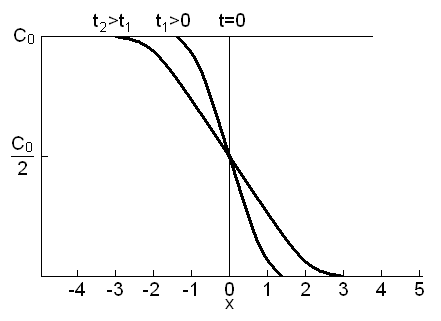
Рис. 1. Распределение примеси из точечного источника
для различного времени диффузии (t1 и t2)
При диффузии в заданную область (x>0) из бесконечного источника (загонка примеси) с постоянной концентрацией С0 распределение концентрации диффузанта вычисляется по уравнению (8). На рис. 2 показано это распределение. Соотношение (8) используется для расчета диффузии в твердый полупроводник из газовой фазы постоянного состава.

Рис. 2. Распределение концентраций примеси за счет диффузии из
бесконечного источника, описываемое дополнительной функцией ошибок.
2 – диффузия из конечного источника. Этот случай соответствует условиям, когда в тонком поверхностном слое полупроводника создана избыточная концентрация примеси С0, а образец подвергается дополнительной высокотемпературной обработке. Избыточная концентрация может быть получена путем диффузии примесей на стадии «загонка» или же, что наиболее распространено на практике, - ионной имплантацией. В этом случае происходит перераспределение примеси из поверхностного слоя в объем твердого тела. Данный этап иногда называется второй стадией диффузии – «разгонкой». Во время процесса «разгонки» количество примесных атомов на поверхности образца будет непрерывно уменьшаться и, одновременно, будет увеличиваться концентрация примеси в слоях, лежащих глубже легированного поверхностного слоя.
Для граничных условий конечного источника решение диффузионного уравнения (4) дает функцию распределения Гаусса. Для одномерного случая оно выглядит так:
![]() ,
(10)
,
(10)
где Q – количество примесей, введенное на этапе «загонка». Графическая интерпретация выражения (10) приведена на рис. 3.
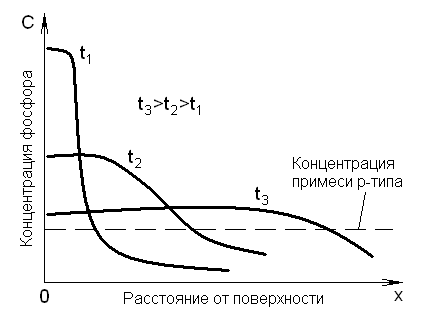
Рис. 3. Влияние времени диффузии на перераспределение примеси фосфора
в Si подложке из конечного источника, описываемое законом Гаусса.
На рис. 4 приведена структура диффузионного n-p-n транзистора, полученного последовательной диффузией фосфора, бора и фосфора в подложку p-типа, и представлены профили концентрации для областей эмиттера, базы и коллектора.
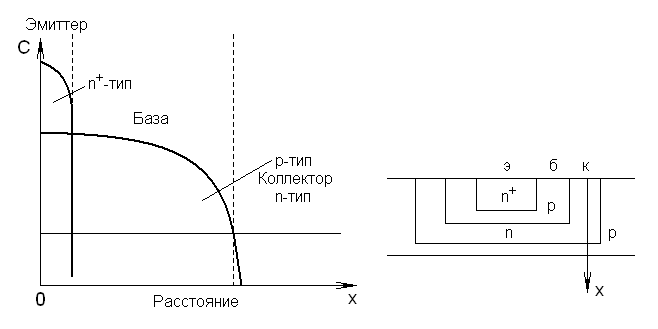
Рис. 4. Профиль концентраций для диффузионных n-p-n структур.
На практике, при формировании элементов ИЭТ, загонку примесей (первый этап диффузии) осуществляют методом ионной имплантации (редко диффузии), а разгонку примесей (второй этап) – методом диффузии из ограниченного источника с целью получения заданных профилей распределение примесей в области активной структуры (рис. 5).
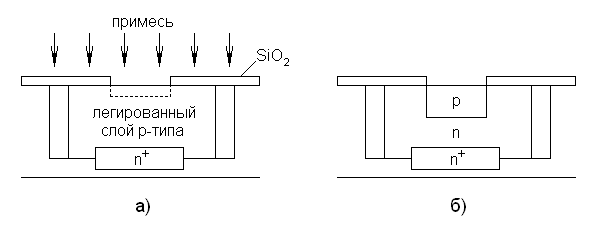
Рис. 5. Этапы формирования p-n-перехода:
а) – загонка примеси методом ионной имплантации или диффузии;
б) – разгонка примеси при термической обработке (диффузия).
Важно отметить, что «разгонка» примесей осуществляется как в инертной, так и в окислительной среде (O2, пары H2O). В случае диффузии в окислительной среде необходимо учитывать перераспределение примесей на границе Si-SiO2. Это явление (перераспределения) называется эффектом сегрегации примесей и характеризуется коэффициентом сегрегации ω. Количественно оно определяется соотношением:
![]() ,
(11)
,
(11)
где CSi и CSiO2 – соответственно равновесные концентрации примесей в Si и SiO2. ω зависит от соотношения коэффициентов диффузии примесей γ, плотности, состава и строения SiO2; соотношение молярных объемов Si, SiO2 и примеси; растворимости примеси в Si и SiO2.
Температурный диапазон реализации диффузионных процессов составляет 950-1250 оС, для Si. Ниже 950 оС значения коэффициентов диффузии очень малы и глубина залегания легированного слоя очень незначительна. Выше 1250-1280 оС качество диффузионных слоев неудовлетворительно.
В зависимости от способа введения в полупроводники диффузанта различают диффузию из газовой (или паровой) фазы, из жидкой фазы и из твердой фазы.
Диффузионные процессы проводят в закрытой или открытой трубе. В первом случае (рис.6,а) пластины полупроводника 1 и источник 2 загружают в кварцевую ампулу 3, которую вакуумируют (до давления 10-4…10-5 мм рт. ст.), герметизируют и помещают в печь 4. Ампулу выдерживают при температуре 900-1300 оС определенное время, в течении которого идет процесс диффузии газообразной примеси на рассчитанную глубину. Недостаток этого метода – низкая производительность и высокая стоимость процесса, т.к. при вскрытии ампула разрушается.
Термин «открытая труба» обусловлен тем, что выходной конец диффузионной трубы сообщается с атмосферой (рис. 6,б-д). Через него в зону диффузии загружают кремниевые пластины 1. Чтобы свести к минимуму загрязнения из атмосферы, над выходом трубы 2 устанавливают вытяжную систему. Во входной конец диффузионной трубы вставляют шлиф для введения газа – носителя 3 – азота или кислорода.

Рис. 6. Способы проведения диффузии.
Диффузант 4 либо наносят на поверхность пластины (рис. 6, б), либо вводят в виде пара или газа в газ – носитель (рис. 6, в). На рис. 6, г показана схема диффузионной печи, применяемой в основном для диффузии из твёрдых источников методом открытой трубы, на рис. 6, д – схема бокс-метода. В последнем случае пластины и источник находятся в полусферическом контейнере 5 однозонной печи.
Наибольшее распространение в промышленности получила диффузия в открытой трубе, проводимая из твёрдых жидких и газообразных источников.
Рассмотрим схему процесса диффузии в потоке газа-носителя с источником жидкого диффузанта, широко используемого в настоящее время.
Для загрузки партии пластин (рис.7) применяют кассеты из кварцевого стекла или кремния. Пластины размещаются поперёк или вдоль оси кассеты и соответственно диффузионной трубы, куда загружаются кассеты с пластинами. При продольном расположении оси снижается турбулентность потока в реакторе.
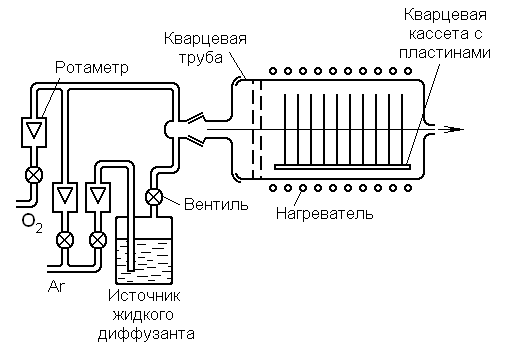
Рис. 7. Схема процесса диффузии в открытой трубе в потоке диффузанта.
Операционный цикл включает следующие переходы:
• так называемая «промывка» реактора аргоном;
• вывод печи на заданный температурный режим (в течение 2-3 ч.);
• загрузка кассеты с пластинами и прогрев её в течение 10 мин. С подачей аргона для удаления десорбирующихся газов;
• подача аргона с парогазовой смесью (диффузант и кислород);
• выдержка в рабочей зоне при постоянной температуре заданное время (собственно диффузия);
• прекращение подачи смеси и извлечение кассеты с пластинами.
Широкое применение получили печи диффузионные однозонные с несколькими трубами, диаметр которых примерно в полтора раза превышает диаметр обрабатываемых пластин. Среди диффузионных систем следует выделить СДО 125-3/015 (диаметр пластин 76 мм), СДОМ (диаметр пластин 100 мм), ОКСИД-ПО (100-150).
Погрешность поддержания температуры в рабочей зоне печи не более 0.5 ºС. Контроль температуры ведётся в нескольких точках (обычно в 3-х точках) платино-платинородиевыми термопарами.
В качестве источника примесей при диффузии используют специальные вещества (чистые или химические соединения), являющиеся источником атомов примеси и называемые диффузантами. По своему агрегатному состоянию диффузанты бывают твёрдые, жидкие и газообразные.
Твёрдые диффузанты. Фосфор. Наиболее
распространенным источником является
безводная пятиокись фосфора (фосфорный
ангидрид) ![]() .
.
помещают в зону источника (рис.6, г) и нагревают до 230-300 ºС. Газ-носитель захватывает молекулы и переносит в зону диффузии. В процессе диффузии между и Si происходит химическая реакция с выделением элементарного P и Si, образующих стекловидное соединение на поверхности пластины, из которого идёт диффузия.
Другими источниками в твёрдой фазе
являются нитрид фосфора ![]() ,
дигидрофосфат аммония
,
дигидрофосфат аммония ![]() ,
гидрофосфат аммония
,
гидрофосфат аммония ![]() .
.
Фосфаты требуют более высоких температур источника (450-400 ºС). Недостатком является непостоянство его состава и связанное с этим изменение давления паров, что даёт невоспроизводимые результаты.
Бор. Самым распространённым источником
в твёрдой фазе для диффузии в открытой
трубе является борный ангидрид ![]() или борная кислота, которая при высокой
температуре дегидратируется с образованием
.
Температура источника составляет около
900 ºС. Обычно
и
или борная кислота, которая при высокой
температуре дегидратируется с образованием
.
Температура источника составляет около
900 ºС. Обычно
и ![]() используют в смеси с
используют в смеси с ![]() ,
т.к. соприкосновение чистого
с кварцем вызывает его расстекловывание.
,
т.к. соприкосновение чистого
с кварцем вызывает его расстекловывание.
Жидкие диффузанты. Фосфор. В качестве
жидких диффузантов используют оксихлорид
фосфора ![]() ,
трихлорид фосфора
,
трихлорид фосфора ![]() и пентафторид фосфора
и пентафторид фосфора ![]() .
Обычно жидкие источники реагируют с
избытком кислорода и образованием
.
Эти диффузанты не гигроскопичны, имеют
малый расход и стабильны по концентрации
фосфора при длительном использовании.
.
Обычно жидкие источники реагируют с
избытком кислорода и образованием
.
Эти диффузанты не гигроскопичны, имеют
малый расход и стабильны по концентрации
фосфора при длительном использовании.
Бор. Наиболее распространён
трёхбромистый бор ![]() .
В газ-носитель добавляют кислород для
окисления
до
и для защиты поверхности от образования
чёрных нерастворимых отложений.
.
В газ-носитель добавляют кислород для
окисления
до
и для защиты поверхности от образования
чёрных нерастворимых отложений.
Газообразные диффузанты. Фосфор. Для
диффузии фосфора в открытой трубе обычно
используют фосфин ![]() .
Механизм диффузии из
такой же, как и механизм диффузии из
.
Недостатком
является его высокая токсичность.
.
Механизм диффузии из
такой же, как и механизм диффузии из
.
Недостатком
является его высокая токсичность.
Бор. В качестве газообразных
источников бора используют трёххлористый
бор ![]() и диборан
и диборан ![]() .
в нейтральной и восстановительной
атмосфере образует с кремнием летучие
соединения и выделяет В. При добавлении
в поток
кислорода образуется борный ангидрид.
Диборан используют в нейтральной,
восстановительной и окислительной
атмосфере. Пиролиз
происходит при Т > 300 ºC.
Лучшей воспроизводимостью обладают
системы с окислительной средой, содержащей
до 0,01%
и до 2,5%
.
в нейтральной и восстановительной
атмосфере образует с кремнием летучие
соединения и выделяет В. При добавлении
в поток
кислорода образуется борный ангидрид.
Диборан используют в нейтральной,
восстановительной и окислительной
атмосфере. Пиролиз
происходит при Т > 300 ºC.
Лучшей воспроизводимостью обладают
системы с окислительной средой, содержащей
до 0,01%
и до 2,5% ![]() в аргоне или азоте. Диборан взаимодействует
с кислородом, образуя и воду:
в аргоне или азоте. Диборан взаимодействует
с кислородом, образуя и воду:
B2H6 + 3O2 = B2O3 + 3H2O
Недостатком являются токсичность, лёгкая воспламеняемость на воздухе при концентрации более 0,8%, взрыв при соприкосновении с хлором.
В диффузионных структурах обычно контролируют глубину залегания p-n-перехода, поверхностную концентрацию, характер распределения диффундирующей примеси и значение градиента концентрации примеси в области p-n-перехода.
Для выявления диффузионных p-n-переходов
пользуются методом косого шлифа
(рис.8,а), т.е. кристалл, содержащий
p-n-переход,
сошлифовывают под небольшим углом
(1-5º). При этом наблюдаемый диффузионный
слой заметно расширяется. Границу
диффузионной области выявляют при
помощи метода селективного окрашивания
специальными травителями. Глубина
залегания ![]() в этом случае определяется по формуле
в этом случае определяется по формуле
![]() ,
(12)
,
(12)
где h – ширина p-n-перехода при заданной величине угла сошлифовывания α.
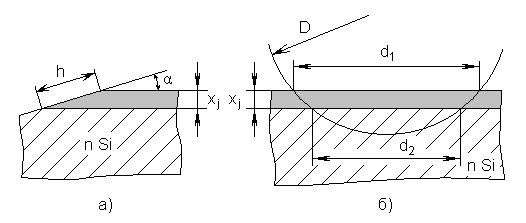
Рис.8. Методы контроля глубины залегания диффузионных слоёв с помощью
косого (а) и сферического (б) шлифов.
Более точные результаты получают при использовании сферического шлифа (рис. 8,б). В этом случае
![]() ,
,
где ![]() – диаметр лунки;
– диаметр лунки; ![]() - диаметр нижней границы p-n-перехода;
D – диаметр шара (30…150мм).
- диаметр нижней границы p-n-перехода;
D – диаметр шара (30…150мм).
Диффузионный слой можно аппроксимировать последовательностью элементарных слоёв с различной, но постоянной в их пределах концентрацией примеси. Проводимость вдоль диффузионного слоя является суммой проводимостей элементарных слоёв. Измерив 4-зондовым методом поверхностную проводимость σSO, удалив элементарный слой толщиной ∆ и вновь измерив поверхностную проводимость σS, среднюю концентрацию свободных носителей заряда в удалённом слое, можно рассчитать по формулам:
![]() ,
,
![]() ,
(13)
,
(13)
где I – ток через образец;
U0, U
- значения напряжения на потенциальных
зондах; μ- средняя подвижность носителей
заряда. Подвижность μ является функцией
концентрации примеси. Поэтому (13) лучше
решать не относительно С, а относительно
произведения ![]() и значения
и значения ![]() вычислять по кривой .
вычислять по кривой .
Определение градиента концентрации примеси определяют путём измерения ёмкости p-n-перехода. При достаточно малых обратных смещениях, когда ширина перехода невелика, распределение примеси в нём с удовлетворительной точностью можно считать линейным. Ёмкость плавного перехода на единицу площади определяется по формуле
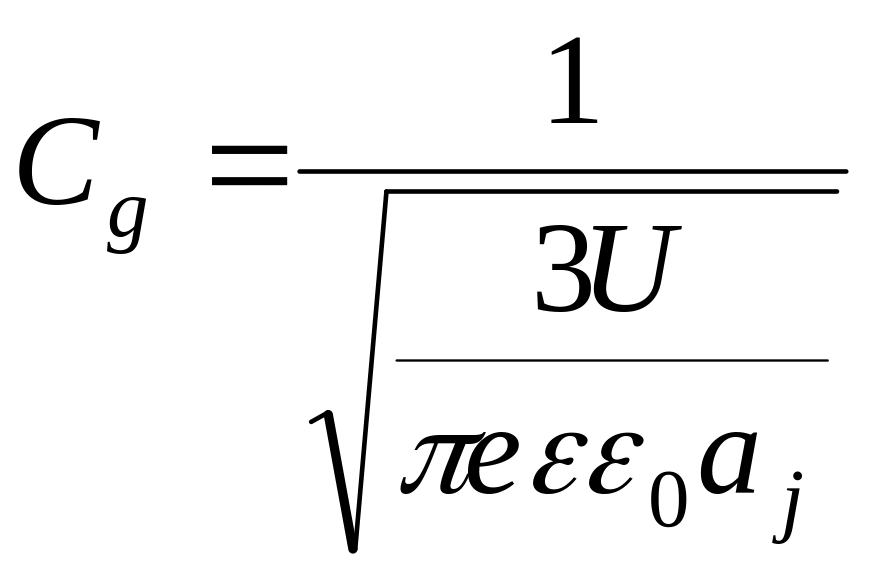 ,
(14)
,
(14)
Отсюда градиент концентрации
![]() ,
(15)
,
(15)
где k= 24/![]() .
Измерив ёмкость при данном напряжении,
можно оценить градиент концентрации
примеси.
.
Измерив ёмкость при данном напряжении,
можно оценить градиент концентрации
примеси.
