
- •Тема 2 молекулярна фізика та термодинаміка
- •1. Основні означення та поняття молекулярно – кінетичної теорії.
- •2. Основні положення молекулярно – кінетичної теорії.
- •3.Тиск газу. Основне рівняння мкт газів.
- •4. Температура.
- •5. Швидкості газових молекул та їх вимірювання.
- •6. Поняття про статистичний розподіл.
- •7. Барометрична формула. Розподіл Максвела - Больцмана.
7. Барометрична формула. Розподіл Максвела - Больцмана.
Рівняння, що дає змогу визначити зміну тиску повітря з висотою, називають барометричною формулою. Вперше вона отримана в 1821р. П.Лапласом.
Розглянемо вертикальний стовп повітря, в якому немає зовнішніх потоків та турбулентності. Тиск повітря на будь-якій висоті зумовлений дією сили тяжіння. З підняттям на dh тиск відповідно зменшиться на dp. Оскільки густину в тонкому шарі можна вважати сталою,
![]()
g - прискорення вільного падіння.
Оскільки
![]() ,
,
m0 – маса молекули,
n0 – концентрація молекул.
З основного рівняння
МКТ
![]() . Отже
. Отже
![]()
Розв’яжемо диференційне рівняння:
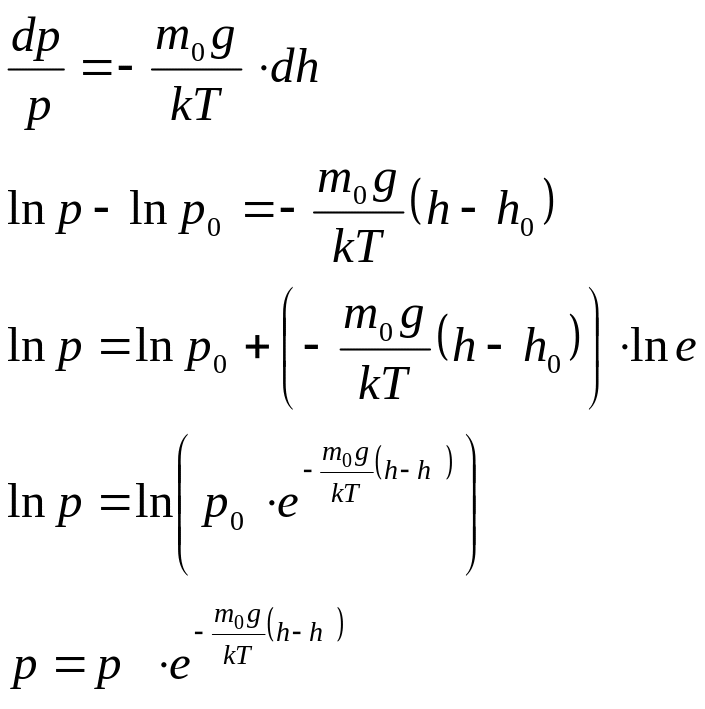
В рахувавши,
що
рахувавши,
що
![]() , отримаємо барометричну формулу
, отримаємо барометричну формулу
![]()
З барометричної формули легко встановити розподіл молекул газу з висотою в полі тяжіння
![]() або
або
![]() (4)
(4)
Л.Больцман показав, що такий закон розподілу частинок справедливий для будь-якого потенціального поля. Тому закон (4) називається розподілом Больцмана і є одним із основних законів МКТ.
Контрольні питання
Дайте визначення поняттям „молекулярна маса”, „молярна маса”, „діаметр молекули”.
Назвіть основні положення МКТ та обґрунтуйте їх.
За яких умов газ оказує тиск? Запишіть основне рівняння МКТ газів.
Дайте визначення абсолютній температурі. Що таке „абсолютний ноль”?
Які висновки зроблено за дослідом Штерна?
Чому неможна говорити про середню швидкість однієї молекули??
Чи можна говорити про тиск або температуру одніїє молекули? Кількох молекул? Чому?
Проаналізуйте розмоділ Максвелла? Зробіть висновки.
Які обмеження має барометрична формула? За яких умов вона справедлива?
Література
И.В. Савельев, Курс физики, т.І, "Наука", М., 1989, § 93 -100
І.М.Кучерук, І.Т.Горбачук, П.П.Луцик, Загальний курс фізики,т.І, „Техніка”, К, 2006, § 14. 1 -14.11
