
- •2. Витамин b1 (тиамин, антиневритный)
- •3. Витамин в2 (рибофлавин, витамин роста)
- •4. Витамин в3 (пантотеновая кислота, антидерматитный)
- •5. Витамин b5 (витамин pp, никотиновая кислота, ниацин, никотинамид, антипеллагрический)
- •6. Витамин в6 (пиридоксин, антидерматитный)
- •7. Витамин b9 (фолиевая кислота, вc)
- •8. Витамин в12 (кобаламин, антианемический витамин)
- •9. Витамин “н” (биотин, коэнзим r, антисеборейный)
- •10. Витамин “с”(аскорбиновая кислота, антицинготный, антискорбутный)
- •13. Отличия катаболизма от анаболизма:
- •Уровни взаимосвязи между ката– и анаболизмом.
- •16. Реакции и процессы, сопряженные с гидролизом атф, в клетках животных и растений:
- •17. Механизмы образования атф в клетках животных и растений:
- •Основные положения хемиосмотической теории Митчелла:
- •20. Цикл Кребса – центральный метаболический путь.
- •Витамины, принимающие участие в работе цикла:
- •23. Катаболическая функция цикла Кребса:
6. Витамин в6 (пиридоксин, антидерматитный)
Химическая природа: производное 3-оксипиридина. Производные отличаются природой замещающей группы в положении 4 пиридинового ядра.
Коферментные формы: пиридоксальфосфат, пиридоксамин.
Участие в метаболизме:
а) играет ключевую роль в азотистом обмене
б)B6 в форме пиридоксальфосфата является простетической группой аминотрансфераз (катализируют обратимый перенос аминогруппы от АК на α-кетокислоту) и декарбоксилаз АК (осуществляет необратимое отщепление CO2 от карбоксильной группы АК с образованием биогенных аминов)
в)необходим для некоторых реакций обмена аминокислот (неокислительное дезаминирование серина и треонина, окисление триптофана)
г)участвует в реакциях синтеза гема гемоглобина (синтез δ-аминолевулиновой кислоты – предшественницы гема).
Суточная потребность взрослого человека: 0.15-0.20 мг.
7. Витамин b9 (фолиевая кислота, вc)
Химическая природа: 3 структурных единицы – остаток птеридина, ПАБК (парааминобензойная кислота) и глутаминовая кислота.
![]()
Коферментная форма: тетрагидрофолиевая кислота (ТГФК)
Участие в метаболизме:
а)ТГФК является коферментом ферментов, переносящих одноуглеродные радикалы (формильную –СНО, метильную –СН3, метиленовую –СН2-, метенильную –СН=, оксиметильную –СН2ОН, формиминогруппу –СН=NН).
б) переносит одноуглеродистые фрагменты при биосинтезе метионина и тимина, серина, образовании пуриновых нуклеотидов и т.д.
Суточная потребность: 0.2 - 0.4 мг.
8. Витамин в12 (кобаламин, антианемический витамин)
Формула - стр.158 учебника Коровкина или стр.168 учебника Николаева.
Химическая структура – порфириноподобное корриновое ядро, содержащее центральный атом кобальта, соединенный с атомами азота четырех восстановленных пиррольных колец и с атомом азота 5,6-диметилбензимидазола.
Коферментные формы: метилкобаламин (CH3-B12), дезоксиаденозилкобаламин (дАВ12)
Участие в метаболизме: а) реакции трансметилирования – метилкобаламин выполняет роль промежуточного переносчика метильной группы (синтез метионина и ацетата)
б) перенос водорода в реакциях изомеризации (глутаматмутазная реакция – взаимопревращения глутаминовой и β-метиласпарагиновой кислот и т.д.)
в) предполагается участие в реакциях трансметилирования и дезаминирования
Суточная потребность: 2.5-5 мкг.
9. Витамин “н” (биотин, коэнзим r, антисеборейный)
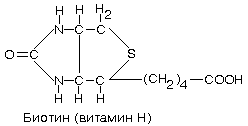
Коферментные формы: остаток биотина, связанный с -аминогруппой остатка лизина (биоцитин).
Участие в метаболизме: биотиновые ферменты катализируют два основных типа реакций:
а) реакции декарбоксилирования (с участием CO2 или HCO3-), сопряженные с распадом АТФ. Пример: ацетил-КоА и пируваткарбоксилазные реакции.
б) реакции транскарбоксилирования (без участия АТФ) – обмен карбоксильной группой между субстратами. Пример: обратимое превращение пировиноградной и щавелевоуксусной кислот.
в) имеют важное значение в синтезе ВЖК, белков, пуриновых нуклеотидов.
