
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При
переходе из начального в конечное
состояние объем газа увеличился, газ
совершил работу А.
Выполняется первый закон термодинамики.
Переданное газу количество теплотыQ равно
сумме изменения внутренней энергии
газа |
|
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через давление и объем газа. Работа А при переходе газа из состояния 1 в состояние 3 площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Положительное значение величины Q означает, что газ получил количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
|
1 |
При переходе из начального в конечное состояние объем газа уменьшился, внешние силы над газом совершили работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно разности изменения внутренней энергии газа и работы А, совершенной над газом. |
|
1 |
|
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа Апри переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V). |
. . |
1 |
|
3 |
Получение правильного численного значения количества теплоты. Отрицательное значение величины Q означает, что газ отдал количество теплоты Q. |
|
1 |
|
|
Максимальный балл |
3 |
||
С3
На диаграмме (см. рисунок) представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа уменьшился, внешние силы над газом совершили работу А'. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно разности изменения внутренней энергии газа и работы А', совершенной над газом. |
|
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А' при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Отрицательное значение величины Q означает, что газ отдал количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме (см. рисунок) представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа уменьшился, внешние силы над газом совершили работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно разности изменения внутренней энергии газа и работы А, совершенной над газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Отрицательное значение величины Q означает, что газ отдал количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме (см. рисунок) представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа увеличился, газ совершил работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно сумме изменения внутренней энергии газа и работы А, совершенной газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Положительное значение величины Q означает, что газ газ получил количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа увеличился, газ совершил работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно сумме изменения внутренней энергии газа и работы А, совершенной газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Положительное значение величины Q означает, что газ газ получил количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа увеличился, газ совершил работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно сумме изменения внутренней энергии газа и работы А, совершенной газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Положительное значение величины Q означает, что газ газ получил количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа уменьшился, внешние силы над газом совершили работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно разности изменения внутренней энергии газа и работы А, совершенной над газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Отрицательное значение величины Q означает, что газ отдал количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены измениния давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа уменьшился, внешние силы над газом совершили работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно разности изменения внутренней энергии газа и работы А, совершенной над газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Отрицательное значение величины Q означает, что газ отдал количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание С3
На диаграмме представлены изменения давления и объема идеального одноатомного газа. Какое количество теплоты было получено или отдано газом при переходе из состояния 1 в состояние 3?

Решение.
№ этапа |
Содержание этапа решения |
Чертёж, график, формула |
Оценка этапа в баллах |
1 |
При переходе из начального в конечное состояние объем газа увеличился, газ совершил работу А. Выполняется первый закон термодинамики. Переданное газу количество теплоты Q равно сумме изменения внутренней энергии газа и работы А, совершенной газом. |
; |
1 |
2 |
Внутренняя энергия идеального газа в состояниях 1 и 3 выражается через значения давления и объема газа. Работа А при переходе газа из состояния 1 в состояние 3 равна площади под графиком диаграммы в единицах (р, V): |
|
1 |
3 |
Получение правильного численного значения количества теплоты. Положительное значение величины Q означает, что газ газ получил количество теплоты Q. |
|
1 |
|
Максимальный балл |
3 |
|
Задание с3
В
цилиндр объемом ![]() насосом
закачивается воздух со скоростью
насосом
закачивается воздух со скоростью ![]() .
В верхнем торце цилиндра есть отверстие,
закрытое предохранительным клапаном.
Клапан удерживается в закрытом состоянии
стержнем, который может свободно
поворачиваться вокруг оси в точке А (см.
рисунок).
.
В верхнем торце цилиндра есть отверстие,
закрытое предохранительным клапаном.
Клапан удерживается в закрытом состоянии
стержнем, который может свободно
поворачиваться вокруг оси в точке А (см.
рисунок).
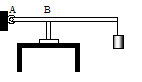
К
свободному концу стержня подвешен груз
массой 2 кг. Клапан открывается через
580 с работы насоса, если в начальный
момент времени давление воздуха в
цилиндре было равно атмосферному.
Площадь закрытого клапаном отверстия ![]() ,
расстояние АВ равно
0,1 м. Температура воздуха в цилиндре
и снаружи не меняется и равна 300 К.
Определите длину стержня, если его можно
считать невесомым.
,
расстояние АВ равно
0,1 м. Температура воздуха в цилиндре
и снаружи не меняется и равна 300 К.
Определите длину стержня, если его можно
считать невесомым.
Решение.
Клапан
откроется, когда избыточная сила F давления
воздуха на клапан изнутри цилиндра
сравняется с силой давления стержня на
этот клапан. Если превышение давления
воздуха в цилиндре над атмосферным ![]() ,
а площадь клапана s,
то
,
а площадь клапана s,
то
![]() .
.
Сила
действия стержня на клапан равна ![]() ,
где m, L и l соответственно
масса груза, длина стержня и длина его
участка АВ.
Итак, должно выполняться условие
,
где m, L и l соответственно
масса груза, длина стержня и длина его
участка АВ.
Итак, должно выполняться условие
![]() .
.
Дополнительное
давление воздуха определяется увеличением
массы ![]() воздуха
в цилиндре. Согласно уравнению
Клапейрона–Менделеева,
воздуха
в цилиндре. Согласно уравнению
Клапейрона–Менделеева,
![]() ,
,
где M — молярная масса воздуха. Поэтому условие открытия клапана имеет вид:
![]() ,
или
,
или ![]() .
.
Если
насос закачивает каждую секунду ![]() кг
воздуха, то массу
он
закачает в цилиндр за время t.
Следовательно, клапан откроется в
момент, когда выполнится равенство
кг
воздуха, то массу
он
закачает в цилиндр за время t.
Следовательно, клапан откроется в
момент, когда выполнится равенство
![]() .
.
Ответ: ![]() .
.
Задание с3
В цилиндр объемом насосом закачивается воздух со скоростью . В верхнем торце цилиндра есть отверстие, закрытое предохранительным клапаном. Клапан удерживается в закрытом состоянии стержнем, который может свободно поворачиваться вокруг оси в точке А (см. рисунок).
К свободному концу стержня длиной 0,5 м подвешен груз массой 2 кг. Клапан открывается через 580 с работы насоса, если в начальный момент времени давление воздуха в цилиндре было равно атмосферному. Площадь закрытого клапаном отверстия . Температура воздуха в цилиндре и снаружи не меняется и равна 300 К. Определите длину AB.
Решение.
Клапан откроется, когда избыточная сила F давления воздуха на клапан изнутри цилиндра сравняется с силой давления стержня на этот клапан. Если превышение давления воздуха в цилиндре над атмосферным , а площадь клапана s, то
.
Сила действия стержня на клапан равна , где m, L и l соответственно масса груза, длина стержня и длина его участка АВ. Итак, должно выполняться условие
.
Дополнительное давление воздуха определяется увеличением массы воздуха в цилиндре. Согласно уравнению Клапейрона–Менделеева,
,
где M — молярная масса воздуха. Поэтому условие открытия клапана имеет вид:
,
или ![]() .
.
Если
насос закачивает каждую секунду
кг
воздуха, то за время ![]() он
закачает в цилиндр массу
он
закачает в цилиндр массу ![]() .
Следовательно, клапан откроется в
момент, когда выполнится равенство
.
Следовательно, клапан откроется в
момент, когда выполнится равенство
![]() .
.
Ответ: ![]() .
.
Задание С3
С
разреженным азотом, который находится
в сосуде под поршнем, провели два опыта.
В первом опыте газу сообщили, закрепив
поршень, количество теплоты ![]() ,
в результате чего его температура
изменилась на некоторую величину
,
в результате чего его температура
изменилась на некоторую величину ![]() .
Во втором опыте, предоставив азоту
возможность изобарно расширяться,
сообщили ему количество теплоты
.
Во втором опыте, предоставив азоту
возможность изобарно расширяться,
сообщили ему количество теплоты ![]() ,
в результате чего его температура
изменилась также на
.
Каким было изменение температуры в
опытах? Масса азота
,
в результате чего его температура
изменилась также на
.
Каким было изменение температуры в
опытах? Масса азота ![]() .
.
Решение.
Согласно первому началу термодинамики,
![]() (1)
(1)
![]() (2).
(2).
Где — приращение внутренней энергии газа (одинаковое в двух опытах), A — работа газа во втором опыте.
![]() .
.
Работа A совершалась газом в ходе изобарного расширения, так что
![]() (3),
(3),
(![]() —
изменение объема газа).
С помощью
уравнения Клапейрона-Менделеева эту
работу можно выразить через приращение
температуры газа:
—
изменение объема газа).
С помощью
уравнения Клапейрона-Менделеева эту
работу можно выразить через приращение
температуры газа:
![]() .
.
Получаем
![]() .
.
Ответ: ![]() .
ПРИМЕЧАНИЕ:
Существует
более короткое решение, однако для него
требуется знание формулы для изменения
внутренней энергии двухатомного газа:
.
ПРИМЕЧАНИЕ:
Существует
более короткое решение, однако для него
требуется знание формулы для изменения
внутренней энергии двухатомного газа: ![]() .
В этой формуле стоит 5/2 вместо привычных
3/2, это отражает тот факт, что у двухатомных
молекул 5 степеней свободы (два вращения
+ три поступательных движения) в отличие
от одноатомных молекул, у которых есть
только три поступательных движения.
(Замечание: для многоатомных молекул
(состоящих из трех и более атомов)
справедлива формула
.
В этой формуле стоит 5/2 вместо привычных
3/2, это отражает тот факт, что у двухатомных
молекул 5 степеней свободы (два вращения
+ три поступательных движения) в отличие
от одноатомных молекул, у которых есть
только три поступательных движения.
(Замечание: для многоатомных молекул
(состоящих из трех и более атомов)
справедлива формула ![]() ,
так как для них есть шесть степеней
свободы: три вращения + три поступательных
движения).
Рассмотрим первый
опыт. Согласно первому началу термодинамики,
все переданное газу тепло идет на
изменение его внутренней энергии,
поскольку поршень фиксирован, и газ не
может совершать работу:
,
так как для них есть шесть степеней
свободы: три вращения + три поступательных
движения).
Рассмотрим первый
опыт. Согласно первому началу термодинамики,
все переданное газу тепло идет на
изменение его внутренней энергии,
поскольку поршень фиксирован, и газ не
может совершать работу:
![]() .
Отсюда сразу находим изменение температуры
азота:
.
Отсюда сразу находим изменение температуры
азота:
![]() Обратите
внимание, что данные задачи избыточны,
в этом способе решения нам вообще не
потребовались данные о втором опыте.
Обратите
внимание, что данные задачи избыточны,
в этом способе решения нам вообще не
потребовались данные о втором опыте.
Задание С3
С разреженным азотом, который находится в сосуде под поршнем, провели два опыта. В первом опыте газу сообщили, закрепив поршень, количество теплоты , в результате чего его температура изменилась на 1 К. Во втором опыте, предоставив азоту возможность изобарно расширяться, сообщили ему количество теплоты , в результате чего его температура изменилась также на 1 К. Определите массу азота в опытах.
Решение.
Согласно первому началу термодинамики,
(1)
(2).
Где — приращение внутренней энергии газа (одинаковое в двух опытах), A — работа газа во втором опыте. Работа A совершалась газом в ходе изобарного расширения, так что
(3),
( — изменение объема газа). С помощью уравнения Клапейрона-Менделеева эту работу можно выразить через приращение температуры газа:
(4).
Решая систему уравнений (1)—(4), будем иметь
![]() .
.
Ответ: ![]() .
ПРИМЕЧАНИЕ:
Существует
более короткое решение, однако для него
требуется знание формулы для изменения
внутренней энергии двухатомного газа:
.
В этой формуле стоит 5/2 вместо привычных
3/2, это отражает тот факт, что у двухатомных
молекул 5 степеней свободы (два вращения
+ три поступательных движения) в отличие
от одноатомных молекул, у которых есть
только три поступательных движения.
(Замечание: для многоатомных молекул
(состоящих из трех и более атомов)
справедлива формула
,
так как для них есть шесть степеней
свободы: три вращения + три поступательных
движения).
Рассмотрим первый
опыт. Согласно первому началу термодинамики,
все переданное газу тепло идет на
изменение его внутренней энергии,
поскольку поршень фиксирован, и газ не
может совершать работу:
.
Отсюда сразу находим массу
азота:
.
ПРИМЕЧАНИЕ:
Существует
более короткое решение, однако для него
требуется знание формулы для изменения
внутренней энергии двухатомного газа:
.
В этой формуле стоит 5/2 вместо привычных
3/2, это отражает тот факт, что у двухатомных
молекул 5 степеней свободы (два вращения
+ три поступательных движения) в отличие
от одноатомных молекул, у которых есть
только три поступательных движения.
(Замечание: для многоатомных молекул
(состоящих из трех и более атомов)
справедлива формула
,
так как для них есть шесть степеней
свободы: три вращения + три поступательных
движения).
Рассмотрим первый
опыт. Согласно первому началу термодинамики,
все переданное газу тепло идет на
изменение его внутренней энергии,
поскольку поршень фиксирован, и газ не
может совершать работу:
.
Отсюда сразу находим массу
азота:
![]() Обратите
внимание, что данные задачи избыточны,
в этом способе решения нам вообще не
потребовались данные о втором опыте.
Обратите
внимание, что данные задачи избыточны,
в этом способе решения нам вообще не
потребовались данные о втором опыте.
Задание С3
Сферическую
оболочку воздушного шара делают из
материала, квадратный метр которого
имеет массу 2 кг. Шар наполняют гелием
при атмосферном давлении ![]() Па.
Определите минимальную массу оболочки,
при которой шар начнет поднимать сам
себя. Температура гелия и окружающего
воздуха одинакова и равна
Па.
Определите минимальную массу оболочки,
при которой шар начнет поднимать сам
себя. Температура гелия и окружающего
воздуха одинакова и равна ![]() .
(Площадь сферы
.
(Площадь сферы ![]() ,
объем шара
,
объем шара ![]() .)
.)
Решение.
II
закон Ньютона в проекциях на
вертикаль: ![]() .
Силы
выражены через радиус r:
.
Силы
выражены через радиус r:
![]()
![]()
откуда
радиус: ![]() ,
где
,
где ![]() —
отношение массы оболочки к ее площади.
Плотности гелия и воздуха:
—
отношение массы оболочки к ее площади.
Плотности гелия и воздуха:
![]() ,
, ![]() ,
, ![]() .
.
Радиус
оболочки: ![]() ,
её масса:
,
её масса: ![]() .
Ответ:
.
Ответ: ![]() .
.
Задание С3
Сферическую
оболочку воздушного шара наполняют
гелием при атмосферном давлении ![]() .
Минимальная масса оболочки, при которой
шар начинает поднимать сам себя, равна
500 кг. Температура гелия и окружающего
воздуха одинакова и равна
.
Чему равна масса одного квадратного
метра материала оболочки шара? (Площадь
сферы
,
объем шара
.)
.
Минимальная масса оболочки, при которой
шар начинает поднимать сам себя, равна
500 кг. Температура гелия и окружающего
воздуха одинакова и равна
.
Чему равна масса одного квадратного
метра материала оболочки шара? (Площадь
сферы
,
объем шара
.)
Решение.
II закон Ньютона в проекциях на вертикаль: . Силы выражены через радиус r:
откуда радиус: , где b — отношение массы оболочки к ее площади. Плотности гелия и воздуха:
, , .
Радиус
оболочки: ![]() ,
её масса:
,
её масса: ![]() .
Отсюда:
.
Отсюда:  .
Ответ:
.
Ответ: ![]() .
.
Задание С3
В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 8 раз, давление воздуха в сосуде увеличилось в 2 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
Решение.
Внутренняя
энергия газа пропорциональна его
температуре и количеству вещества
(газа) в сосуде: ![]() .
Согласно уравнению Клапейрона–Менделеева,
.
Согласно уравнению Клапейрона–Менделеева, ![]() .
Следовательно,
.
Следовательно, ![]() .
Согласно условию задачи, p возросло
в 2 раза, а V уменьшилось
в 8 раз. Следовательно, U уменьшилась
в 4 раза.
Ответ: внутренняя
энергия воздуха в сосуде уменьшилась
в 4 раза.
.
Согласно условию задачи, p возросло
в 2 раза, а V уменьшилось
в 8 раз. Следовательно, U уменьшилась
в 4 раза.
Ответ: внутренняя
энергия воздуха в сосуде уменьшилась
в 4 раза.
Задание С3
В сосуде с небольшой трещиной находится воздух. Воздух может медленно просачиваться сквозь трещину. Во время опыта объем сосуда уменьшили в 4 раза, давление воздуха в сосуде увеличилось тоже в 4 раза, а его абсолютная температура увеличилась в 1,5 раза. Каково изменение внутренней энергии воздуха в сосуде? (Воздух считать идеальным газом.)
Решение.
Внутренняя энергия газа пропорциональна его температуре и количеству вещества (газа) в сосуде: . Согласно уравнению Клапейрона–Менделеева, . Следовательно, . Согласно условию задачи, p возросло в 4 раза, а V уменьшилось в 4 раз. Следовательно, U не изменилось. Ответ: внутренняя энергия воздуха в сосуде не изменилась.
Задание С3
Воздушный
шар имеет газонепроницаемую оболочку
массой 400 кг и наполнен гелием. Какова
масса гелия в шаре, если на высоте, где
температура воздуха ![]() ,
а давление
Па,
шар может удерживать в воздухе груз
массой 225 кг? Считать, что оболочка
шара не оказывает сопротивления изменению
объема шара.
,
а давление
Па,
шар может удерживать в воздухе груз
массой 225 кг? Считать, что оболочка
шара не оказывает сопротивления изменению
объема шара.
Решение.
Шар с грузом удерживается в равновесии при условии, что сумма сил, действующих на него, равна нулю. В проекциях на вертикальную ось это дает:
![]() ,
,
где M и m —
массы оболочки шара и груза, ![]() —
масса гелия, a
—
масса гелия, a ![]() —
сила Архимеда, действующая на шар. Из
условия равновесия следует:
—
сила Архимеда, действующая на шар. Из
условия равновесия следует: ![]() .
Давление p гелия
и его температура T равны
давлению и температуре окружающего
воздуха. Следовательно, согласно
уравнению Клапейрона–Менделеева,
.
Давление p гелия
и его температура T равны
давлению и температуре окружающего
воздуха. Следовательно, согласно
уравнению Клапейрона–Менделеева, ![]() ,
где
,
где ![]() —
молярная масса гелия,
—
молярная масса гелия, ![]() —
средняя молярная масса воздуха,
—
средняя молярная масса воздуха, ![]() —
объем шара. Отсюда
—
объем шара. Отсюда
![]() ;
; ![]() ;
; ![]() .
.
Следовательно, ![]() .
Ответ:
.
.
Ответ:
.
Задание С3
Воздушный шар имеет газонепроницаемую оболочку массой 400 кг и содержит 100 кг гелия. Какой груз он может удерживать в воздухе на высоте, где температура воздуха , а давление Па? Считать, что оболочка шара не оказывает сопротивления изменению объема шара.
Решение.
Шар с грузом удерживается в равновесии при условии, что сумма сил, действующих на него, равна нулю. В проекциях на вертикальную ось это дает:
,
где M и m — массы оболочки шара и груза, — масса гелия, a — сила Архимеда, действующая на шар. Из условия равновесия следует: . Давление p гелия и его температура T равны давлению и температуре окружающего воздуха. Следовательно, согласно уравнению Клапейрона–Менделеева,
,
где — молярная масса гелия, — средняя молярная масса воздуха, — объем шара. Отсюда
; ; .
Следовательно, ![]() .
Ответ:
.
Ответ: ![]() .
.
Задание С3
Вертикально, расположенный замкнутый цилиндрический сосуд высотой 50 см разделен подвижным поршнем весом 110 Н на две части, в каждой из которых содержится одинаковое количество идеального газа при температуре 361 К.
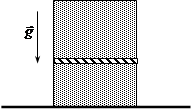
Сколько молей газа находится в каждой части цилиндра, если поршень находится на высоте 20 см от дна сосуда? Толщиной поршня пренебречь.
Решение.
Уравнения
состояния газа верхней и нижней
частей: ![]() ,
, ![]() (1).
Где
(1).
Где ![]() и
и ![]() —
объемы верхней и нижней частей.
Объемы:
—
объемы верхней и нижней частей.
Объемы: ![]() ,
, ![]() ,
где S —
сечение поршня, Н —
высота сосуда, h —
высота, на которой находится поршень.
Условие равновесия поршня
,
где S —
сечение поршня, Н —
высота сосуда, h —
высота, на которой находится поршень.
Условие равновесия поршня ![]() (2),
где Р —
вес поршня.
Подставляя выражения
(1) в (2), получим для количества молей
газа
(2),
где Р —
вес поршня.
Подставляя выражения
(1) в (2), получим для количества молей
газа
![]() .
.
Ответ: ![]() .
.
С3
Воздушный
шар, оболочка которого имеет массу ![]() и
объем
и
объем ![]() ,
наполняется горячим воздухом при
нормальном атмосферном давлении и
температуре окружающего воздуха
,
наполняется горячим воздухом при
нормальном атмосферном давлении и
температуре окружающего воздуха ![]() C.
C.

Какую минимальную температуру t должен иметь воздух внутри оболочки, чтобы шар начал подниматься? Оболочка шара нерастяжима и имеет в нижней части небольшое отверстие.
Решение.
Условие
подъема шара: ![]() ,
где М —
масса оболочки, m —
масса воздуха внутри оболочки, отсюда
,
где М —
масса оболочки, m —
масса воздуха внутри оболочки, отсюда ![]() ,
где
,
где ![]() —
плотность окружающего воздуха,
—
плотность окружающего воздуха, ![]() —
плотность воздуха внутри оболочки,V —
объем шара. Для воздуха внутри шара:
—
плотность воздуха внутри оболочки,V —
объем шара. Для воздуха внутри шара: ![]() ,
или
,
или ![]() ,
где р —
атмосферное давление, Т —
температура воздуха внутри шара.
Соответственно, плотность воздуха
снаружи:
,
где р —
атмосферное давление, Т —
температура воздуха внутри шара.
Соответственно, плотность воздуха
снаружи: ![]() ,
где T_0 —
температура окружающего воздуха.
,
где T_0 —
температура окружающего воздуха.
![]()
![]() .
.
Ответ: ![]() .
.
Задание С3
В горизонтальной трубке постоянного сечения, запаянной с одного конца, помещен столбик ртути длиной 15 см, который отделяет воздух в трубке от атмосферы. Трубку расположили вертикально запаянным концом вниз и нагрели на 60 К. При этом объем, занимаемый воздухом, не изменился. Давление атмосферы в лаборатории — 750 мм рт. ст. Какова температура воздуха в лаборатории?
Решение.
Условие
механического равновесия столбика
ртути определяет давление воздуха в
вертикальной трубке: ![]() ,
где
,
где ![]() —
давление атмосферы. Здесь
—
давление атмосферы. Здесь ![]() .
Поскольку нагревание воздуха в трубке
происходит до температуры Т и
первоначального объема, то по уравнению
Клапейрона–Менделеева:
.
Поскольку нагревание воздуха в трубке
происходит до температуры Т и
первоначального объема, то по уравнению
Клапейрона–Менделеева:
![]() ,
, ![]() .
.
Отсюда ![]() .
Ответ:
.
Ответ: ![]() .
.
Задание С3
В
калориметре находился 1 кг льда. Чему
равна первоначальная температура льда,
если после добавления в калориметр 15 г
воды, имеющей температуру ![]() ,
в калориметре установилось тепловое
равновесие при
,
в калориметре установилось тепловое
равновесие при ![]() ?
Теплообменом с окружающей средой и
теплоемкостью калориметра пренебречь.
?
Теплообменом с окружающей средой и
теплоемкостью калориметра пренебречь.
Решение.
Количество теплоты, необходимое для нагрева льда, находящегося в калориметре, до температуры t:
![]() (1).
(1).
Количество
теплоты, отдаваемое водой при охлаждении
ее до
: ![]() (2).
Количество
теплоты, выделяющееся при отвердевании
воды при
:
(2).
Количество
теплоты, выделяющееся при отвердевании
воды при
: ![]() (3).
Количество
теплоты, вьщеляющееся при охлаждении
льда, полученного из воды, до температуры
t:
(3).
Количество
теплоты, вьщеляющееся при охлаждении
льда, полученного из воды, до температуры
t:
![]() (4).
(4).
Уравнение
теплового баланса: ![]() (5).
Объединяя
(1)—(5), получаем:
(5).
Объединяя
(1)—(5), получаем:
![]() .
.
Ответ: ![]() .
.
Задание С3
В
калориметре находился лед при
температуре ![]() .
Какой была масса
.
Какой была масса ![]() льда,
если после добавления в калориметр
льда,
если после добавления в калориметр ![]() воды,
имеющей температуру
воды,
имеющей температуру ![]() ,
и установления теплового равновесия
температура содержимого калориметра
оказалась равной
,
и установления теплового равновесия
температура содержимого калориметра
оказалась равной ![]() ,
причем в калориметре была только вода?
,
причем в калориметре была только вода?
Решение.
Количество
теплоты, полученное при нагреве льда,
находящегося в калориметре, до
температуры
: ![]() (1).
Количество
теплоты, полученное льдом при его таянии
при
:
(1).
Количество
теплоты, полученное льдом при его таянии
при
: ![]() (2).
Количество
теплоты, отданное водой при охлаждении
её до
:
(2).
Количество
теплоты, отданное водой при охлаждении
её до
: ![]() (3).
Уравнение
теплового баланса:
(3).
Уравнение
теплового баланса: ![]() (4).
Объединяя
(1)—(4), получаем:
(4).
Объединяя
(1)—(4), получаем:
![]() .
.
Ответ: ![]() .
.
