
- •Внутренняя энергия тел и способы ее изменения. Изменение внутренней энергии при: нагревании и охлаждении, парообразовании и конденсации, плавлении и конденсации.
- •Способы изменения внутренней энергии
- •Работа газа при изобарном изменении его объема. Первое начало термодинамики.
- •Первое начало термодинамики
- •3. Применение первого начала термодинамики к изо процессам. Адиабатный процесс. Примеры.
- •Необратимость тепловых процессов. Второе начало термодинамики
- •Принцип действия тепловой машины двс: устройство и принцип работы. Проблемы охраны окружающей среды.
- •Взаимодействие заряженных тел. Закон Кулона. Закон сохранения электрического заряда. Электризация тел.
- •Напряженность электрического поля. Принцип существования полей. Графическое изображение полей точечных зарядов.
- •Работа по перемещению заряда, совершаемая силами электрического поля. Потенциал и разность потенциалов.
- •9. Проводники и диэлектрики в электростатическом поле. Поляризация диэлектриков.
- •10. Конденсаторы. Электроемкость конденсатора. Способы соединения конденсаторов. Применение конденсаторов.
- •11. Постоянный электрический ток, его характеристики и условия существования.
- •13. Электрические цепи. Последовательное и параллельное соединение проводников.
- •14. Работа, мощность и тепловое действие электрического тока. Короткое замыкание. Практическое применение теплового действия тока.
- •15. Эдс. Закон Ома для полной цепи.
- •17. Электрический ток в газах. Несамостоятельные и самостоятельные разряды. Виды самостоятельных разрядов и их характеристика.
- •18. Электрический ток в вакууме. Двухэлектродная электронная лампа. Устройство и принцеп работы электронно-лучевой трубки.
- •19. Полупроводники. Собственная и приносная проводимость полупроводников.
- •21. Магнитное поле условие его существования. Магнитная индукция. Магнитное поле прямого тока, соленоида.
- •22. Взаимодействие токов. Действие магнитного поля на проводник с током. Закон Ампера. Применение закона Ампера.
- •23. Строение магнита сферы Земли и ее взаимодействие с Солнечным ветром. Сила Лоренца. Солнечная активность.
- •24. Магнитные свойства вещества. Ферромагнетика и их применение.
- •25. Опыты Фарадея. Электромагнитная индукция. Магнитный поток.
- •26. Направление индукционного тока. Правило Ленца. Закон эми.
- •27. Вихревое электрическое пол. Эдс индукции в движущихся проводниках.
- •34. Физические основы радиосвязи и радиолокации. Примеры их практического использования.
- •35. Корпускулярная и волновая теория о природе света. Скорость света.
- •36. Законы преломления и отражения света. Скорость света.
- •37. Виды линз. Изображение в линзе. Формула тонкой линзы.
- •38. Дисперсия света. Цвета тел.
Внутренняя энергия тел и способы ее изменения. Изменение внутренней энергии при: нагревании и охлаждении, парообразовании и конденсации, плавлении и конденсации.
Внутренняя энергия 1 атомного газа.
WpΣ=0 ΣEп=0
Для идеального газа WpΣ=0. Поэтому внутренняя энергия U идеального газа складывается из кинетических энергий хаотического, теплового движения его молекул:
Если 1 атомный газ содержит N молекул, каждая из которых обладает в среднем кинетической энергии <Wк>=3/2 кг , то внутренняя энергия этого газа равна:
U=N<Wк>m/M*NA*3/2*kT=3/2*m/M*RT=3/2*PV
U=3/2*m/M*RT
U=3/2*PV
Способы изменения внутренней энергии
Теплообмен- самопроизвольный, необратимый процесс передачи энергии от более нагретых тел к менее нагретым без совершения работы.
Теплопроводность- передача энергии от более нагретых частей тел к менее нагретым, приводящая к выравниванию температуры.
Конвекция- обмен энергией между движущимся неравномерно нагретыми частями газов или жидкостей. Ее интенсивность зависит от разности температуры между слоями и вязкости среды.
Излучение- передача энергии без непосредственно контактов тел, обменивающихся энергией.
Расчет изменения внутренней энергии для различных процессов
-
ПРОЦЕСС
ФОРМУЛА
ПРИМЕЧАНИЕ
Нагревание и охлаждение
ΔU=cmΔT
c-удельная теплоемкость тела
Плавление или кристаллизация
ΔU=±λm
λ- удельная теплота плавления
Парообразование или конденсация
ΔU=±rm
r- удельная теплота парообразования
Сгорание
ΔU=qm
q- удельная теплота сгорания
Работа газа при изобарном изменении его объема. Первое начало термодинамики.
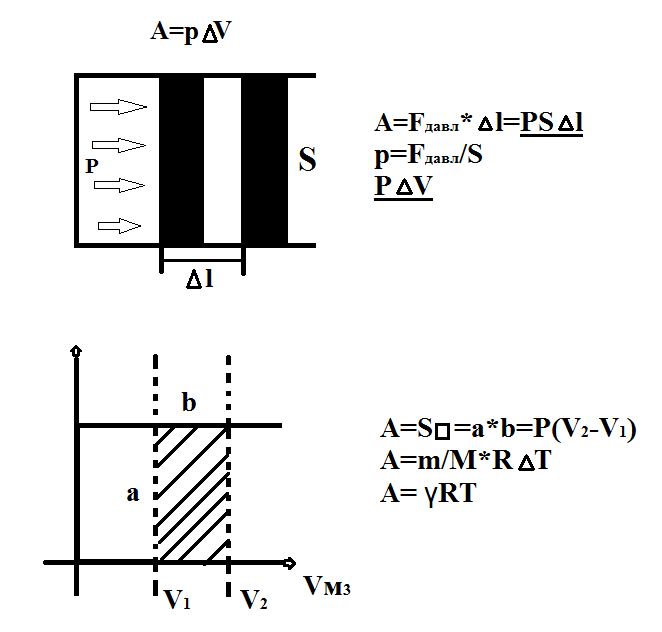
Работа совершаемая идеальным газом при его расширении.
Если газ, расширяясь передвигает поршень на расстояние Δl, то он производит над ним работу.
A=FΔl=pSΔl=Pδv
Работа
при расширении газа (ΔV>0),
работа при сжатии отрицательна (ΔV<0).
Выражение справедливо при любых
изменениях объема твердых, жидких и
газообразных тел. (S-площадь
поршня; p-давление; SΔl=Δl-
изменение объема системы)
Первое начало термодинамики
Это закон сохранения и превращение энергии применительно к термодинамическим процессам
Q=ΔU+A’
Количество теплоты переданное системе идет на увеличение внутренней энергии этой системы и совершения работы этой системой (газа).
A’- работа самого газа над внешними телами A’>0, т.к u↑
A- работа над газом
A<0, т.к u↓
A’=A
3. Применение первого начала термодинамики к изо процессам. Адиабатный процесс. Примеры.
-
ПРОЦЕСС
Условие протекания процесса
(Q=ΔU+A) применимо к изо процессу
Изотермическое расширение

Q=A
Изотермическое сжатие
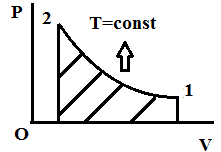
Q=A
Изохорное охлаждение
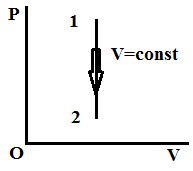
Q=ΔU
Изохорное нагревание
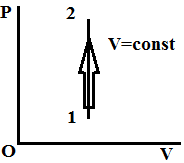
Q=ΔU
Изобарное расширение
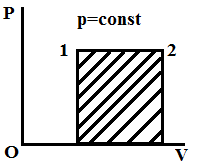
Q=ΔU+A
Изобарное сжатие

Q=ΔU+A
Адиабатное расширение
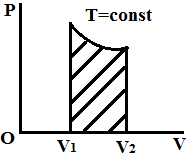
ΔQ=0
A’=-ΔU
Понятие о вечном двигателе. Это воображаемый механизм, который безостановочно движ-ся и совершает работу не потребляя при этом энергии из вне:
A’=-ΔU- вечный двигатель первого рода не возможен, т.к нельзя бесконечно совершать работу за счет бесконечной внутренней эгергии.
