
- •С.В. Іванов, п.С. Борсук, н.М. Манчук загальна хімічна технологія
- •Передмова
- •Теоретичні основи хімічної технології вступ
- •1. Основи хіміко-технологічних процесів
- •1.1 Хіміко-технологічний процес і його зміст
- •1.2. Класифікація хімічних реакцій, які покладені в основу промислових хіміко-технологічних процесів.
- •1.3. Технологічні критерії ефективності хіміко-технологічного процесу
- •2. Структура хімічного виробництва
- •3. Хіміко-технологічні системи
- •3.1. Поняття хіміко-технологічної системи (хтс)
- •3.2. Моделі хіміко-технологічних систем
- •3.3. Технологічні зв'язки в хтс
- •4. Поняття про синтез хіміко-
- •4.1. Texнологічні концепції створення хтс
- •4.2. Аналіз хтс
- •5. Матеріальні і теплові баланси хіміко-технологічних систем
- •5.1. Баланс співвідношень
- •5.1.2. Приклади розрахунку балансів
- •5.2 Основні поняття ексергетичного аналізу хтс
- •6. Термодинамічні розрахунки хіміко-технологічних процесів
- •6.1. Рівновага хімічних реакцій
- •6.2. Константа рівноваги й енергія Гіббса. Рівняння ізотерми Вант-Гоффа
- •6.3. Хімічна рівновага в гетерогенних реакціях
- •7. Вибір технологічних режимів проведення хтп
- •7.1. Способи зміщення рівноваги
- •7.2. Залежність константи рівноваги від температури
- •7.3. Розрахунок рівноваги за термодинамічними даними
- •8. Використання законів хімічної кінетики при виборі технологічного режиму.
- •8. 1. Швидкість гомогенних хімічних реакцій
- •8.2. Залежність швидкості хімічних реакцій від концентрації реагентів; кінетичні рівняння
- •8.3. Способи зміни швидкості простих і складних реакцій
- •9. Кінетика хіміко-технологічних процесів
- •9.1. Вплив різних чинників на швидкість хімічних процесів, які перебігають на мікрорівні
- •9.2. Кінетика хтп, що ґрунтується на оборотних хтп
- •9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
- •9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
- •9.3.3. Методи інтенсифікації гомогенних процесів
- •9.4. Кінетика гетерогенних некаталітичних процесів
- •9.4.2. Швидкість гетерогенних процесів
- •9.4.4. Визначення лімітуючої стадії гетерогенного процесу
- •9.4.5. Способи збільшення швидкості процесу
- •9.5 Типи реакторів для гетерогенних процесів
- •9.5.1 Реактори для проведення реакцій в системах г-т і р-т
- •9.5.2 Реактори для проведення реакцій в системах г—р і р—р
- •10. Каталітичні процеси.
- •10.2. Технологічні характеристики каталізаторів
- •10.3. Гомогенний і гетерогенний каталіз
- •10.4. Властивості твердих каталізаторів і їхнє виготовлення
- •10.5. Апаратурне оформлення каталітичних процесів
- •10.5.3 Апарати зі зваженим (киплячим, псевдокиплячим) шаром каталізатора
- •11. Хімічні реактори
- •11.1 Класифікація реакторів
- •11.2. Вимоги до хімічних реакторів
- •11.3. Структура математичної моделі хімічного реактора
- •10.4. Реактор ідеального змішування періодичний
- •11.5 Реактори безперервної дії
- •11.5.1 Реактор ідеального витіснення (рів)
- •11.5.2. Реактор ідеального змішування безперервний (різ–б)
- •11.5.3 Загальне проектне рівняння реактора
- •11.6 Каскад реакторів ідеального змішання (к-різ)
- •11.7 Графічний метод розрахунку к – різ
- •11.8. Вплив кінетики на вибір типу реактора
- •11.9. Селективність, вихід, ступінь перетворення
- •11.9.2. Залежність селективності від ступеня перетворення
- •11.10. Хімічні реактори з неідеальною структурою потоків
- •11.11. Моделі ректорів з неідеальною структурою потоку
- •11.12. Ячеїста модель.
4.2. Аналіз хтс
4.2.1 Задачі аналізу ХТС. Вони полягають в одержанні відомостей про функціонування системи в залежності від прийнятої хімічної схеми, структури технологічних зв'язків між елементами і підсистемами, а так само від конструкційних і технологічних параметрів, виходячи з заданих властивостей і показників функціонування, що мають оптимальне значення
Для цього необхідні: 1. технологічний аналіз ХТС – одержання технологічних показників: температури, тиску, розмірів потоків, виходу продукту, селективності, кількості відходів і т.ін.;
2. техніко-економічний аналіз ХТС – одержання економічних критеріїв оцінки ефективності системи: – витратних коефіцієнтів на виробництво продуктів і т.ін. і , в кінцевому рахунку, одержання відомостей про собівартість продукції; 3. аналіз функціонування системи – стійкість, надійність, безпека роботи та ін. При цьому необхідно враховувати, що ХТС має властивості, не характерні для окремих її елементів, це обумовлено взаємозалежністю режимів елементів.
Аналіз ХТС здійснюється при розробці проектування системи для визначення її ефективності, а також для порівняння різних варіантів реалізації процесу з метою вибору з них оптимального. Аналіз використовується і за модернізації і реконструкції діючих ХТС. Наведені вище показники роботи ХТС визначаються в резуль-таті рішення систем рівнянь матеріальних і теплових балансів.
5. Матеріальні і теплові баланси хіміко-технологічних систем
Баланси ХТС передають закони збереження маси - матеріальні баланси й енергії - енергетичні баланси, зокрема теплові баланси. Баланси ХТС складаються, як правило, для стаціонарних процесів або для ХТС у цілому, або для окремих елементів обо груп елементів. В останніх випадках зі схеми “вирізається” елемент чи сукупність елементів (рис.5.1.).
Подібне виділення окремих елементів чи групи елементів ХТС надає інформацію не тільки про ефективність ХТС у цілому, але і її складових, що дозволяє виявити "вузькі місця", варіювати параметри елементів чи їх сукупність і направлено здійснювати інтенсифікацію ХТС.
Матеріальний баланс ґрунтується на тому, що у всякій замкненій системі маса речовин, що вступили в реакцію, дорівнює масі речовин, що утворилися в результаті взаємодії.
Наприклад
, у реактор надходять речовини, маси
яких m 1,
m2,
m3
,. mS.
В результаті взаємодії одержують R
продуктів з масою. mR![]() ,
mR
,
mR![]() ,
mR
,
mR![]() ,.
. . mR
,.
. . mR![]() .
Рівняння балансу такої системи буде:
.
Рівняння балансу такої системи буде:
m1 + m2 + m3 . +. mS = mR + mR + mR . . +. mR
І ІІ
ІІ
ІІ

 І
І



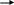

Рис. 5.1. Порядок розрахунку ХТС: І - один елемент,
ІІ – група елементів; ІІІ – ХТС у цілому
![]() (5.1)
(5.1)
або
![]() (5.2)
(5.2)
Тепловий баланс заснований на тому, що прихід теплоти в даному процесі дорівнює витраті її в тому же процесі. Якщо прийняти, наприклад, що в адіабатичному реакторі перебігає екзотермічна реакція, то рівняння теплового балансу буде:
Qp +m1HІ+m2H2 +msHs = m΄1H΄1+m΄2H΄2+mrH΄r
Qp+![]() =
=
![]()
![]() (5.3)
(5.3)
Qp + = = 0, (5.4)
де НJ і Н΄і- ентальпії речовин, що надійшли в реактор і продуктів реакції відповідно;
Qp- теплота хімічної реакції.
Рівняння (5.1-5.4) справедливі для розімкнутих систем. Для замкнених систем при складанні балансів враховується наявність рециркуляції технологічних потоків. Тоді відповідно до рис.4.1 рівняння балансу буде:
mn = m0+mR
Співвідношення потоків у системах з рециклом, як указувалося, враховує коефіцієнт рециркуляції - KR і відношення рециркуляції -R.
Тоді, оскільки:
KR=mR/m0 і R = mR /mn
рівняння балансу приймає вигляд:
mn = m0+Rmn=m0/(1-R) або (5.5)
mR=KR∙m0 (5.6)
