
- •С.В. Іванов, п.С. Борсук, н.М. Манчук загальна хімічна технологія
- •Передмова
- •Теоретичні основи хімічної технології вступ
- •1. Основи хіміко-технологічних процесів
- •1.1 Хіміко-технологічний процес і його зміст
- •1.2. Класифікація хімічних реакцій, які покладені в основу промислових хіміко-технологічних процесів.
- •1.3. Технологічні критерії ефективності хіміко-технологічного процесу
- •2. Структура хімічного виробництва
- •3. Хіміко-технологічні системи
- •3.1. Поняття хіміко-технологічної системи (хтс)
- •3.2. Моделі хіміко-технологічних систем
- •3.3. Технологічні зв'язки в хтс
- •4. Поняття про синтез хіміко-
- •4.1. Texнологічні концепції створення хтс
- •4.2. Аналіз хтс
- •5. Матеріальні і теплові баланси хіміко-технологічних систем
- •5.1. Баланс співвідношень
- •5.1.2. Приклади розрахунку балансів
- •5.2 Основні поняття ексергетичного аналізу хтс
- •6. Термодинамічні розрахунки хіміко-технологічних процесів
- •6.1. Рівновага хімічних реакцій
- •6.2. Константа рівноваги й енергія Гіббса. Рівняння ізотерми Вант-Гоффа
- •6.3. Хімічна рівновага в гетерогенних реакціях
- •7. Вибір технологічних режимів проведення хтп
- •7.1. Способи зміщення рівноваги
- •7.2. Залежність константи рівноваги від температури
- •7.3. Розрахунок рівноваги за термодинамічними даними
- •8. Використання законів хімічної кінетики при виборі технологічного режиму.
- •8. 1. Швидкість гомогенних хімічних реакцій
- •8.2. Залежність швидкості хімічних реакцій від концентрації реагентів; кінетичні рівняння
- •8.3. Способи зміни швидкості простих і складних реакцій
- •9. Кінетика хіміко-технологічних процесів
- •9.1. Вплив різних чинників на швидкість хімічних процесів, які перебігають на мікрорівні
- •9.2. Кінетика хтп, що ґрунтується на оборотних хтп
- •9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
- •9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
- •9.3.3. Методи інтенсифікації гомогенних процесів
- •9.4. Кінетика гетерогенних некаталітичних процесів
- •9.4.2. Швидкість гетерогенних процесів
- •9.4.4. Визначення лімітуючої стадії гетерогенного процесу
- •9.4.5. Способи збільшення швидкості процесу
- •9.5 Типи реакторів для гетерогенних процесів
- •9.5.1 Реактори для проведення реакцій в системах г-т і р-т
- •9.5.2 Реактори для проведення реакцій в системах г—р і р—р
- •10. Каталітичні процеси.
- •10.2. Технологічні характеристики каталізаторів
- •10.3. Гомогенний і гетерогенний каталіз
- •10.4. Властивості твердих каталізаторів і їхнє виготовлення
- •10.5. Апаратурне оформлення каталітичних процесів
- •10.5.3 Апарати зі зваженим (киплячим, псевдокиплячим) шаром каталізатора
- •11. Хімічні реактори
- •11.1 Класифікація реакторів
- •11.2. Вимоги до хімічних реакторів
- •11.3. Структура математичної моделі хімічного реактора
- •10.4. Реактор ідеального змішування періодичний
- •11.5 Реактори безперервної дії
- •11.5.1 Реактор ідеального витіснення (рів)
- •11.5.2. Реактор ідеального змішування безперервний (різ–б)
- •11.5.3 Загальне проектне рівняння реактора
- •11.6 Каскад реакторів ідеального змішання (к-різ)
- •11.7 Графічний метод розрахунку к – різ
- •11.8. Вплив кінетики на вибір типу реактора
- •11.9. Селективність, вихід, ступінь перетворення
- •11.9.2. Залежність селективності від ступеня перетворення
- •11.10. Хімічні реактори з неідеальною структурою потоків
- •11.11. Моделі ректорів з неідеальною структурою потоку
- •11.12. Ячеїста модель.
9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
9.3.1. Селективність для паралельних реакцій. Оскільки селективність є важливим показником ХТП, встановимо залежність φ= f(T) для паралельних реакцій типу:
 (9.6)
(9.6)
В цьому випадку селективність за цільовим продуктом R:
φ=![]() .
(9.7)
.
(9.7)
Підставивши в в це рівняння значення υr і υs, знаходимо:
φR=f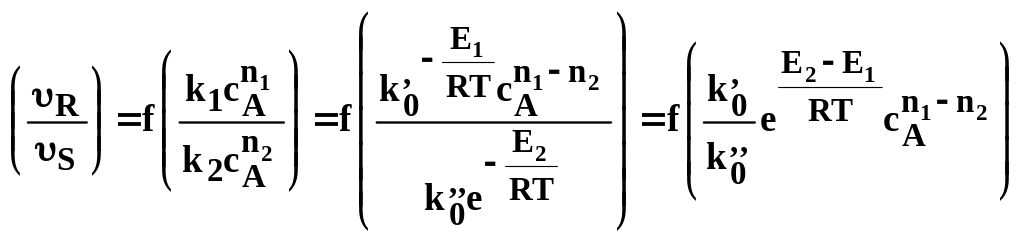 (9.8)
(9.8)
Всі величини, що входять в рівняння (9.8), сталі, за винятком температури, тому при зміні температури змінюється також і селективність, і залежно від значення різниці Е2 –Е1, вплив температури може бути або позитивним, або негативним . Оскільки при низькій температурі знижується швидкість процесу, то і в даному випадку існує деяка найбільш вигідна оптимальна температура Топт. як з погляду термодинаміки (рівноважна), так і з погляду кінетики, при якій досягається необхідна селективність і, зрештою , найбільша економічність процесу.
Аналогічна закономірність спостерігається і в послідовних реакціях. Тому для того, щоб у виробничих умовах забезпечити найбільш високу ефективність процесу, його необхідно проводити у області температурного оптимуму.
Таким чином, температура являється могутнім чинником інтенсифікації хімічного процесу, але можливості для використання цього чинника обмежені спроможністю негативного впливу на процес. У кожному конкретному випадку повинна бути встановлена економічно раціональна температура; вона завжди дещо нижче за Топт, знайденої теоретичним шляхом, оскільки за теоретичного розрахунку не всі фактори враховуються.
9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
Концентрація реагуючих речовин впливає на швидкість реакції всіх типів (окрім реакцій нульового порядку ): з збільшенням концентрації вихідних реагентів швидкість реакції зростає. Так наприклад, сумарна швидкість модельної хімічної реакції дорівнює різниці між швидкостями прямої і зворотної реакцій:
υ=υ1-υ2=k1∙CаА∙СвВ−k2∙CrR∙CsS (9.9)
З цього рівняння виходить, що чим більше значення С А і СВ, тим вища швидкість, а також, що з часом сумарна швидкість реакції знижується, оскільки концентрації вихідних реагентів (СА, СВ) зменшуються, а концентрації продуктів реакції (СR, CS) збільшуються. Тому для того, щоб судити про зміну швидкості реакції, будують криві залежності концентрацій реагентів, що беруть участь в реакції, від часу, тобто встановлюють залежність С= f(τ).
Розглянемо цю залежність для різних типів реакцій. Швидкість необоротної реакції найбільш простого типу:
A![]() ,
,
-υ=![]() (9.10)
(9.10)
Після інтегрування цього рівняння в межах зміни τ від 0 до τ, а концентрації СА від початкового значення СА0, до СА і, приймаючи, що k не залежить від τ, знаходимо:
 ,
,
![]() ,
або
,
або
![]() (9.11)
(9.11)
З рівняння (9.11) виходить, що в міру перебігу реакції, тобто в міру збільшення τ, концентрація вихідної речовини СА знижується за експоненціальним законом, відповідно зменшується і швидкість реакції (рис. 9.8, а). З рис. 9.8,а також видно , що для того, щоб довести реакцію до кінця, необхідний великий час процесу τ, тому що СА асимптотично наближається до нуля. На практиці реакцію не доводять до кінця, її зупиняють через деякий проміжок часу, коли СА>0 і рушійна сила процесу достатньо велика; такий час можна назвати оптимальним τопт .- Внаслідок того, що реакція перебігає не повністю, наприкінці процесу отримують суміш продуктів А і R. Отже, процес слід організувати так, щоб після стадії хімічного перетворення була стадія розділення , а також так, щоб після виділення продукту R вихідний реагент А знов був використаний в реакції, тобто процес необхідно оформити за циклічною схемою.
Для простих оборотних реакцій залежність С= ƒ(τ) складніша. Наприклад, для простої оборотної реакції типу А ↔ R процес зупиняється в той момент, коли концентрація вихідного реагенту СА досягне значення концентрації цього реагенту в стані рівноваги СА* (рис. 9.8,б). Оскільки поблизу рівноваги швидкість взаємодії дуже мала, процес зупиняють після досягнення деякого оптимального часу τопт, при якому різниця СА — С*А (рушійна сила процесу) ще значна і, отже, швидкість процесу досить висока.
Швидкість реакції в цьому випадку виражається рівняннями:
-υA=![]() ,
,
υR=
![]() .
. ![]()
Із складних реакцій розглянемо тільки необоротні паралельні і послідовні реакції.
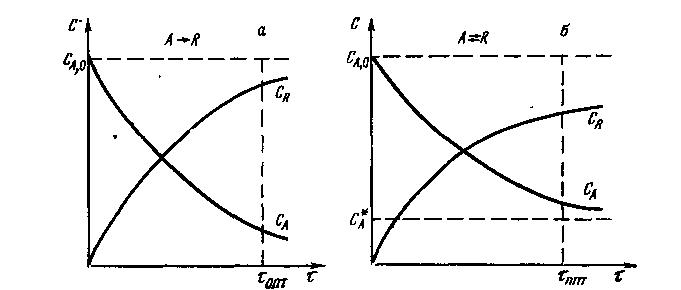
Рис. 9.8. Зміна концентрації компонентів С в часі τ
Для необоротних паралельних реакцій типу:
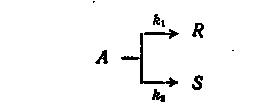 (9.13)
(9.13)
зміна концентрації вихідного реагенту і цільового продукту R в часі показана на рис. 9.8. Швидкості реакцій можуть бути виражені такими рівняннями:
υA=k1CA+k2CA=CA(k1+k2),
υR=k1CA.
υS=k2CA. (9.14)
Найбільш проста схема двох необоротних послідовних реакцій може бути представлена у вигляді:
![]() (9.15)
(9.15)
З часом значення СА знижується, а СR спочатку збільшується, досягає деякого максимального значення, а потім убуває внас-лідок його розкладання і утворення продукту N.
При цьому концентрація проміжного продукту R в деякий момент часу залежить від співвідношення швидкостей кожної з послідовних реакцій. Розрізняють три випадки:
к1>>к2 к1<<к2 k1≈k2
На рис. 9.9 показана зміна концентрації A, R і S в часі для кожного з цих випадків. Із рисунка видно, що якщо k1 >>k2, то за інших рівних умов, за повної витрати продукту А утворюється суміш, що містить продукти R і S. Якщо k1<<к2, то проміжний продукт R у міру його утворення інтенсивно витрачається, тому з самого початку реакції відбувається накопичення речовини S. Якщо к1≈к2, то криві залежності СR=f(τ) і CN=f(τ) займають проміжне положення між кривими, які відповідають k1>>k2 і к1<<k2.
Ш

Максимальна концентрація проміжного продукту СR досягається за умови: dCR/dτ=0.
Тиск також завдає великий вплив на швидкість хімічних процесів, особливо в тих випадках, коли процеси перебігають в газовій фазі або ж при взаємодії газів з рідинами і твердими речовинами.

Рис. 9.9. Зміна концентрації компонентів С паралельних необоротних реакцій:

 R
R
А в часі.
Це пояснюється тим, що за підвищення тиску зменшується об'єм газової фази і відповідно збільшується концентрація реагуючих речовин. Загальну швидкість модельної реакції, якщо вона необоротна або оборотна, але перебігає далеко від рівноваги, можна виразити у вигляді рівняння:
![]()
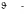 (9.17)
(9.17)
де рА, рВ — парціальний тиск вихідних реагентів.
Але парціальний тиск кожного реагенту пропорційний загальному тиску Р: ра =lP і рВ=mР, (де l, m — сталі).
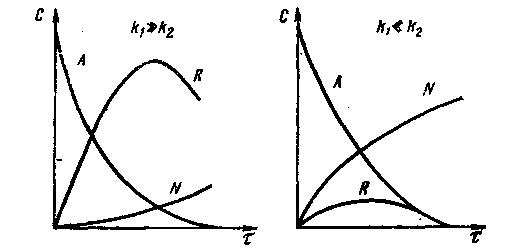
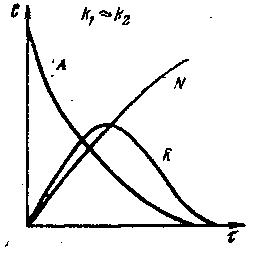
Рис. 9.10. Зміна концентрації компонентів С послідовної необоротної реакції A R N в часі.
Підставивши ці значення в рівняння (9.17), знаходимо:
=kla Pamb Pb=k'Pa+b=k'Pn, (9.18)
де k'=klamb; n — порядок реакції (n = а + b).
Таким чином, швидкість реакції пропорційна тиску в ступені, рівному порядку реакції. Отже, зміна тиску найсильніше впливає на реакції високого порядку (рис. 9.11).
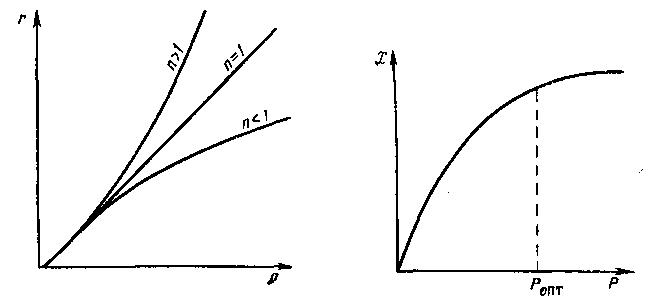
Рис. 9.11. Залежність швидко-сті реакції від тиску Р для газових реакцій різного порядку
Проте підвищення тиску має межу, оскільки dX/dP 0
(рис 9.12), крім того, збільшення тиску призводить до зростання витрати електроенергії, зміні властивостей газу і рідини (зокрема до підвищення їх в'язкості), необхідності застосовування міцніших конструкційних матеріалів і т. ін. Тому у виробничих умовах слід враховувати всі чинники і встановлювати так званий оптимальний тиск Ропт, при якому досягається найбільш висока економічна ефективність технологічного процесу.
Рис. 9.12. Залежність ступеня перетворення X від тиску Р для простої необоротної реакції А→R
В деяких випадках підвищення тиску дає можливість вести процес за температури, що перевищує температуру кипіння розчи-
нів під атмосферним тиском (що також сприяє збільшенню швидкості процесу). Прикладом цьому може слугувати процес варіння целюлози, що проводиться за температури 413—423 К і тиску
0,6—0,8 МПа. У цих умовах значно зростає швидкість процесу і по-переджається кипіння розчину.
У твердофазних процесах за надвисокого тиску відбувається перебудова електронних оболонок атомів і деформація молекул, що може здійснювати суттєвий вплив на швидкість перебігаючих процесів.
