
- •С.В. Іванов, п.С. Борсук, н.М. Манчук загальна хімічна технологія
- •Передмова
- •Теоретичні основи хімічної технології вступ
- •1. Основи хіміко-технологічних процесів
- •1.1 Хіміко-технологічний процес і його зміст
- •1.2. Класифікація хімічних реакцій, які покладені в основу промислових хіміко-технологічних процесів.
- •1.3. Технологічні критерії ефективності хіміко-технологічного процесу
- •2. Структура хімічного виробництва
- •3. Хіміко-технологічні системи
- •3.1. Поняття хіміко-технологічної системи (хтс)
- •3.2. Моделі хіміко-технологічних систем
- •3.3. Технологічні зв'язки в хтс
- •4. Поняття про синтез хіміко-
- •4.1. Texнологічні концепції створення хтс
- •4.2. Аналіз хтс
- •5. Матеріальні і теплові баланси хіміко-технологічних систем
- •5.1. Баланс співвідношень
- •5.1.2. Приклади розрахунку балансів
- •5.2 Основні поняття ексергетичного аналізу хтс
- •6. Термодинамічні розрахунки хіміко-технологічних процесів
- •6.1. Рівновага хімічних реакцій
- •6.2. Константа рівноваги й енергія Гіббса. Рівняння ізотерми Вант-Гоффа
- •6.3. Хімічна рівновага в гетерогенних реакціях
- •7. Вибір технологічних режимів проведення хтп
- •7.1. Способи зміщення рівноваги
- •7.2. Залежність константи рівноваги від температури
- •7.3. Розрахунок рівноваги за термодинамічними даними
- •8. Використання законів хімічної кінетики при виборі технологічного режиму.
- •8. 1. Швидкість гомогенних хімічних реакцій
- •8.2. Залежність швидкості хімічних реакцій від концентрації реагентів; кінетичні рівняння
- •8.3. Способи зміни швидкості простих і складних реакцій
- •9. Кінетика хіміко-технологічних процесів
- •9.1. Вплив різних чинників на швидкість хімічних процесів, які перебігають на мікрорівні
- •9.2. Кінетика хтп, що ґрунтується на оборотних хтп
- •9.3 Швидкість хтп, що ґрунтується на паралельних та послідовних гомогенних реакціях
- •9.3.2. Вплив технологічних параметрів на швидкість гомогенних процесів
- •9.3.3. Методи інтенсифікації гомогенних процесів
- •9.4. Кінетика гетерогенних некаталітичних процесів
- •9.4.2. Швидкість гетерогенних процесів
- •9.4.4. Визначення лімітуючої стадії гетерогенного процесу
- •9.4.5. Способи збільшення швидкості процесу
- •9.5 Типи реакторів для гетерогенних процесів
- •9.5.1 Реактори для проведення реакцій в системах г-т і р-т
- •9.5.2 Реактори для проведення реакцій в системах г—р і р—р
- •10. Каталітичні процеси.
- •10.2. Технологічні характеристики каталізаторів
- •10.3. Гомогенний і гетерогенний каталіз
- •10.4. Властивості твердих каталізаторів і їхнє виготовлення
- •10.5. Апаратурне оформлення каталітичних процесів
- •10.5.3 Апарати зі зваженим (киплячим, псевдокиплячим) шаром каталізатора
- •11. Хімічні реактори
- •11.1 Класифікація реакторів
- •11.2. Вимоги до хімічних реакторів
- •11.3. Структура математичної моделі хімічного реактора
- •10.4. Реактор ідеального змішування періодичний
- •11.5 Реактори безперервної дії
- •11.5.1 Реактор ідеального витіснення (рів)
- •11.5.2. Реактор ідеального змішування безперервний (різ–б)
- •11.5.3 Загальне проектне рівняння реактора
- •11.6 Каскад реакторів ідеального змішання (к-різ)
- •11.7 Графічний метод розрахунку к – різ
- •11.8. Вплив кінетики на вибір типу реактора
- •11.9. Селективність, вихід, ступінь перетворення
- •11.9.2. Залежність селективності від ступеня перетворення
- •11.10. Хімічні реактори з неідеальною структурою потоків
- •11.11. Моделі ректорів з неідеальною структурою потоку
- •11.12. Ячеїста модель.
9.3.3. Методи інтенсифікації гомогенних процесів
Каталізатори винятково впливають на швидкість хімічних реакцій , знижуючи енергію активації, яка входить в показник ступеня рівняння Арреніуса. Внаслідок цього швидкість реакції у присутності каталізатора іноді збільшується в мільйони разів. Звичайно каталізатор вибирають з таким розрахунком, щоб він володів селективною дією, тобто прискорював процес отримання цільового продукту.
Раніше вказувалося, що на практиці найчастіше використовується класифікація хімічних реакцій за фазовою ознакою, відповідно розрізняють гомогенні і гетерогенні реакції. За цією ж ознакою найчастіше підрозділяють хімічні процеси і реактори, в яких ці процеси здійснюються.
У гомогенних системах всі реагуючі речовини перебувають в одній якій-небудь фазі: газовій (г), рідкій (р) або твердій (т).
У гетерогенних системах реагуючі речовини знаходяться в різних фазах: газ—рідина (г—р), газ—тверде (г—т), рідина—твер-де (р−т), дві рідини (р-р), що не змішуються, і дві тверді фази (т-т).
Найчастіше в промислових процесах зустрічаються системи г—р, г—т і р—т. Іноді в промислових процесах беруть участь три або чотири фази, наприклад г—р—т, г—р—р, г—р —т—т. Звичайно за окремі фази приймають тільки основні компоненти і не враховують наявність малих кількостей домішок. Так, наприклад, в системах р—р і р—т часто міститься газова фаза, оскільки процеси проводяться у присутності повітря або інших газів, або ж у присутності пари, тому що рідкі компоненти частково випаровуються. Але газову фазу враховують тільки в тому випадку, якщо вона робить істотний вплив на процес.
Деякі процеси розпочинаються в гомогенному середовищі, а потім в результаті появи нової фази система переходить в гетерогенну. Наприклад, при отриманні полістиролу до рідкого стиролу додають пероксид бензоїлу і нагрівають, при цьому відбувається полімеризація стиролу з утворенням нової фази — твердого полістиролу.
Швидкість реакції в гомогенних системах вища, ніж в гетерогенних, тому що в першому випадку реакції перебігають на рівні окремих молекул (так званий мікрорівень). Тому в практичних умо-вах звичайно прагнуть перевести гетерогенний процес в гомогенний (шляхом плавлення або розчинення твердих реагуючих речовин, абсорбції або конденсації газів).
Строго гомогенні процеси, тобто процеси, що перебігають в одній фазі, зустрічаються в промисловості порівняно рідко, оскільки будь-яка речовина містить сліди різних домішок, що знаходяться в іншій фазі. Наприклад, в 1 дм3 чистого гірського повітря міститься близько 1000 зважених частинок, а в 1 дм3 дистильованої води до 20000 частинок. Оскільки сліди чужорідних домішок часто активно впливають на хід процесу як каталізатори або інгібітори, більшість процесів лише умовно можна віднести до гомогенних. Число таких умовно гомогенних процесів велике в технології і неорганічних, і органічних речовин. Наприклад, окиснення сірководню і пари сірки киснем повітря у виробництві сірчаної кислоти:
2H2S+3О2=2SО2+2H2О−ΔН, (9.19)
S+O2=SO2–ΔН (9.20)
перебігає в гомогенній газовій фазі, незважаючи на наявність в повітрі великого числа твердих частинок. До гомогенних процесів відносять також окиснення оксиду азоту (II) до оксиду азоту (IV) киснем повітря у виробництві нітратної кислоти:
2NO+О2 2NO2–ΔН (9.21)
і багато інших.
Особливо численні і різноманітні гомогенні процеси в газовій фазі, що здійснюються в технології органічних речовин. Прикладом цьому може слугувати спалювання всіляких видів газоподібного палива і, зокрема, природного газу. Процес спалювання різного рідкого палива також в більшості випадків являється гомогенним процесом, тому що всяке рідке паливо заздалегідь випаровується, а пара, що утворилися, потім окиснюються киснем повітря.
У технології органічних речовин сутність багатьох гомогенних процесів в газовій фазі полягає в тому, що газоподібні вихідні речовини або пара, яку одержують випаровуванням рідини, обробляються тим або іншим газоподібним компонентом: хлором, оксидом сірки (IV), оксидами азоту і ін., при цьому звичайно перебігають паралельні і послідовні реакції.
Наприклад, за термічної дії хлору на метан при 523—673 К, одержують ряд сполук:
СН4+Сl2—>НС1+СН3С1 (хлористий метил) (9.22)
СН3С1+С12—>НС1+СН2Сl2 (хлористий метилен) (9.23)
СН2С12+С12—>НС1+СНС13 (хлороформ) (9.24)
СНСl3+С12 НС1+ СС14 (тетрахлорид вуглецю) (9.25)
З великого числа процесів, що перебігають в рідкій фазі, до гомогенних можна віднести процеси нейтралізації водних розчинів кислот водними розчинами лугів. Наприклад, при взаємодії аміачної води і сірчаної кислоти в коксохімічному виробництві одержують сульфат амонію:
2NH4OH+H2SO4=(NH4)2SO4+2Н2О (9.26)
До гомогенних реакцій відносяться також деякі обмінні реакції, що перебігають в розчинах:
KCl+NaNO3 NaCl+KNO3 (9.27)
У рідкій фазі одержують прості і змішані ефіри з спиртів, наприклад, при розкладанні етилсульфату метиловим спиртом:
C2H5OSO2OH+СН3ОН С2Н5ОСН3+H2S04 (9.28)
У гомогенному середовищі здійснюють такий важливий процес, як отримання адипінової кислоти:
3 С6Н11ОН+8НNОз—>ЗС6Н10О4+7Н20+8NO (9.29)
і багато інших.
Гомогенні процеси в більшості випадків перебігають в кінетичній області, тобто загальна швидкість процесу визначається швидкістю хімічної реакції і підкоряється закономірностям, встановленим для процесів, що перебігають на мікрорівні.
Швидкості гомогенних процесів, в основі яких лежать прості необоротні реакції першого і другого порядків (А R і 2А R), виражаються рівняннями:
![]() ,
,
(9.30)
,
,
(9.30)
з яких виходить, що для підвищення швидкості необхідно збільшувати значення k (шляхом підвищення температури або застосуванням каталізатора) і САо. Оскільки на практиці в більшості випадків гомогенні реакції являються складними (паралельними або послідовними), то залежно від значення констант швидкостей цих реакцій концентрація продуктів реакцій змінюватиметься в часі по різному. При цьому, чим вищий порядок реакції, тим більший вплив робить концентрація вихідного реагенту на швидкість відповідної реакції. Наприклад, за наявності двох паралельних реакцій першого і другого порядків збільшення САо в два рази змінює співвідношення швидкостей цих реакцій в 4 рази. Після інтегрування приведених вище рівнянь в межах зміни ХА від 0 до ХА знаходимо:
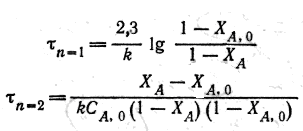 (9.31)
(9.31)
Якщо ХАо=0, то
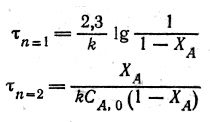 (9.32)
(9.32)
Одержані рівняння дозволяють визначити час τ, необхідний для досягнення заданого кінцевого ступеня перетворення ХА. З цих рівнянь виходить, що константа швидкості реакції першого порядку вимірюється в год-1, а реакції другого порядку-в м3∙кмоль∙год-1.
Гомогенний процес на макрорівні перебігає у тому випадку, коли на хімічну реакцію накладаються інші фізичні або фізико-хімічні процеси. Наприклад, при взаємодії двох рідких вихідних реагентів або їх розчинів швидкість гомогенного процесу залежить від умов і швидкості перемішування рідин; якщо хімічна взаємодія перебігає за підігрівання, то швидкість гомогенного процесу залежатиме також від способу підведення теплоти.
