
- •Тема1.Методи одержання електродів та порошкових матеріалів для напилення і наплавлення
- •І чистим вуглецем:
- •Запитання для самоперевірки
- •Тема 2. Склад та фізико-хімічні властивості порошків
- •Металеві порошки характеризуються хімічними, фізичними і технологічними властивостями.
- •Запитання для самоперевірки
- •Тема 3. Особливості нанесення покриттів із різних груп
- •18.2. Введення до складу покрить пластичного матеріалу
- •Д исперсність порошку, мкм с, % (за масою) н, мПа
- •Лекція 24. Металооксидні покриття
- •Лекція 25. Будова поверхні металу, на який наносять покриття, і явища, що відбуваються на ній
- •Тема 4. Принцип вибору матеріалів для різних типів
- •Лекція 29. Вибір типу покрить і його складу
- •Запитання для самоперевірки
- •А. Сплави на основі нікелю і титану
- •М. Механічні суміші
- •К. Композиційні порошки
- •Л. Чисті метали
- •Тема 1. Методи одержання електродів та порошкових матеріалів для напилення і наплавлення............................................................ 3
- •Тема 2.Склад та фізико-хімічні властивості порошків....................... 25
- •Тема 3. Особливості нанесення покриттів із різних груп матеріалів.... 52
- •Тема 4.Принцип вибору матеріалів для різних типів покрить............ 110
- •65044, Одеса, пр. Шевченка, 1
Тема1.Методи одержання електродів та порошкових матеріалів для напилення і наплавлення
Лекція 1. Методи наплавлення матеріалів
Методи наплавлення, електроди,присадочні та порошкові матеріали
Основним завданням наплавлення є відновлення зношених деталей машин і апаратів, а також зміцнення з метою зменшення зносу чи поліпшення інших хімічних чи фізичних властивостей.
Існує декілька методів наплавлення. Основні з них такі:
електродугове ручне в повітряному середовищі й у захисних газах, електродугове під шаром флюсу, електрошлакове ігазополуменеве, електродугове на постійному струмі. В останньому випадку електро-дом є графіт, а наплавний матеріал - присадка.
З наплавних матеріалів також роблять електроди як суцільні так і трубчасті з порошковим наповненням.
Сталi, використовувані для виготовлення зварювального дроту, за ДСТ 2246-70 додатково маркуються буквами Св, а наплавного дроту, за ДСТ 10543 – 82 — буквами Нп.
Електроди для дугового зварювання позначаються буквою Э і наступними за нею буквами і цифрами. Перші дві чи три цифри позначають вміст вуглецю в сотих частках відсотка. Цифри, що йдуть за літерними позначеннями елементів, зазначають середній вміст елемента у відсотках (якщо вміст елемента менше ніж 1,5 %, цифру не ставлять). При середньому вмісті кремнію до 0,8 % і марганцю до 1,0 % букви С і Г не ставлять.
Прутки для наплавлення позначають індексом ПрН, гранульовані порошки зі сплавів - індексом ПГ. Далі йдуть букви і цифри, що зазначають середній вміст елементів сплаву, з якого виготовлений порошок. Порошкові дріт і стрічка позначаються відповідно ПП і ПЛ. А стрічка зпечена з порошків - ЛС.
Електроди групи I застосовують для наплавлення деталей, експлуатованих при звичайній температурі. Метал, наплавлений електродами групи II має структуру бейніту чи мартенситу з залишковим аустенітом (при високому вмісті вуглецю утворюються також і карбіди). Наплавлені шари володіють високою червоностійкістю, тому ці матеріали можна застосовувати з метою підвищення зносостійкості штампів для гарячої обробки металів тиском. Електроди групи III дозволяють наносити шари, що добре обробляються у відпаленому стані. Після загартування і відпуску твердість наплавленого металу висока (до HRC 54—62). Для наплавлення деталей з високомарганцевистої сталi марки 110Г13Л (експлуатованих при великих ударних навантаженнях) застосовують електроди групи IV. Електроди групи V призначені для наплавлення металорізального інструмента і штампів для гарячої обробки металів тиском.
Таблиця 1.1
Наплавні електроди
Група |
Тип електрода |
HRC |
Марка електрода |
Наплавлення |
I |
Э-10Г2 Э-11ГЗ Э-12Г4 Э-15Г5 ЭН-14М2Х ЭН-40 ЭН-50 |
25 32 37 40 27 35 - 40 50
|
ОЗН-250У ОЗН-ЗООУ ОЗН-350У ОЗН-400У |
Деталей, експлуатованих в умовах інтенсивного зношування; що супроводжуються ударами |
II
|
ЭН - 80ХЧСГ Э - ЗОВ8ХЗ Е - 35Х12ВЗСФ ЭН - 60Х2СМ |
55 50 |
ЦШ-1, ИН-1 Ц-16 |
Гарячих штампів |
ІІІ
|
Э-37Х9С2 Э-70ХЗСМТ Э-100 Х 12М ЭН-70ХПНЗ |
25 |
ОЗШ - 3 ЭН-60МЭН-Х12М |
Холодних штампів після загартування і відпуску наплав-леного шару HRC = 54 - 62 |
IV
|
Э-65Х11НЗ Э-65Х25М13НЗ |
|
ОМГ - Н ЦНИИН - 4 |
Зношених деталей зі сталі 110Г1ЗЛ |
V
|
Э - 90В10Х5Ф2 Э -105У6Х5МЗФЗ Э -08К15В7М5ХЗСФ ЭН - 80В18Х4Ф ЭН - У30Х25РС2Г |
60 60 |
ЦИ-2У И-1 ОЗИ-4
Вуглецю 3-3,5%
|
Металорізального інструмента, витяжних і прошивних гарячих штампів |
VI |
Э-95Х7Г5С Э-30Х5В2Г2СМ |
48-55 |
12АН/ЛИВТ ТКЗ-Н |
Деталей, що працюють в умовах ударно-абразивного зношування, структура -.мартенсит + карбід |
VII |
Э-300Х28Н4С4 Э-10Х14В13Ф2 |
50 56 |
ЦС-1 ВСН-6 |
Деталей, експлуатованих в умовах інтенсивного абразивного зношування з ударними навантаженнями.Структура мартенсит + карбід. Ударні наван. середні |
VIII
|
Э - 320Х23С2ГТР Э - 320Х25С2ГР |
56 - 60 |
Т-620 Т-590 Мартенсит, карбід |
Деталей, експлуатованих в умовах абразивного зношування при відсутності ударів |
IX |
Э -08Х17Н8С6Г Э- 13Х16Н8М5С5Г4Б Э-190ДО62Х29В5С2 |
|
ЦН-6М ЦН-6Л, ЦН-12М УН-12Л, ЦН-2 |
Ущільнювальних поверхностей трубопровідної арматури для енергетики і нафтоапаратури. Противозадирність при терті без змащення, антиерозійні та анти-корозійні властивості |
Електроди груп VI — VIII служать для наплавлення деталей, що працюють при різних сполученнях ударного й абразивного впливу, відповідно при максимальному, середньому і мінімальному ударних навантаженнях.
Структура наплавлень із твердістю HRC—48…62 складається переважно з мартенситу і надлишкового карбіду хрому. Метал, наплавлений при використанні електродів групи ІХ, володіє високими продуктивними властивостями при терті без змащення, а також високими антиерозійними й антикорозійними властивостями і високою зносостійкістю при звичайних і високих температурах.
Спеціальні електроди ВСН-6; 1,2 % С, Si – 1,2%, Мn-0,8%, Сr-13 %, W-13,3 %, V-1,6 %, HRC - 55.
Сталевий наплавний дріт (з вуглецевої, легованої і високолего-ваних сталей) використовують як електрод при відновлювальному зносостійкому наплавленні під флюсом, а також у середовищі вуглекислого газу й у сумішах захисних газів. Холоднокатану електродну стрічку з корозійно-стійких сталей використовують для антикорозійного наплавлення в хімічному, нафтовому й атомному машинобудуванні.
Сталевий наплавний дріт марок Нп випускається за
ДСТ10543 - 82, а сталевий зварювальний марок Св для наплав-лення за ДСТ 2246—70. Твердість шарів, наплавлених дротами марок Нп, коливається в межах НВ 1600—3400 МПа (після наплавлення) і HRC 32—56 (після загартування), а дротами марок Св у межах НВ 1200— 3000 МПа (після наплавлення) і HV 5500—6000 МПа (після загартування).
Для наплавлення матеріалів з підвищеним змістом вуглецю і легуючих компонентів застосовують порошкові дроти, що являють собою оболонку з пластичного металу, заповнену сумішшю легуючих, газо- і шлакоутворюючих матеріалів (табл. 1.2).
Аналогічну будову мають порошкові стрічки (шириною 10—30 мм, товщиною 3— 4 мм) ПЛ-АН101 (для наплавлення високохромистого чавуну типу 300Х25НЗС) і ПЛ-АН102 (для наплавлення сплаву типу 250Х20СЗФ). Порошкові стрічкові електроди використовують, зокрема, для наплавлення деталей засипного апарата доменних печей тощо. Склад і властивості порошкових дротiв регламентую-ться такими документами:
ДСТ 26101- 84; ТУ 144-(247—72). (344—73). (484-74);
ТУ 144-609 (610, 683. 684, 770)-76; ТУ 144-799 (800, 802, 840)- 77;
ТУ 48-21-(49—72); ТУ 19-4206-35—75; ТУ 86 УРСР 085.137—76; ТУ ИЭС18—75 (41—78); ТУ ВНИИСТ.
Порошкові стрічки випускаються відповідно до ДСТ 26467—85, ТУ ИЭС 89—73. (107—75), (108—75), (164—77); ТУ 48' 19-43—73.
Таблиця 1.2
Порошковий дріт
Марка дроту |
Наплавлю-ваний метал |
Додатко-вий захист |
HRC наплавлено-го металу |
Призначення (наплавлювані вироби) |
ПП-АН105 |
100М13Н4 |
— |
20—25 |
Залізничні хрестовини, виливки зі сталі 110М13Л |
ПП-АН106 |
10Х14Т |
— |
42—48 |
Ущільнювальні поверхні арматури для температури <450°С |
ПП-АН125 |
200Х15СТР |
— |
50—58 |
Зуби і козирки ковшів екскаваторів |
ПП-АН170 |
70Х20РЗТ |
— |
60—65 |
Робочі колеса і улітки ґрунтових насосів |
ПП-ЗХ2В8 |
35Х2В8Ф |
Флюс АН - 20 |
44—50 |
Валки гарячої прокатки, ножі блюмінгів |
ПП-25Х5ФМС |
25Х5ФМС |
Те ж |
40—46 |
Обтискні валки гарячої прокатки |
1.2. Спечені порошкові матеріали.
Спечені електродні стрічки виготовляють прокаткою суміші порошку (заліза, нікелю, міді) і порошків легуючих матеріалів з наступним спіканням стрічки в захисному середовищі. При наплавленні під флюсом АН-60 спеченої стрічки ЛС-70ХЗМН одержують зносостійкий шар твердістю HRC 58—62. Наплавлений спеченою електродною стрічкою ЛС-5Х4ВЗФС метал має високу термостійкість (застосовують для наплавлення валків гарячої прокатки металів). Спечені стрічки застосовуються в автомобільній промисловості, в металургійному і хімічному машинобудуванні та ін.
Для захисту наплавлюваного металу використовуються флюси. Ці неметалічні матеріали, розплавляючись при наплавленні, захищають метал від окислювання, забезпечують стабільність дуги й одержання наплавленого металу заданого складу.
Застосовують також спечені прутки і присаджувальні кільця. Присаджувальні кільця марок ПК-НХ35СЗ (ТУ ЛЗЛК) і ПК-ХН60ВУ (ТУ 37.311.017—74) з жаростійких хромонікелевих сплавів використовують для плазмового наплавлення клапанів автомобільних двигунів та інших двигунів внутрішнього згоряння. Спечені електроди з карбiдохромових керметів КХН-15, КХН-20 і КХН-30 (на основі карбіду хрому з нікелевим зв'язуванням) застосовують для наплавлення шарів, що володіють високими твердістю, зносостійкістю і стійкістю до окислювання і корозії.
Для наплавлення зносостійких і жаростійких шарів газополуменевим і дуговим способами застосовують литі присаджувальні прутки із сормайту, стеліту і реліту [Пр-С1. Пр-С2,
Пр-С27, Пр-ВЗК, Пр-ВЗК-Р (ДСТ 21449— 75); Реліт-3, Релит-тз
(ТУ 48-42-34—70), АН-ЛЗ (ТУ 26-02-769—77)]. Литі кільця марок ЭП (ТУ 14-131-133—73, ТУ 14-131-344—77) використовують для плазмового наплавлення клапанів автомобільних двигунів.
У табл. 1.3 наведений хімічний склад сормайтів та їхнi властивості.
Сормайт № 1 — заевтектичний сплав, близький за складом і структурою до високохромистих чавунів; сормайт №2 доевтек-тичний сплав, близький до високохромистих сталей. Структура сор-майтів складається зі складних карбідів хрому і заліза і евтектики. Сормайти наплавляють на деталі, що піддаються абразивному зно-шуванню (плужні лемеші, ножі бульдозерів і грейдерів, шнеки цементних насосів тощо), на інструменти для обробки металів тис-ком, на деталі, що працюють у середовищі агресивних газів при під-вищених температурах (засипних апаратів доменних печей та ін.).
Випускаються сормайти у вигляді прутків (діаметром 6—7 мм) і великих (з розмірами часток до 1,25 мм) та дрібних (0,02—0,04 мм) порошків. Прутковий сормайт звичайно наплавляють дуговим або газополуменевим методом, порошковий сормайт — за допомогою струмів високої частоти.
Високою зносостійкістю і стійкістю проти корозії володіють хромовольфрамокобальтові наплавні сплави - стеліти. Виготовляють і застосовують стеліти В2К, ВЗК (табл. 1.4) та ВЗКР.Основою сплаву є аустеніт, що обумовлює високу ударну стійкість, міцно утримуючи карбідні зерна. Вміст карбідної фази складає 30…45 %. Для підвищення пластичності в стеліти вводять рідкоземельні елементи. Стеліти випускаються у вигляді стрижнів діаметром 4—7 мм. Їх наплавляють на поверхні деталей, що зношуються, і крайки інструментів дуговим, електрошлаковим, газополуменевим чи індукційним способом у два-три шари.
Зносостійкість підвищується в 3—5 разів. Твердість і відповідно зносостійкість наплавлених шарів мало змінюються до температури 700°С. Широкому застосуванню стелітів перешкоджає дефіцитність основних компонентів (кобальту, вольфраму).
Релiт
—
евтектична суміш карбідів вольфраму
(WC і W![]() C).
Містить 95—96 % W і 3.6—4.0 % загального
вуглецю (вільного не більше ніж 0,1 %). Має
більш високу твердість (24 000-30 000 МПа),
нiж
монокарбід вольфраму. Випускають реліт
у вигляді крупки марки 3 (зерновий) і у
вигляді електродів ТЗ (трубчасто-зерновий).
Застосовують реліт для армування
бурового інструмента, щік дробарок,
ковшiв
екскаваторів(
табл.
1.6
).
C).
Містить 95—96 % W і 3.6—4.0 % загального
вуглецю (вільного не більше ніж 0,1 %). Має
більш високу твердість (24 000-30 000 МПа),
нiж
монокарбід вольфраму. Випускають реліт
у вигляді крупки марки 3 (зерновий) і у
вигляді електродів ТЗ (трубчасто-зерновий).
Застосовують реліт для армування
бурового інструмента, щік дробарок,
ковшiв
екскаваторів(
табл.
1.6
).
Таблиця 1.3
Хімічний склад і властивості сормайтів (ДСТ 21449—75)
.
Сор-майт |
Зміст елементів, % |
Властивості |
|||||||||||
Fe |
Сг |
Ni |
С |
Si |
Mn |
S |
Р |
|
|
ТПЛ
ОС |
т/м3 |
HRC |
|
№1 (Пр-C1) |
Осно-ва |
27—31 |
3—5 |
2,5—3,3 |
2,8—3,5 |
0,4—1,5 |
До 0,07 |
До 0,06 |
700 |
12 |
1275 |
7,4 |
>50 |
№2 (Пр-С2) |
Осно-ва |
13—17 |
1,5—2,5 |
1,5—2,0 |
1.5—2.2 |
0,4—1,0 |
До 0,07 |
До 0.06 |
1100 |
13 |
1300 |
7,6 |
>44 |
Таблиця 1.4
Хімічний склад і властивості стелітів (Fe решта)
Сплав |
Вміст елементів, % |
т/м3 |
ТПЛ
ОС |
|
HRC |
||||||||
Cr |
W |
Co |
Ni |
C |
Si |
Mn |
P |
S |
|||||
В2К |
27-33 |
13-17 |
47-55 |
2.0-2.2 |
1.8-2.5 |
1.0-2.0 |
1.0-1.2 |
<0.008 |
<0.07 |
---- |
1260 |
600-700 |
46-48 |
В3К |
28-32 |
4-5 |
58-62 |
2.0-2.2 |
1.0-1.5 |
2.3-2.5 |
----- |
------ |
------ |
8.55 |
1275 |
600-700 |
42-43 |
1.3 Порошкові та зернисті наплавні матеріали
Їх застосовують при індукційній, плазмовій і газополуменевій наплавці. Вони випускаються грубозернисті (розмір часток 1,25 - 0,8 мм), дрібні (0,8 - 0,4 мм) і дуже дрібні < 0,16 мм. Великі йдуть для наплавлення ТВЧ, дрібні - для плазмового, дуже дрібні -для газополуменевого напилення.
Для наплавлення застосовують також різні суміші порошків, феросплавів, вуглецевих матеріалів, а також карбідів і боридів. Призначаються вони для наплавлення графітовим електродом на деталі які працюють в режимi інтенсивного абразивного зношу-вання.
Склад, твердість покриття після наплавлення та галузі викорис-тання деяких порошкових наплавних матеріалів наведений у табл.1.5.
Таблиця 1.5.
Хімічний склад і призначення гранульованих порошків
Марка порошку |
Середній хімічний склад, % |
HRC Наплле-ного металу |
Призначення (наплавлювані вироби) |
||||||
С |
Si |
Mn |
Cr |
Ni |
B |
Fe |
|||
ПГ-С1 ПГС-27 ПГ-АН1 ПГУС25 Вокар ПГ-СР2 ПГ-СРЗ Сталініт С-2М ФБХ6-2 КБ Х БХ |
2,9 3,5-4,5 2-2,8 4.9 9.5 0.35 0.55 8 7 3.5-5.5 4-6 0.3-1
|
3.5 1-2 1.5-2 2.1 ---- 2.5 3.0 3 05-3 1-2.5 0.5-1.4 0.5-1 |
1.2 0.8-1.5 0.5-1.5 1.2 --- --- ---- 13 ---- 6-8.5 ---- 2.5-5.5 |
29.0 25-28 26-32 38.0 - -- 13.5 15.0 18 24-26 28-37 42-52 35-44 |
4.0 1.5 -2----- 1.4 Осноа Осноа --- ---- ----- ----- ----- |
---- 0,3 W 1.6 -- ---- 1.8 2.4 ----1.3-9. 0.8 |
Осн Осн Осн Осн 85%W 5.0 <5.0 Осн Осн Осн Остал Остал |
51 53 54 55 75 35 45 60 54 53 60 63
|
Деталі металургійного обладнання,сільсь-когосподарських машин. Лемехи плугів і деталі, що піддаються абразивному зношуванню без ударів.Ущільню-вальні поверхні арматури теплових і атомних електро-станцій для темпе-ратур до 600 °С |
Таблиця 1.6.
Гранулометричний склад сплаву реліт
Марка сплаву* |
Розміри зерен реліту,мм |
№ сита** |
Розміри трубки, мм |
|||
З (зерновий) |
ТЗ (трубчасто-зерновий) |
Зовнішній діаметр |
Товщина стінки |
Довжина (±7) |
||
3 – 25 3 – 16 3-9 ------ 3 - 6 3 - 4 |
ТЗ-25-7 ТЗ-16-6 T3-9-5 T3-9-4 T3-6-4 T3-4-3 |
2,5-1,6 1,6-0,9 0,9-0,63 0,9-0,63 0,63-0,45 0,45-0,28 |
2,5-1,6 1,6-0,9 0,9-0,63 0,9-0,63 0,63-0,45 0,45-0,28 |
6 7 5 4 4 3 |
0,4 0,4 0,4 0,3 0,3 0,3 |
390 390 390 390 390 390 |
*- Друга цифра позначає максимальний розмір зерен, мм, збільшений у 10 разів, третя цифра позначає діаметр трубки.
**- Перше число показує номер сита, через який частинки проходять, а друге - номер сита, на якому вони затримуються
Лекція 2. Властивості і методи одержання карбідів
2.1. Властивості металоподібних карбідів
Карбіди перехідних металів з незаповненими d - електронними оболонками мають високу твердість, зносостійкість і температуру плавлення. Порошки з них широко використовують як основний компонент твердих сплавів i наплавлюваних матеріалів, для напилювання покрить газотермічними методами.
Основні властивості і структура найбільш використовуваних карбідів перехідних елементів наведені в табл. 2.1
Таблиця 2.1
Структура і властивості металоподібних карбідів
перехіднихметалів
Карбід |
Кристалічна гратка |
т/м3 |
Тпл оС |
Н |
|
Е |
|
TiC ZrC0.97 HiC0.99 VC0.87 NbC0.99 TaC0.98 Cr23C6 Cr7C3 Cr3C2 Mo2C WC W2C |
Кубічна » » » » » » Гексаго – нальна Ромбічна Гексаго- нальна
|
4,94 6,56 12,76 5,71 7,80 14,50 6,96 6,90 6,60 9,18 15,67 17,23 |
3067 3420 3828 2648 3600 3983 1500 1780 1810 2400 2776 2700 |
29000 26000 27000 29000 24000 25000 9700 13800 13300 15000 21000 19900
|
52,2 50,0 45,0 65,0 51,1 42,1 127 109 75 71 19,2 80,0
|
4,940,1 4,010,8 4,80,1 4,95 4,750,09 5,50,11 --- --- 3,698 5,307 7,370,15 --- |
205,55 193,26 205,61 99,02 137,59 143,30 600,43 209,75 98,90 46,93 38,79 -------- |
2.2. Неметалічні карбіди
Крім
карбідів перехідних металів, велике
поширення в техниці мають два неметалічних
карбіди: кремнію SiC і бору В![]() С.
С.
Карбід
кремнію (карборунд) являє собою сполуку
напівпровідника кремнію з вуглецем.
Він буває в двох модифікаціях: з
гексагональною кристалічною ґраткою![]() і з кубічною типу алмазу
і з кубічною типу алмазу![]() .
Карбід кремнію відрізняється високою
твердістю, теплопровідністю, вогнестiйкістю,
специфічними електричними
напівпровідниковими властивос-тями.
Він хімічно стійкий (на нього діє тільки
суміш азотної і плави-кової кислот, а
також фосфорна кислота при температурі
230
оС).
При нагріванні в повітряному середовищі
на його поверхні утворюється шар SiО2,
що захищає
Si
від подальшого окислювання. Основні
властивості карбіду кремнію наведені
в табл. 2.2.
.
Карбід кремнію відрізняється високою
твердістю, теплопровідністю, вогнестiйкістю,
специфічними електричними
напівпровідниковими властивос-тями.
Він хімічно стійкий (на нього діє тільки
суміш азотної і плави-кової кислот, а
також фосфорна кислота при температурі
230
оС).
При нагріванні в повітряному середовищі
на його поверхні утворюється шар SiО2,
що захищає
Si
від подальшого окислювання. Основні
властивості карбіду кремнію наведені
в табл. 2.2.
Таблиця 2.2.
Властивості карбіду кремнію
Модифі- кація |
, т/м3 |
Твердість |
Температура дисоціації,
ОС |
ОС-1 |
Е 10 МПа |
|
|
За Моосом |
Н , МПа |
||||||
Гексагональна |
3,214 |
9,0 – 9,3 |
21300-29500 |
2780 |
4,2-4,7 (при 427 оС) |
4,08 |
69,49 |
Кубічна |
3,166 |
9,2 – 9,8 |
26100-37400 |
2830 |
3,8 (при 200оС) |
4,013 – 4,324 |
------- |
Другий карбід неметалічного походження - карбід бору (В4С).
Він має дуже високу твердість,поступаючись тільки алмазу, високу хімічну стійкість, практично не розкладається мінеральними кислотами та їхніми сумішами. Ґратка В4С характеризується лінійним ланцюжком - С-С-С, тому він є дірочним напівпровідником. Основні властивості його такі:
Густина – 2,52 г/см3 .
Температура плавлення -2350 °С.
Мiкротвердість - 49500 МПа.
Температура кипіння -3500 °С.
Теплота утворення з елементів - 512 КДж/моль.
Теплопровідність
при 100
![]() С
-121-67
Вт/мк.
С
-121-67
Вт/мк.
Питомий
електроопір,
при температурі
20
оС
-10![]() Ом
Ом![]() м
м
2.3. Одержання карбідів
До основних методів одержання карбідів належать:
1. Прямий синтез з елементів.
2. Відновлення оксидів металів вуглецем з одночасною карбідизацією дуговим,електрошлаковим, газополуменевим чи індукційним методами.
3.Метод високотемпературного синтезу, що самопоширюється.
4. Плазмохімічний метод.
5.Осадження з газової фази.
6.Електроліз з розплавлених середовищ.
Прямий
синтез
оснований на взаємодії металів чи
неметалів з вуглецем при високих
температурах. Для цього беруть порошок
металу і сажу у співвідношеннях,
необхідних для одержання карбіду
потрібного складу за реакцією Me + ХС =>
Me C![]() ,де
0,5<х
,де
0,5<х![]() 1.
Зі зменшенням величини частинок металу
і сажі реакція відбувається швидше.
1.
Зі зменшенням величини частинок металу
і сажі реакція відбувається швидше.
Для одержання рівномірної суміші порошки змішують, наприклад, у кульових млинах 1-2 год. Потім суміш просівають на ситах із сіткою №08, брикетують на механічних пресах, щоб зменшити обсяг шихти і для поліпшення контакту між частинками. Температура процесу одержання основних карбідів наведена в табл.2.3.
Таблиця 2.3
Температура процесу одержання основних карбідів
Реакція одержання карбіду |
Температура одержання °С |
Реакція одержання карбіду |
Температура одержання ,°С |
Ti+C TiC Zr+C ZrC Hf+C HfC V+C VC Nb+C NbC |
1400 – 1550 1400 – 1600 1500 – 1600 1400 – 1500 1400 - 1700 |
Ta+C TaC 3Cr+2C Cr3C2 7Cr+3C Cr7C3 2Mo+C Mo2C W+C WC |
1200 – 1600 1500 – 1600 1400 – 1450 1200 – 1400 1400 – 1600 |
У середовищі аргону |
|
У середовищі аргону |
|
Цей процес грунтується на дифузії вуглецю в металах і стає помітним лише при температурах вище за 1000 °С.
У вакуумних печах процес відбувається швидше. У середовищі водню він теж вище через утворення ацетилену
2С+Н2 С2Н2 ,
який взаємодіє з металом, утворюючи карбіди
C2H2 + 2 Me 2МеС + Н2,
Метод відновлення оксидів металів вуглецем з одночасною карбідизацією.
Тут одночасно відбувається відновлення металу вуглецем і взаємодiя металу, що утворився, з надлишковим вуглецем за реакцією
МеО2 + ЗС МеС + 2СО.
Наприклад:
TiО2 + ЗС TiС + 2СО , t = 2000 °C - аргон;
ZrO2 + ЗС ZrC + 2СО, t = 2000 °С - аргон;
Nв2O5 + 7С 2NвC+ 5CO, t = 1900 °С - аргон;
WO3 + 4С WC + ЗСО, t=1500 °С - аргон.
Одержання карбідів методом самопоширюваного високотемпературного синтезу (СВС)
Цей метод грунтується на реакціях екзотермічної взаємодії двох чи декількох елементів.
Для здійснення процесу СВС використовують порошки металiв розміром 50 мкм і сажі до 1 мкм. Чим менше розмір частинок тим інтенсивніше і повніше відбувається синтез.
Для одержання тонких порошків великі порошинки пластичних металів Ti, Nb, Мо, Zr гiдрують. Гідриди, що утворилися, крихкі. Їх подрібнюють, а потім дегідрують.
Реактор являє собою циліндричну герметичну судину, здатну працювати у вакуумі (1Па) і витримувати тиск до 1ГПа.
Внутрішню поверхню судини викладають вогнетривким матеріалом, найчастіше графітом.
Після завантаження реактора і його герметизації роблять локальне нагрівання шихти з потужністю не менше ніж 40 Дж/смс, а тривалість нагрівання становить не менше ніж 5 с.
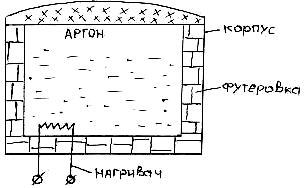
Рис. 2.1. Схема реактора СВС
Тепло реакції нагріває холодні шари i вони починають реагувати передаючи тепло екзотермічної реакції більш холодним шарам. Швидкість поширення фронту горіння становить 0,5 -15 м/с, а температура від 2000 до 4000 °С.
Одержання карбідів плазмохімічним методом
Температура плазми коливається від 10000 до 30000 °С. Якщо в плазму вдувати порошки металів, оксидів, галогенідів, а також вуглецевовмiсних газiв чи пари, наприклад СН4, то відбувається їхня атомізація й іонізація. Елементи в стані плазми дуже активні і швидко утворюють різні з'єднання в тому числі і карбіди.
При швидкому їхньому охолодженні утворюється твердий карбід металу чи неметалу. Метод малопродуктивний. У дуговому плазмотроні використовують електроди із суміші металу і вуглецю – віцей метод більш продуктивний.
Одержання карбідів осадженням з газової фази
Цей процес відбувається на нагрітій підкладці в результаті взаємодії галогенідів з вуглецевомісними газоподібними речовинами. Схема такої реакції має вигляд
nMeClx + CnHm nMeC + nxHCl + [m-nx]/2H2.
Наприклад: SiCl4 + СH4 SiC + 4НСl t = 1100 °С ;
TiCl4 + СН4 TiC + 4НСl t = 1000 °С ;
NbCl5
+
СH4
+
![]() H2
NbC
+
5НСl
-
в
середовищі водню
t =
600 °С.
H2
NbC
+
5НСl
-
в
середовищі водню
t =
600 °С.
Реакції в середовищі водню відбуваються при більш низьких температурах.
Одержання карбідів електролізом
Процес
здійснюють при силі струму 20А i температурі
розплавле-них солей бури. Так для
одержання WC
використовують такі компоненти: Na2OB2O3
+ 2Na
CO![]() + 4,5LiF
+ 0,15WO3.
Шар карбіду вольфраму осаджується на
графітовому катоді.
+ 4,5LiF
+ 0,15WO3.
Шар карбіду вольфраму осаджується на
графітовому катоді.
Лекція 3. Структура, властивості і методи одержання нітридів
3.1. Структура і властивості нітридів
Високими характеристиками, такими як зносостійкість, твердість, жаростійкість, хімічна стійкість володіють нітриди перехідних металів, а також кремнію і бору.
Деякі властивості їх наведені в табл. 3.1.
Таблиця 3.1
Структура і властивості металоподібних нітридів
Нітрид |
Кристалічні ґратки |
Область гомогенності, % ат.частки |
, т/м3 |
Тпл ОС |
Н , МПа |
Омм |
Е 10 МПа |
|
TiN ZrN HfN V3N VN Nb2N NbN Ta2N TaN Cr2N CrN Mo2N WN |
ГЦК ГЦК ГЦК ГПУ ГЦК ГПУ ГПУ ГПУ ГПУ ГПУ ГЦК ГЦК ГЦК |
37,5-50,0 46 – 50 ------- 25 – 33 41 - 50 28,5 –33,5 50,0 – 50,6 28,5 – 31,0 44,5 – 47,3 32 – 33 ------- 32 – 33 ------- |
5,43 7,09 13,84 5,97 6,04 8,23 8,40 15,81 15,46 6,51 6,14 9,44 -----
|
3200 2980 3000 ------- 2050 2450 2300 2050 3087 1650 1500 895 Розклада-єтся при Т >>700 °С |
2000018500 21500 19000 15200 17200 16500 12200 10800 15700 10930 6300 ------- |
25 21 33 123 85 142 78 263 128 84 640 20 ----- |
3,9 – 5,0 3,0 – 4,5 4,8 ----- 3,5 – 4,6 ----- 4,0-4,836 ----- 5,758 3,10 3,198 ------ ------ |
294,34 342,96 345,45 -------- 192,01 ----- 194,83 242,83 223,85 -------- ------- --------- --------- |
Металоподібні нітриди є провідниками з високою теплопровідністю. Структурно вони являють собою сполуки з азотом на основі фаз втiлення з кубічною і гексагональною структурами. Пластичність їх вище, ніж інших тугоплавких сполук (карбідів, боридів, силіцидів). Характерним для металоподібних нітридів є широка область гомогенності. Наносяться у вигляді покрить газо фазними, вакуумними, iонно-плазмовими методами.
3.2. Нітриди неметалів і алюмінію
Крім нітридів перехідних металів широке застосування мають нітриди неперехідних металiв алюмінію, а також неметалів кремнію і бору. Вони відрізняються високою зносостійкістю (крім гексагонального BN), високою стійкістю в агресивних середовищах, значною термостійкістю при швидких теплозмінах і високою вогнестійкістю. Введення в нітриди деяких оксидів підвищує їхнi властивості. Такою є композиція Si3N4 – Ai2O3, яку називають "СIАЛОН" . Si3N4 – Ai2O3 – TiC має торгову марку "силiнiт" і є дуже перспективним матеріалом.
Властивості нітридів бору, кремнію й алюмінію наведені в табл. 3.2.
Нітриди кремнію стійкі в розплавах багатьох металів. Вони практично не взаємодіють з розплавленим алюмінієм навіть при 1000 оС, зі свинцем до 400 оС, з оловом до 300 °С, цинком до 550 °С и дуже слабко взаємодіють з рідким Mg при t = 750 °С і міддю при t = 1150 °С.
Таблиця 3.2
Властивості неметалічних нітридів і нітриду алюмінію
Нітрид |
Кристалічна ґратка |
т/м3 |
Tпл (дисоціа- ції), ОС |
Н , МПа |
Е 10 ,МПа |
|
OC-1 |
, кДж/моль
|
AlN |
Гексагональна щільно упакована
|
3,12 – 3,27 |
2400 (розкла- дається) |
12300 |
-------- |
>1013 (при 20ОС) |
4 - 6 |
288,01 |
|
Гексагональна
|
2,29 |
3000 (під тиском азоту) |
1 - 2 (за Моосом) |
0,865 – 0,344 |
1013 (при 20ОС) |
0,5-1,7 |
224,61 |
Si2N4 |
Кубічна Гексагональна
|
3,45 3,18 |
1900 (розкла-дається) |
60000 33000 1200 |
8,09-9,73 3,2 |
Діалект-рик 1013 - 1014 |
2,75 |
675,93 |
Зразки Si3N4 помітно не взаємодіють із соляною, азотною, сiрчаною і фосфорною кислотами в будь-яких концентраціях. Концентрована сірчана кислота практично не діє на нітрид бору BN, а концентрована фосфорна, плавикова, азотна, а також вуглець чотироххлористий, газолін і бензин діють на нього слабко. Не діє на Si3N4 і BN також хлор і сірководень при t 1000 oС, розплави хлоридів натрію і калію при t 800 oС.
3.3. Одержання нітридів
Основні методи одержання нітридів такі:1) азотування металів чи їхніх гідридів; 2) метод СВС; 3) метод плазмохімічного синтезу; 4) відновлення оксидів металів твердим відновлювачем у середовищі азоту (аміаку); 5) осадження нітридів з газової фази.
Азотування металів. Процес здійснюється під впливом азоту, чи аміаку та іншого азотовмісного газу на порошки металів чи їхніх гідридів у муфельних прохідних печах при t = 800 – 1200 °С при безупинній подачі газу протягом 1 - 2 год. Чим дрібніше порошок, тим більше його поверхня і швидше відбувається процес.
Активніше утвориться нітрид у випадку використання амiаку. Це дозволяє одержувати більш тонкі порошки, а при розкладанні виділяється водень, що взаємодіє з киснем, i завжди адсорбується поверхнею порошку, очищає її й активує.
Азотування
в аміаку відбувається за схемою
NН3
N
+
![]() Н2;
Н2;
N+Ti = TiN.
Метод СВС. Як сировину використовують тонкі порошки металів і азот під тиском 1-2 Гпа.
До фронту горіння повинен постійно подаватися азот. Це можливо при великих тисках.
І порошок, і продукт мають бути газопроникні.
При оптимальних умовах проведення СПС відбувається практично повне перетворення вихідних речовин у кінцеве.
Метод плазмохімічного синтезу
Як вихідні матеріали використовують порошки, галогеніди, оксиди, що вводять або в зону розряду, або у високотемпературну плазму.
Як плазмоутворюючі гази використовують: Аг, Не, Н2, N2 та ін. Азот володіє найбільшою питомою теплотою згоряння.
Одержання нітридів відновленням оксидів металів твердим відновлювачем у середовищі азоту
Процес відбувається за реакцією
2MeО+2X+N2 2MeN+2XO,
де Ме - метал; Х - неметалічний відновлювач (вуглець, кремній, бор).
Для зменшення вмісту вуглецю в кінцевому продукті, процес необхідно здійснювати при максимально можливих низьких температурах.
Так, наприклад, при одержанні нітридів титану і ніобію оптимальними є температури відповідно 1250 °С та 1400 °С.
2TiО2 + 4C+N2 2TiN + 4CO, t=1200 °C.
але утворення карбіду титану відбувається при 1600 - 2000 °С, а карбід Nb утворюється при t = 1800-1900 °С за реакцією Nв205 + 5C + N2 2NвN + 5CO.
Тривалість ізотермічної витримки 3 - 4 год, тиск азоту 0,4 МПа і швидкість його подачі 0,18 м/с. У цьому випадку нітрид містить 0,5 - 0,7 % вуглецю, якщо це нітрид титану. А в нітриді ніобію він взагалі відсутнiй.
Одержання нітридів з газової фази здійснюється за однією із наведених реакцій:
2MeCl4 + 2NH3 + H2 2MeN + 8HCl;
2МеOCl2 + 2NH3+Н2 2МеN + 2Н2O + 4НСl;
2MeCl + N2 + H2 2MeN + 2HCl.
Наприклад, 2TiCl4+2NH3 = 2TiN + 6HCl + Cl2, t = 1000 °С.
TiCl4 і NH3 нагрівають до 700 – 900 °С і подають у кварцову трубу через форсунку. Початкова температура в камері повинна бути не нижче 750 – 950 °С, а на виході 1000 -1200 °С. Швидкість руху газів від 2 до 20 м/с.
Нітрид титану відокремлюють від газової суміші електростатичним методом і фільтрацією на керамічних фільтрах. Одержують нітриди 0,1 - 0.6 мкм.
Лекція 4. Будова, властивості і методи одержання боридiв
4.1. Будова і властивості боридiв
Подвійні боридi (наприклад TiВ2 і СrВ2) мають більш високі твердість, зносостійкість і жаростійкість, ніж одинарні.
Зі зростанням спiввідношення бор/метал зменшується питомий електричний опір і коефіцієнт термічного розширення, збільшуються температура плавлення, мікротвердість і поліпшуються інші механічні характеристики. Це свідчить про зміцнення міжатомних зв'язків у ґратках при переході від нижчих боридів до вищих.
При переході від діборидів металів 4-ї групи до діборидів 5-ї, а потім до 6-ї температура плавлення, мікротвердість і модуль пружності зменшуються, а коефіцієнт термічного розширення збільшується.
Бориди застосовують для виготовлення сопел установок, що розпорошують рідкі метали, човників, тиглiв, а також для нанесення захисних покрить наплавленням і газотермічним напилюванням.
Основні властивості боридів наведені в табл. 4.1.
Таблиця 4.1
Структура і властивості боридів
Борид |
Кристалі-чна ґратка |
, т/м3 |
Tпл, ОС |
Н , МПа |
|
OC-1 |
Е 10 , МПа |
кДж/моль |
TiB2 |
Гексагон. |
4,45 |
2980 |
34800 |
9,0 |
4,5 |
5,405 |
319,5 |
ZrB2 |
» |
6,17 |
3200 |
21900 |
9,7 |
5,9 |
4,958 |
323,62 |
HfB2 |
» |
10,5 |
3250 |
29000 |
10,6 |
6,3 |
4,797 |
325,50 |
VB2 |
» |
5,1 |
2400 |
28000 |
22,7 |
7,9 |
3,404 |
--------- |
NbB |
Ромбічна |
7,6 |
2300 |
22000 |
40,0 |
12,9 |
-------- |
--------- |
NbB2 |
Гексагон. |
6,97 |
3000 |
26000 |
25,7 |
7,7 |
6,376 |
--------- |
TaB2 |
» |
11,7 |
3037 |
26000 |
32,5 |
7,9 |
6,867 |
188,25 |
Cr2B |
Ромбічна |
6,5 |
1870 |
13500 |
107,0 |
14,2 |
4,101 |
--------- |
CrB |
» |
6,2 |
2100 |
21000 |
45,5 |
12,3 |
3,606 |
77,04 |
CrB2 |
Гексагон. |
5,6 |
2200 |
22000 |
30,0 |
10,5 |
4,503 |
123,23 |
MoB |
Тетрагон. |
8,8 |
2600 |
23000 – 24500 |
--------
|
------- |
-------- |
70,74 |
WB |
» |
16,0 |
2800 – 2920 |
----- |
--------- |
------- |
-------- |
71,11 |
Структура нижчих боридів, багатих металом, визначається металевою підграткою, а вищих, багатих бором, - атомами бору, що утворюють тверді пiдгратки з ковалентними зв'язками бор-бор у вигляді сіток.
4.2. Одержання боридів
Існує кілька методів одержання боридів:
1. Прямий синтез з елементів.
2. СВС.
3. Металотермічне відновлення.
4. Відновлення оксидів металів бором з одночасним боруванням.
5. Електроліз розплавлених середовищ.
6. Осадження з газової фази,
7. Відновлення оксидів металів карбідом бору.
8.Спільне відновлення оксидів металів іборного ангідриду вуглецем.
9. Метод плазмохімічного синтезу.
При прямому синтезі процес відбувається за реакцією
Me + В МеВ,
яка може здійснюватися як у рідкій фазі шляхом плавлення шихти в дугових і індукційних печах, так і у твердому стані.
СВС - метод одержання боридів аналогічний карбідному і належить до типу «безгазових систем горіння». При наявності чистої суміші процес відбувається при високих температурах (наприклад, ТіВ2 – 2920 °С); при наявності в суміші інертної добавки температура знижується (наприклад, ZгВ2 при чистій суміші 3040 °С, а при наявності інертної добавки t = 2117 – 2667 °C)
Металотермічне відновлення
Як сировину використовують оксиди металів, а відновлювачами служать Al, Mg, Ca ,Si.Реакції відбуваються за схемою
МеО + В3О3 + Аl(Mg, Ca ,Si) МеB + Al( Mg, Ca ,Si)On . Наприклад: V2O5 + B2O3 + 8Mg 2VB + 8MgO;
ТiO2 + B2O3 + 5Mg TiB2 + 5MgO;
Сг2O3 + 2B2O3 + 9Mg 2CrB2 + 9MgO.
Відновлення оксидів металів бором з одночасним бору-ванням.
У цьому випадку процес відбувається за реакцією
3MeO+5B 3MeB+B2O3. Шихту, узяту в стехіометричному співвідношенні, пресують у брикети завантажують у контейнер з ідентичного бориду і поміщають у вакуумну піч
Одержання боридов електролізом
Їх можна одержувати електролізом розплавів, що складаються із сумішей лужних і луго-земельних металів з їхніми оксидами.
В якості флюсів використовують фториди магнію, кальцію та літію.
При електролізі на катоді виділяється елементарний бор який утворюється в результаті відновлення ангідриду бору лужним металом
2 B2О3 + 3Na 3NaВО2 + B.
Поряд з цим відбувається процес відновлення оксиду тугоплавкого металу, що взаємодіє з бором, утворюючи борид
TiО2 + 4Na Ti + 2Na2О; Ti + 2B TiB2.
Одержання боридів осадженням з газової фази.
Боромістким компонентом може бути бромід чи хлорид бору які відновлюються за реакцією
МеClх +n ВCl3 + (х + 3*n)/2Н2 МеB2 + (х + 3*n)НСl
Наприклад: TiCl4 + 2BCl + 5H2 TiB2 + 10HCl .
Одержання боридів відновленням оксидів металів карбідом бору (борокарбідний метод). Метод є одним з основних при промисловому одержанні боридів перехідних металів.
Основою цього методу є реакції типу
2МеО + В4С + С 2МеВ2 + 2СО.
Одержання боридів спільним відновленням оксидів металів і борного ангідриду вуглецем (вуглецевий метод). Цей метод є також одним з основних при виробництві боридів у промислових масштабах. Він оснований на реакції: МеО+В2О3+ 2СМехВу+ 2СО і відрізняється від борокарбідного тим, що як вихідну сировину можуть використовувати більш дешеві матеріали: оксиди, борний ангідрид. Оптимальні температури процесу одержання діборидів: для титану, цирконію і ніобію -1900 °С, гафнію -2000 °С, ванадію і хрому -1800 °С, вольфраму, W2B5 у двох стадіях відновлення при 850 °С -1 год, і утворення бориду при 1600°С - 2 год.
Газополуменевий метод подібний до того,що застосовується при одержанні карбiдів, а також нітридів перехідних металів. Але широкого промислового поширення він не одержав через дорожнечу устаткування і складності технології.
Лекція 5. Структура, властивості і методи одержання силіцидів
5.1. Структура і властивості силіцидів
Силіциди перехідних металів 4…6 груп знаходять широке застосування в літакобудуванні, атомній, ракетній і космічній техниці, головним чином для виготовлення деталей високої жаростійкістi і жароміцностi, а також для одержання захисних покрить. Найбільше застосування одержав дісиліцид молібдену, MoSi2 завдяки доброї елекропровідності і високої стійкості до окислювання. З нього виготовляють електричні нагрівальні елементи і покриття на деталях працюючих на повітрі при температурі до 1600 °С. Властивості дісиліцидів «великої десятки» тугоплавких металів наведені в табл. 5.1
5.2. Методи одержання силіцидів
Даним часом застосовуються такі методи:
1. Прямий синтез з елементів.
2. Одержання силіцидів методом СВС.
3. Відновлення їхніх оксидів з одночасним силіціюванням.
4. Синтез з розчинів у металевих розплавах.
5. Осадження з газової фази.
6. Електроліз розплавлених середовищ.
Таблиця 5.1
Властивості деяких дісилицидів
Матеріал |
Густина
т/м3 |
Tпл ОС |
Н , МПа |
Е 10 ,МПа |
OC-1 |
|
TiSi2 |
4.13 |
1540 |
8920 |
3.551 |
10.3 |
132.15 |
ZnSi2 |
4.86 |
1700 |
10630 |
2.599 |
8.37 |
149.36 |
HfSi2 |
9.03 |
1750 |
9120 |
----- |
------- |
225.94 |
VSi2 |
4.66 |
1660 |
8900 – 9600 |
----- |
12.0 |
148.47 |
NbSi2 |
5.66 |
2100 |
10820 |
2.551 |
10.6 (20-1100OC) |
123.32 |
TaSi2 |
9.1 |
2200 |
14070 |
------- |
10.2 |
116.01 |
CrSi2 |
5.0 |
1500 |
9960 –11500 |
------- |
12.9 (20-700OC) |
98.77 |
MoSi2 |
6.24 |
2030 |
12000-13500 |
4.405 |
8.3 |
118.49 |
Wsi2 |
9.25 |
2165 |
13000-14000 |
5.307 |
7.35 |
91.86 |
Одержання силіцидів прямим синтезом з елементів
Він проводиться з чистих елементів металу і кремнію і оснований
на реакції Me + 2Si MeSi2.
Процес здійснюють у муфельних печах при температурі 100 – 1200 °С, тільки силіцид хрому одержують при більш низьких температурах 900 -1000 °С.
Метод одержання силіцидів СВС
Він такий як і при утворенні боридів по типу безгазового горіння. При цьому процес відбувається постійно через утворення низьких силіцидів з переходом до вищих. Прикладом може служити MoSi2 :
nМо + Si2 Мо3Si2 Mo5Si2 MoSi2.
Одержання силіцидів відновленням з окислів з одночасним силіціюванням. У цьому процесі можливі кілька варіантів:
відновлення оксидів металів кремнієм за реакцією 2MeO + 5Si 2MeSi2 + SiO ;
спільне відновлення оксидів металів і кремнію вуглецем, за реакцією МеО + 2SiO2 + 5C MeSi2 + 5CO;
відновлення оксидів металів карбідом кремнію за реакцією
MeO + 2SiC MeSi2 + CO + C.
Oдержання силіцидів синтезом із простих речовин у металевих розплавах. Тут реакція утворення силіцидів здійснюється в допоміжній металевій ванні з наступним виділенням одержуваного продукту хімічним шляхом.
Метод характеризується порівняно низькими температурами процесу і його простотою.
Метал утворюючий розплавлену ванну має відповідати таким вимогам: 1) при температурах процесу добре розчиняти вихідні матеріали, 2) не взаємодіяти і не утворювати сполуки з кремнієм і відповідним металом, 3) при температурі утворення силіцидів перебуває в рідкому стані і мати невисоку пружність пари, 4) легко і цілком відокремлюватися від утворюючого продукту. Для утворення ванни можуть бути використані такі метали: Al, Bi, Сu, Sn, Pb, Zn, Ag.Практичне застосування одержали: Ag, Al, Сu, Pb, Sn.
Швидкість утворення силіцидів у розплавах свинцю й олова невелика внаслідок деякої розчинності кремнію в них. Однак у цих середовищах реакція проходить більш повно. Стосовно до цинкових розплавів схема утворення силіциду така:
Zn![]() +
Siтв
Zn - Sip
;
+
Siтв
Zn - Sip
;
Zn + Метв MeZn (Meтв);
Sip + MeZn (Метв) MeSip.тв + Znр .
Температура процесу 700 – 900 °С.
Одержання силіцидів осадженням з газової фази.
Силіциди одержують у результаті взаємодії при високих темпе-ратурах порошку металу з кремнієм відновленим з газової фази,
Me + 2SiCl4 + 4H2 Me Sі2+8HCl
З підвищенням температури від 800 до 1200 °С швидкість осадження і вихід продукту збільшується. Процес носить дифузій-ний характер і відбувається постадiйно від низьких силіцидів до вищих.
Наприклад, для силіцидів титану:
Ti+Si Ti5Si3 Ti5Si4 TiSi TiSi2 .
Одержання силіцидів з розплавлених середовищ солей
Використовують розплави фторсиліцидів калію (K2SiF6) чи натрію і солі металевого компонента. Для одержання дiсилiцидiв Ti, Zr, Cr використовують розплави силікатів у суміші з оксидами тугоплавких металів. Силіциди виділяються на катоді у вигляді правильних кристалів. Метод промислового значення не має. Крім перерахованих матеріалів для утворення покрить використовують також деякі окисли, наприклад Аl2О3 - твердість 20000 - 24000ГПа, SiO2 - 11-12ГПа і деякі інші окисли.
Лекція 6. Порошки для газотермічного напилювання. Одержання порошків
6.1. Принцип одержання порошків відновленням
Найпростіша реакція відновлення може бути представлена так:
MeA + X Me + XA – Q,
де Me - будь-який метал, А - неметалічна складова (кисень, хлор,
фтор, сольовий залишок та ін.) відновлюваної хімічної сполуки, Х - відновлювач, Q - тепловий ефект реакції.
Реакція відновлення можлива лише у випадку, якщо при утворенні сполуки відновлювачем ХА виділяється енергії більше ніж при утвореннi сполуки металу МеА за реакцією Me + A MeА+Qo, тобто Q >Qo. Наприклад, при 1000 °С вільна енергія утворення діоксиду цирконію за реакцією Zr + О2 = ZrО2 становить 420 (Кдж/г-ат. кисню), а оксиду кальцію Ca + О2=CaО - порядку 525 (Кдж/г-ат. кисню). Тому Са активно відновлює цирконій з його оксиду за реакцією ZrО2 + 2Ca = Zr + 2CaО.
Але міцність сполуки змінюється з його валентністю. Сполуки металу термічно тим мiцнішi, чим нижча його валентність. Наприклад, оксид титану ТіО значно мiцніший TiO2. Реакції відновлення відбуваються постадійно ТіО2 TiО Ti. Тому в розрахунках необхідно враховувати теплоту утворення самого міцного із з'єднань. У випадку Ti різниця енергій утворення
QMeA – QХА < 0.
Якщо відновлювачем є метал, то процес називають металотермічним.
6.2. Одержання порошків Fe, W, Ti, Ta, Nb
Залiзо відновлюють з окислів або газами водню і моноокисла вуглецю, або чистим твердим вуглецем. У випадку водню реакції йдуть по стадіях: t= 900°-1000°C
ЗFe2O3 + H2 = 2F3O4 + H2O + 7,14 Kдж;
F3O4 + Н2 = 3FeO + Н2O – 63 Kдж;
FeO + H2 = Fe + H2O – 30 Kдж.
Найбільш розповсюджений метод одержання порошку заліза це відновлення його CO, хоча чистота нижче ніж у випадку водню.
Аналогічно відновлюють воднем і інші метали.
WO![]() +
3H
+
3H![]() =
W
+
3H
О,
t=1100
–
1200
°C,
=
W
+
3H
О,
t=1100
–
1200
°C,
а також моноокисом вуглецю:
3WO + 3CO =3W + 3CO2
