
- •Раздел 4.1 даёт возможность познакомиться с элементами теории колебательно-вращательных спектров и научиться извлекать из них необходимую информацию о строении молекул исследуемого газа.
- •4.1. Ик спектры двухатомных молекул в газе
- •4.1.1. Энергетические состояния молекул
- •4.1.2. Колебательные уровни двухатомной молекулы
- •4.1.3. Вращательные уровни двухатомной молекулы
- •4.1.4. Колебательные спектры двухатомных молекул
- •4.2. Методики регистрации ик спектров
- •4.2.1. Ик спектрометры с непрерывной развёрткой
- •4.2.2. Ик Фурье спектрометры
- •4.2.3. Принцип работы ик Фурье спектрометра
- •4.3. Элементы статистической термодинамики
- •4.3.1. Расчёт статсумм
- •4.3.2. Расчёт термодинамических характеристик
- •4.4. Лабораторные работы
- •4.4.1. Работа ик-1. Определение энтропии двухатомных молекул по данным ик-спектроскопии
- •4.4.2. Работа ик-2. Определение константы равновесия реакции 2 no2 n2o4
- •4.5. Контрольные вопросы к работам ик-1 и ик-2
4.5. Контрольные вопросы к работам ик-1 и ик-2
Почему наблюдаемый вами ИК-спектр двухатомной молекулы содержит много линий, хотя у двухатомной молекулы всего одна колебательная степень свободы?
Объясните наблюдаемый вид спектра. Выберите одну из линий в спектре и объясните, какому переходу она соответствует.
Почему в спектре молекулы СО отсутствует Q-ветвь (0–0 переход), а в спектре монооксида азота Q-ветвь наблюдается?
Газообразные CO и CO2 имеют поглощение в ИК области, а O2 – нет. Почему?
Что такое статистическая сумма? Почему поступательная статсумма зависит от объёма?
К чему относятся рассчитанные вами статсуммы: к молекуле или к молю?
Рассчитанные вами термодинамические функции относятся к молекуле или к молю?
Принцип работы ИК-Фурье спектрометра. Порядок работы.
Устройство вакуумной установки.
(К работе ИК-2) При каком общем давлении диоксида азота концентрации мономера и димера становятся равными?
Библиографический список к работам ИК-1 и ИК-2
Мальцев А. А. Молекулярная спектроскопия. М.: Изд-во МГУ, 1980.
Бенуэлл К. Основы молекулярной спектроскопии. М.: Мир, 1985.
Брейсуэлл Р. Н. Преобразование Фурье. В мире науки (Scientific American, издание на русском языке), № 8,, 1989, С. 48.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приложение 4.1
Молекула NO в
основном электронном состоянии имеет
отличную от нуля
![]() проекцию полного орбитального момента
электронов на ось молекулы (
проекцию полного орбитального момента
электронов на ось молекулы (![]() для NO), а также обладает отличным от нуля
полным электронным спиновым моментом
для NO), а также обладает отличным от нуля
полным электронным спиновым моментом
![]() .
Для таких величин S
и Λ
общепринятым обозначением для
молекулярного электронного терма
.
Для таких величин S
и Λ
общепринятым обозначением для
молекулярного электронного терма
![]() является
является
![]() .
Вырождение терма
равно четырём. Это вырождение частично
снимается, если учесть, что при
.
Вырождение терма
равно четырём. Это вырождение частично
снимается, если учесть, что при
![]() орбитальное движение электронов создает
магнитное поле в направлении оси
молекулы, которое вызывает прецессию
спина S
вокруг оси молекулы с сохранением
компоненты спина
орбитальное движение электронов создает
магнитное поле в направлении оси
молекулы, которое вызывает прецессию
спина S
вокруг оси молекулы с сохранением
компоненты спина
![]() вдоль этой оси. В результате, спин-орбитальное
взаимодействие приводит к расщеплению
вдоль этой оси. В результате, спин-орбитальное
взаимодействие приводит к расщеплению
![]() -кратно
вырожденного терма
на двукратно вырожденные по проекции
-кратно
вырожденного терма
на двукратно вырожденные по проекции
![]() полного углового момента электронов
подуровни
полного углового момента электронов
подуровни
![]() ,
являющиеся аналогами атомных мультиплетов
,
являющиеся аналогами атомных мультиплетов
![]() в приближении LS‑связи.
Схема сложения моментов представлена
на рис. 4.14.
в приближении LS‑связи.
Схема сложения моментов представлена
на рис. 4.14.
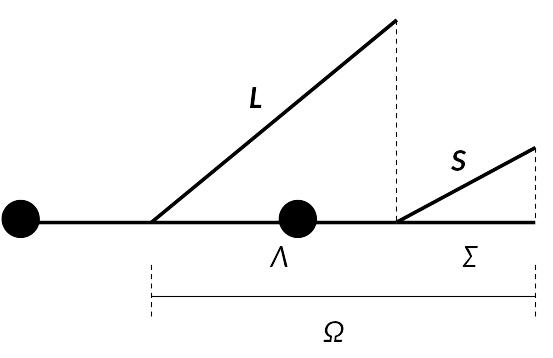
Рис. 4.14. Векторная диаграмма сложения моментов для невращающейся молекулы
Если спин-орбитальное взаимодействие A много больше, чем вращательная постоянная молекулы B, а вращательное число J невелико, то поправка к энергии мультиплетного терма за счёт спин-орбитального взаимодействия и вращения молекулы может быть представлена в виде:
![]() (4.12)
(4.12)
Здесь
![]() задает величину спин-орбитального
взаимодействия,
задает величину спин-орбитального
взаимодействия,
![]() ,
,
![]() ,
,
![]() ,
a
суммарный (за исключением ядерных
спинов) момент вращения молекулы J
может принимать значения
,
a
суммарный (за исключением ядерных
спинов) момент вращения молекулы J
может принимать значения
![]() …
.В случае молекулы NO в основном электронном
состоянии
,
а
,
поэтому реализуются состояния
…
.В случае молекулы NO в основном электронном
состоянии
,
а
,
поэтому реализуются состояния
![]() и
и
![]() .
Если теперь учесть диапазон возможных
значений J
для этих состояний, то формулы 4.12
достаточно для объяснения величины
расстояния 3B
между Q-ветвью
и первыми линиями P-
и R-ветвей
в колебательно-вращательном спектре
NO, а также (при учёте того, что
.
Если теперь учесть диапазон возможных
значений J
для этих состояний, то формулы 4.12
достаточно для объяснения величины
расстояния 3B
между Q-ветвью
и первыми линиями P-
и R-ветвей
в колебательно-вращательном спектре
NO, а также (при учёте того, что
![]() )
для объяснения асимметричного уширения
полосы Q-ветви в области низких частот.
Изложенный здесь механизм сложения
моментов соответствует так называемому
типу связи a
по Гунду. С другими вариантами связи
электронных моментов молекулы с
вращательным моментом ядер можно
ознакомиться, прочитав главу XI
(Двухатомная молекула) из третьего тома
курса теоретической физики Л.Д. Ландау
и Е.М. Лифшица (Квантовая механика.
Нерелятивистская теория).
)
для объяснения асимметричного уширения
полосы Q-ветви в области низких частот.
Изложенный здесь механизм сложения
моментов соответствует так называемому
типу связи a
по Гунду. С другими вариантами связи
электронных моментов молекулы с
вращательным моментом ядер можно
ознакомиться, прочитав главу XI
(Двухатомная молекула) из третьего тома
курса теоретической физики Л.Д. Ландау
и Е.М. Лифшица (Квантовая механика.
Нерелятивистская теория).
Формула 4.12 не
объясняет, наблюдающегося с ростом J
расщепления, линий P-
и R-ветвей
в колебательно-вращательном спектре
NO. Это расщепление является особенностью
![]() состояний (для других
состояний (для других
![]() эффект менее значителен) и называется
-удвое-нием.
Теоретическая интерпретация эффекта
-удвоения
для
эффект менее значителен) и называется
-удвое-нием.
Теоретическая интерпретация эффекта
-удвоения
для
![]() -термов
зависит от величины спина S.
В частности, для применения теории
возмущений оказывается удобным
использовать положительную
-термов
зависит от величины спина S.
В частности, для применения теории
возмущений оказывается удобным
использовать положительную
![]() (не меняющуюся при одновременном
изменении знака координат электронов
и ядер) и отрицательную
(не меняющуюся при одновременном
изменении знака координат электронов
и ядер) и отрицательную
![]() комбинации волновых функций двукратно
вырожденного мультиплета
.
Применительно к молекуле NO достаточно
сложное теоретическое рассмотрение
даёт следующий результат для вращательных
поправок к энергии:
комбинации волновых функций двукратно
вырожденного мультиплета
.
Применительно к молекуле NO достаточно
сложное теоретическое рассмотрение
даёт следующий результат для вращательных
поправок к энергии:
![]() 4.13
4.13
где
![]()
![]() ,
4.14
,
4.14
где
![]()
Для низших
колебательных состояний величины Aυ,
Bυ,
γυ,
pυ
и qυ
можно считать равными соответствующим
величинам для нулевого колебательного
состояния, которые известны из прецизионных
экспериментов (![]() ,
,
![]() ,
,
![]() ,
,
![]() ,
,
![]() ).
Заметим, что при T = 300 К
величина kT
равна 431,6 см–1,
что заметно больше, чем приведённое
выше значение для константы A0,
которая определяет масштаб расщепления
между уровнями
).
Заметим, что при T = 300 К
величина kT
равна 431,6 см–1,
что заметно больше, чем приведённое
выше значение для константы A0,
которая определяет масштаб расщепления
между уровнями
![]() и
и
![]() в молекуле NO.
в молекуле NO.
Согласно формулам
4.13, 4.14 наблюдаемое в эксперименте
-удвоение
связано с различной энергией уровней
![]() и
и
![]() .
Формула 4.14 не предсказывает расщепления
(-удвоения)
для уровней
.
Формула 4.14 не предсказывает расщепления
(-удвоения)
для уровней
![]() ,
однако небольшое расщепление все же
существует, оно связано с неучтёнными
в формуле 4.14 поправками теории возмущений
более высокого порядка. Более того,
формулы 4.13, 4.14 применимы только при
условии
,
однако небольшое расщепление все же
существует, оно связано с неучтёнными
в формуле 4.14 поправками теории возмущений
более высокого порядка. Более того,
формулы 4.13, 4.14 применимы только при
условии
![]() .
С ростом J
происходит всё более увеличивающееся
(за счёт Bυ,
γυ
и qυ)
смешивание состояний
и
.
С ростом J
происходит всё более увеличивающееся
(за счёт Bυ,
γυ
и qυ)
смешивание состояний
и
![]() ,
а также состояний
и
,
а также состояний
и
![]() .
Кроме того, ко всем этим состояниям
начинают примешиваться функции
возбуждённых электронных состояний,
главным образом,
.
Кроме того, ко всем этим состояниям
начинают примешиваться функции
возбуждённых электронных состояний,
главным образом,
![]() ‑типа.
Это соответствует постепенному переходу
от связи типа a
к связи типа b
по Гунду.
‑типа.
Это соответствует постепенному переходу
от связи типа a
к связи типа b
по Гунду.
Приложение 4.2
Свойства двухатомных молекул
Молекула |
|
|
re, Å |
I1047, кг м2 |
Be, см–1 |
H2 |
4396,554 |
117,973 |
0,741 |
0,46 |
60,87 |
O2 |
1579,78 |
11,699 |
1,207 |
19,35 |
1,447 |
CO |
2169,812 |
13,289 |
1,128 |
14,5 |
1,93 |
H35Cl |
2990,95 |
52,819 |
1,275 |
2,64 |
10,606 |
NO |
1904,40 |
14,187 |
1,151 |
16,42 |
1,705 |
– волновое число собственных колебаний, – коэффициент ангармоничности, re – равновесное межъядерное расстояние, I – момент инерции, Be – вращательная постоянная.
1 См. раздел 4.1.4.
2 О расчёте статсумм и термодинамических функций см. раздел 4.3.
