
- •1. Общий порядок оформления работ по синтезу органических соединений
- •2. Порядок заполнения таблицы «Расчет синтеза»
- •3. Порядок заполнения таблицы «Сводная таблица результатов синтеза»
- •4. Галогенирование
- •4.1. Бромистый этил (бромэтан)
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы
- •4.2. Бромистый бутил (1-бромбутан)
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция галогенпроизводных
- •Контрольные вопросы и задания
- •5. Нитрование
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •5.2. Нитрометан
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •6. Сульфирование
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •6.3. Сульфаниловая кислота
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7. Ацилирование
- •7.1. Ацетанилид
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7.2. Аспирин (о-ацетоксибензойная кислота)
- •Посуда и приборы
- •Методика синтеза
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •7.4. Этилформиат
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •9. Диазотирование
- •9.1. Фенол
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •9.2. Йодбензол
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •10. Красители
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Контрольные вопросы
- •10.2. Метиловый оранжевый
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.3. Малахитовый зеленый
- •Посуда и приборы
- •Химизм получения малахитового зеленого
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.4. Фенолфталеин
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •10.5. Флуоресцеин
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •11. Щелочное плавление
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительная реакция
- •Контрольные вопросы
- •12. Реакции Канниццаро
- •12.1. Бензойная кислота и бензиловый спирт
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •12.2. Бензиловый спирт
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •13. Окисление
- •13.1. Ацетон
- •Посуда и приборы
- •Методика синтеза
- •Физические свойства
- •Отличительные реакции
- •Контрольные вопросы
- •Библиографический список
- •Лабораторный практикум по органическому синтезу
- •1 70026, Тверь, наб. Афанасия Никитина, 22
Посуда и приборы
Для синтеза метилового оранжевого, шт.:
-
Стакан В-1-400 ТС . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Стакан В-1-100 ТС . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Термометр СП-4 (0±50) . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Мешалка механическая . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Баня ледяная . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Пробка резиновая № 29 . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Штатив . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
1
Прибор для синтеза метилового оранжевого представлен на рис. 43. Установку снабжают термометром (для контроля температуры в реакционном стакане), механической мешалкой (для центровки стеклянную мешалку пропускают через резиновую пробку, диаметр которой бóльше диаметра мешалки) и ледяной баней.
а
б
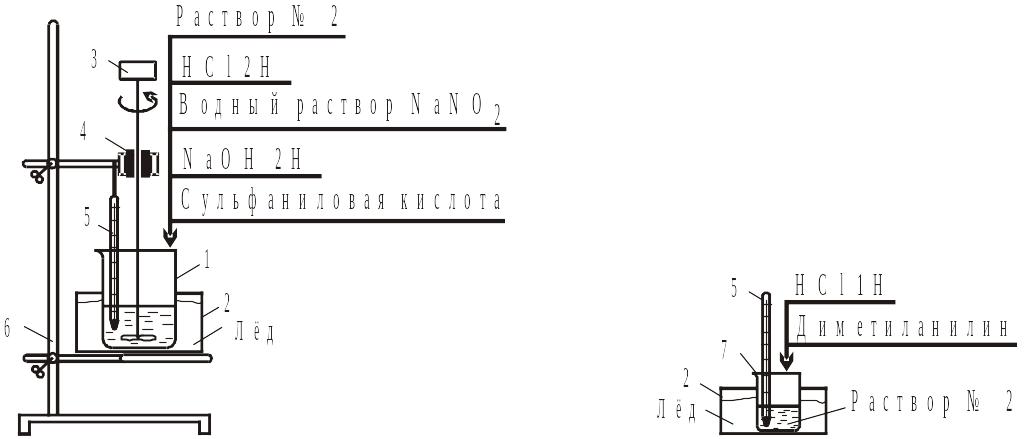

Рис. 43. Прибор для синтеза метилового оранжевого:
а – приготовление раствора № 1; б – приготовление раствора № 2; 1, 7 – стакан; 2 – баня ледяная; 3 – мешалка механическая; 4 – пробка резиновая; 5 – термометр; 6 – штатив
Методика синтеза
Раствор № 1. В стакан емкостью 400 мл, снабженный механической мешалкой (рис. 43), помещают 5 г сульфаниловой кислоты в 12 мл 2н раствора гидроксида натрия, прибавляют 2 г нитрита натрия, растворенного в 24 мл воды. Полученную смесь охлаждают льдом и к ней приливают при перемешивании 12 мл 2н соляной кислоты.
Раствор № 2. Отдельно в небольшом стакане растворяют 5 г свежеперегнанного N,N-диметиланилина в 50 мл 1н соляной кислоты и охлаждают раствор в бане со льдом до 0–5ºС.
Затем к раствору № 1 приливают при перемешивании раствор № 2 и добавляют 2н раствор гидроксида натрия до щелочной реакции по универсальному индикатору. Натриевая соль красителя выделяется в виде оранжево-желтых листочков. После 1,5–2-часового стояния краситель отфильтровывают на воронке Бюхнера (см. рис. 15).
Получают 4 г красителя.
Физические свойства
Метиловый оранжевый (метилоранж, оранж III, гелиантин, 1-(п-диметиламинофенилазо)-4-бензолсульфакислый натрий) – кристаллическое вещество оранжевого цвета:
![]()
Молярная масса 327,34.
Гелиантин является одним из общеупотребительных кислотно-щелочных цветных индикаторов.
Отличительная реакция
В щелочной среде гелиантин имеет желтый цвет, в нейтральной – оранжевый, а в кислой – красный. Он изменяет цвет при рН = 3,2–4,4 вследствие превращения одной хромофорной группы
![]()
( хиноидной группировки) в другую (–N=N– азогруппу).
Красный гелиантин имеет хиноидную группировку
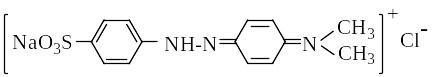
.
П ри прибавлении к нему щелочи образуется желтый гелиантин с азогруппой
.
