
- •ХимичесКая кинетика и катализ
- •3. Влияние температуры на скорость химической реакции.
- •5. Формула Максвелла – Больцмана (самостоятельно).
- •6. Катализаторы и каталитические процессы.
- •3. Влияние t0 на скорость химической реакции Сл 4(0).
- •4. Энергия активации.
- •6. Катализаторы и каталитические процессы
- •2.3.2 Автокатализ.
- •2.3.3 Гетерогенный катализ.
- •Самостоятельно
- •1. Классификация химических реакций.
- •5. Формула Максвелла - Больцмана
- •Уравнение ** можно переписать для константы скорости реакции:
ХимичесКая кинетика и катализ
1. Классификация химических реакций (самостоятельно).
2 Скорость химической реакции.
3. Влияние температуры на скорость химической реакции.
4. Энергия активации.
5. Формула Максвелла – Больцмана (самостоятельно).
6. Катализаторы и каталитические процессы.
2. Скорость химических реакций.
Под скоростью химической реакции понимается изменение концентрации реагирующих веществ в единицу времени.
Ч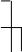
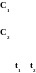
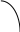

 тобы
вычислить u
реакции нужно определить, насколько
изменилась концентрация одного из
реагирующих веществ в единицу времени
(рис.
1 СЛ. 1(0)).
тобы
вычислить u
реакции нужно определить, насколько
изменилась концентрация одного из
реагирующих веществ в единицу времени
(рис.
1 СЛ. 1(0)).
Рис. 1.
СЛ. 1(1) Dt=t2-t1, -DC=C2-C1 Þ u= -DC/Dt
Знак минус говорит о том, что с уменьшением С скорость тоже уменьшается. Если u рассчитывается по одному из продуктов реакции, то u=DC/Dt . Несмотря на знак минус в уравнении u считается положительной величиной.
Более применимое вычисление скорости хим. реакции вытекает из закона действия масс СЛ.2(0).
Согласно этому закону u~ концентрации реагирующих веществ в данный момент времени. СЛ. 2 (1)Для реакции А®В, u может быть выражена следующим кинетически уравнением: u=КСА, где СА - концентрация вещества А в данный момент времени, К - коэффициент пропорциональности - константа u химических реакций.
Сл. 2 (2) При взаимодействии 2х и более веществ mA + nB ®pC + gD, математическое выражение скорости будет: u=KCAmCBn. т.е. u химических реакций прямо пропорциональна произведению реагирующих веществ, стехиометрические коэффициенты входят в уравнения в виде степени при соответствующей концентрации.
Константа u химической реакции не изменяется при изменении концентраций реагирующих веществ. Иногда К называют удельной скоростью реакции, т.е. при СА = СВ = 1, К = u.
Константа скорости зависит от природы реагирующих веществ, t0, присутствия примесей (в том числе катализаторов), от среды в которой протекает реакция.
Чем больше константа скорости, тем быстрее идет реакция.
Обобщая можно сделать следующий вывод:
Скорость химической реакции пропорциональна концентрации реагирующих веществ: СЛ. 3:
![]()
Где:
СА, СВ – молярные концентрации реагентов в любой момент времени моль/л,
a, b – стехиометрические коэффициенты,
а – порядок реакции по веществу А,
b – порядок реакции по веществу В,
а + b –общий кинетический порядок реакции. Общий порядок простой реакции совпадает с ее молекулярностью.
k – константа скорости химической реакции.
3. Влияние t0 на скорость химической реакции Сл 4(0).
Опыт показывает, что с повышением t0 скорость химических реакций возрастает. Сл 4(1) В уравнении химической кинетике u=КCАСВ влияние t0 включает в себя К. С увеличением t0 возрастает К Þ и возрастает u.
Сл 4(2). Если через Кt - конст. при t0 = t0, а Kt+10 при t0=t0+10 его, то отношение величины первой называется температурным коэффициентом скорости реакции (g), g= Kt+10/ Kt.
Сл 4(3). Согласно эмпирическому правилу Вант-Гоффа g колеблется от 2 до 4, т.е. повышая t0 на 100 u возрастает в два- четыре раза.
Сл 4(4). Пример если g = 2, t0 + 1000, то скорость реакции увеличится в 1024 раза, т.е.
Kt+100/ Kt=g10=210=1024.
Обобщение – СЛ.5.
увеличение температуры в арифметической прогрессии, влечет за собой увеличение скорости реакции, в геометрической.
Х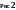


 отя
из правила Вант-Гоффа коэффициент g
должен быть постоянным для каждой
химической реакции, это справедливо
лишь на очень узком интервале температур.
При значительных перепадах температуры
g
значительно уменьшается при увеличении
температуры (рис.
2 СЛ. 6).
отя
из правила Вант-Гоффа коэффициент g
должен быть постоянным для каждой
химической реакции, это справедливо
лишь на очень узком интервале температур.
При значительных перепадах температуры
g
значительно уменьшается при увеличении
температуры (рис.
2 СЛ. 6).
Точная зависимость К скорости реакции от t0 была найдена Аррениусом. СЛ.7(0) Уравнение Аррениуса имеет вид: lnK=B - A/T, где К - константа u реакции; А и В - постоянные характерные для данной реакции; Т - температура.
к
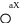
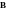

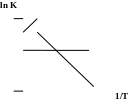
 ак
видно из уравнения lnК обратно пропорционален
Т. Коэффициенты А и В находят графически
(рис.
3 СЛ.7(1)).
ак
видно из уравнения lnК обратно пропорционален
Т. Коэффициенты А и В находят графически
(рис.
3 СЛ.7(1)).
