
- •12. Элементы органической
- •12.1. Введение
- •12.2. Особенности органических соединений
- •12.3. Тип химических связей и валентность углерода в органических соединениях
- •12.4. Основные положения теории
- •Химического строения органических
- •Соединений
- •А. М. Бутлерова
- •Изомерия положения функциональной группы:
- •III. В молекулах органических веществ атомы и группы атомов влияют друг на друга. Это взаимное влияние определяет свойства веществ.
- •12.5. Классификация органических
- •12.6. Номенклатура органических соединений
- •12.8. Углеводороды
- •12.8.1. Классификация углеводородов
- •12.8.2. Алканы (парафины) Определение, общая формула
- •Изомерия и номенклатура алканов
- •Химические свойства алканов
- •II. Реакции окисления
- •IV. Реакции крекинга алканов
- •V. Изомеризация
- •Получение алканов
- •Применение
- •12.8.2. Алкены (олефины, этиленовые ув) Определение, общая формула
- •I. Реакции присоединения
- •III. Реакции полимеризации
- •IV. Изомеризация.
- •V. Реакции замещения
- •Получение
- •Реакции присоединения
- •12.8.4. Алкины (ацетиленовые ув)
- •Изомерия и номенклатура
- •Химические свойства
- •II.Реакции окисления
- •III. Реакции полимеризации
- •IV. Реакции замещения атомов «н», связанных с sp-гибридизованными атомами углерода
Реакции присоединения
Например, присоединение галогенов:
СН2= СН–СH=СН2 + Br2 → СН2– СН=СH–СН2 + Br2 →
Бутадиен-1,3 (H2O) ׀ ׀ (H2O)
Br Br
1,4-Дибромбутен-2
СН2–СН–СH–СН2
׀ ׀ ׀ ׀
Br Br Br Br
1,2,3,4-Тетрабромбутан
Бромная вода обесцвечивается.
Обычно присоединение происходит по концам молекулы бутадиена-1,3, π-связи разрываются, к крайним атомам углерода присоединяются атомы брома, а свободные валентности образуют новую π-связь, т. е. в результате присоединения происходит перемещение двойной связи. При избытке брома может быть присоединена еще одна молекула его по месту образовавшейся двойной связи.
2. Реакции полимеризации:
кат. t°
nСН2= СН–СH=СН2 → (–СН2– СН=СH–СН2–)n
Бутадиен-1,3 Бутадиеновый каучук
Способы получения
I. Получение бутадиена-1,3:
1) Дегидрирование и дегидратация этанола (реакция Лебедева):
425°С
2СН3–СН2–ОН → СН2= СН–СH=СН2 + Н2 + 2Н2О
Al2O3, ZnO,
2) Дегидрирование н-бутана или бутена-1:
500–600°С
С Н3–СН2–СH2–СН3
СН2=
СН–СH=СН2
+ 2Н2
Н3–СН2–СH2–СН3
СН2=
СН–СH=СН2
+ 2Н2
Al2O3, Cr2O3
С H2=СН–СН2–СН3 500–600°С СН2= СН–СH=СН2 + Н2
MgO, ZnO
II.Получение изопрена
CH3 CH3
׀ t° ׀
CH3– CH2– CН–CH3 CH2= C–CН=CH3 + 2H2
Al2O3, Cr2O3
2-Метилбутан Изопрен
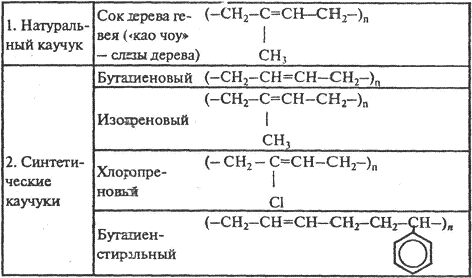
КАУЧУКИ
Каучуки — природные или синтетические продукты полимеризации некоторых диеновых углеводородов с сопряженными связями. Важнейшими физическими свойствами каучуков являются:
эластичность (т. е. способность восстанавливать форму);
непроницаемость для воды и газов.
Получение бутадиенового каучука ( метод Лебедева):

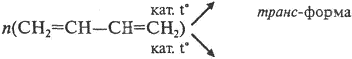

12.8.4. Алкины (ацетиленовые ув)
Алкины
— это углеводороды, в молекулах которых
два атома углерода находятся в состоянии
sp-гибридизации
и связаны друг с другом тройной связью:
–C![]() C–
(табл.1.)
C–
(табл.1.)
Общая формула: СnH2n–2 где n ≥ 2.
Длина связи C C в алкинах равна 0,120 нм.
Каждый атом углерода в состоянии sp-гибридизации связан с двумя другими атомами и может присоединять еще два атома.
Гомологический ряд
-
Молекулярная формула алкина СnH2n–2
Название алкина
Международная номенклатура
Рациональная номенклатура
С2Н2
Этин
Ацетилен
С3Н4
Пропин
Метилацетилен
С4Н6
Бутин
С5Н8
Пентин
