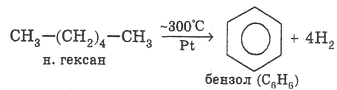- •12. Элементы органической
- •12.1. Введение
- •12.2. Особенности органических соединений
- •12.3. Тип химических связей и валентность углерода в органических соединениях
- •12.4. Основные положения теории
- •Химического строения органических
- •Соединений
- •А. М. Бутлерова
- •Изомерия положения функциональной группы:
- •III. В молекулах органических веществ атомы и группы атомов влияют друг на друга. Это взаимное влияние определяет свойства веществ.
- •12.5. Классификация органических
- •12.6. Номенклатура органических соединений
- •12.8. Углеводороды
- •12.8.1. Классификация углеводородов
- •12.8.2. Алканы (парафины) Определение, общая формула
- •Изомерия и номенклатура алканов
- •Химические свойства алканов
- •II. Реакции окисления
- •IV. Реакции крекинга алканов
- •V. Изомеризация
- •Получение алканов
- •Применение
- •12.8.2. Алкены (олефины, этиленовые ув) Определение, общая формула
- •I. Реакции присоединения
- •III. Реакции полимеризации
- •IV. Изомеризация.
- •V. Реакции замещения
- •Получение
- •Реакции присоединения
- •12.8.4. Алкины (ацетиленовые ув)
- •Изомерия и номенклатура
- •Химические свойства
- •II.Реакции окисления
- •III. Реакции полимеризации
- •IV. Реакции замещения атомов «н», связанных с sp-гибридизованными атомами углерода
II. Реакции окисления
При обычных условиях алканы устойчивы к действию окислителей (КМп04, К2Сг207).
1.Окисление кислородом воздуха при высоких температурах (горение):
а) полное окисление (избыток 02) с образованием углекислого газа и воды. Алканы горят на воздухе с выделением большого количества тепла. Поэтому природный газ, главным компонентом которого является метан СН4, используется в быту и в промышленности в качестве высококалорийного топлива:
-4 T +4
CH4 + 2O2 → CO2 + 2H2O
б) неполное окисление (недостаток 02):
-4 T +4
2CH4 + 3O2 → 2CO + 4H2O
-4 T 0
CH4 + O2 → C + 2H2O
2. Окисление кислородом воздуха при невысоких температурах в присутствии катализаторов (неполное каталитическое окисление).
O
![]()
В результате могут образоваться альдегиды R— С ,
H
кетоны R—С — R , спирты ROH, карбоновые кислоты RCOOH.
![]()
O
Неполное окисление может происходить без разрыва углеродной цепи (число атомов «С» в молекуле продукта реакции равно числу атомов «С» в молекуле исходного алкана) и с разрывом углеродной цепи (число атомов «С» в молекуле продукта реакции меньше, чем в молекуле исходного алкана).
Например, при каталитическом окислении метана в зависимости от природы катализатора и условий проведения реакции могут образоваться следующие продукты:
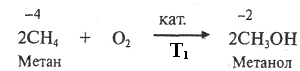
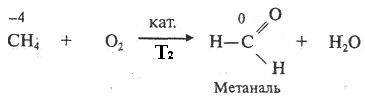

Метановая кислота
О О
KMnO4
CH3–CH2–CH3 –––→ CH3– C + HC + CO2
T4 OH OH
III. Реакции дегидрирования и дегидроциклизации.
При дегидрировании простейшего алкана - метана - в зависимости от условий образуются либо свободный углерод (в виде сажи), либо простейший алкин — этин:
1200°C
CH4 → C + 2H2
1000°C
2CH4
→ HC![]() CH
+ 3H2
CH
+ 3H2
этин (ацетилен)
При дегидрировании гомологов метана в присутствии катализаторов образуются алкены; например:
T
СН3–СН2–СН2–СН3 → СН3–СН=СН–СН3 + H2
Cr2 O3
Дегидрирование алканов с n ≥ 6 при определенных условиях может сопровождаться циклизацией с образованием ароматических УВ (бензола и его гомологов):