
304- Органическая химия_Черных В.П. и др_Х., 2007 -776с
.pdf
ВВедение В органическую химию
21
квыводу о тетраэдрической направленности связей атома углерода в пространстве (четыре валентности атома углерода направлены
куглам тетраэдра, в центре которого находится углеродный атом).
Свое дальнейшее развитие теория химического строения получила с введением в органическую химию электронных представлений. В 1916 году американским ученым Гильбертом Ньютоном Льюисом была предложена электронная теория химической связи (так называемая теория электронных
пар), согласно |
которой |
химическая |
связь |
Фридрих август кекуЛе |
|||||
в органических |
соединениях представлена |
||||||||
парой электронов, выделяемых по одному |
|
|
(1829—1896) |
|
|||||
|
|
|
|
|
|||||
каждым из связываемых атомов. Кроме того, |
Немецкий химик-органик. Науч- |
||||||||
Г. Н. Льюис высказал предположение, что |
ные интересы — теоретическая ор- |
||||||||
электронная пара, участвующая в образо- |
ганическая |
химия и |
органический |
||||||
вании химической связи, может смещаться |
синтез. |
Предложил |
циклическую |
||||||
к одному из атомов. Эта мысль оказалась |
структурную формулу бензола (1865). |
||||||||
Синтезировал тиоуксусную |
(1854), |
||||||||
чрезвычайно важной и была положена в ос- |
|||||||||
гликолевую (1856) кислоты, трифе- |
|||||||||
нову теории электронных смещений. В ра- |
нилметан |
(1872), антрахинон |
(1878). |
||||||
ботах Роберта Робинсона (1922), а позднее |
Предложил методы синтеза тиофена. |
||||||||
Кристофера Ингольда |
(1926—1934) |
были |
|||||||
Высказал (1857) мысль о валентности |
|||||||||
введены и развиты представления о смеще- |
как о целом числе единиц сродства, |
||||||||
нии электронов в простых связях (индук- |
которым обладает атом. Президент |
||||||||
тивный эффект) и кратных (мезомерный |
Немецкого |
химического общества |
|||||||
эффект). Теория электронных смещений по- |
(1878, 1886, 1891). |
|
|
||||||
лучила довольно широкое распространение
ворганической химии, поскольку она позволяет установить зависимость между электронным строением и реакционной способностью органических соединений. Новым этапом в развитии теории химического строения явилось применение
в30-х годах прошедшего столетия в органической химии квантовой механики. В это время разработаны квантово-механические методы описания структуры молекул — метод молекулярных орбиталей (Джо Эдвард Леннард-Джонс, Роберт Сандерсон Малликен, Фридрих Хунд, 1928—1932) и метод валентных связей (Лайнус Карл Полинг, Джон Кларк Слейтер, 1931—1934). Используя метод валентных связей, американский физик и химик Л. Полинг разработал теорию резонанса, которая позволила объяснить многие свойства ароматических систем. С помощью метода молекулярных орбиталей немецкий химик и физик Эрих Хюккель дал объяснение устойчивости ароматических систем и сформулировал теоретически обоснованное правило, позволяющее предсказать, будет система ароматической или нет (правило Хюккеля). Интенсивному развитию квантовомеханических исследований способствовало появление в 60-х годах XX века элек- тронно-вычислительной техники.

Глава 1
22
1.4. СПОСОБЫ ИЗОБРАЖЕНИЯ ОРГАНИЧЕСКИХ МОЛЕКУЛ
структурная формула. Структурная (графическая) формула отражает природу атомов, входящих в состав молекулы, их число и последовательность связывания, а также тип связей между ними.
Химические связи в структурной формуле условно принято обозначать валентным штрихом:
H |
H H |
H |
H |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
H |
|
H |
||||
H—C—C—C—H |
H—C—C—H |
H |
|
H |
|
|||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
— |
C |
|
H—C—C—C—H |
||||
H |
|
H |
|
|
|
|||||||||
|
|
|
|
|
|
С |
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H—C—H |
|
H |
|
H |
|
|
|
|
|
|||||
H |
H |
|
H |
О H |
||||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
H |
|
|
|
|
|
|
|
|
|
|
||
|
|
изобутан |
циклопропан |
этилен |
|
|
|
ацетон |
||||||
Для удобства записи часто используют сокращенную структурную формулу, в которой часть связей не обозначается, а приводятся лишь те, которые необходимы для однозначного описания структуры молекулы:
CH3—CH—CH3, или (CH3)2CHCH3
CH3
изобутан
CH3—C—CH3, или CH3CОСH3
О
ацетон
О
CH3—C 
О, или (CH3CО)2О
CH3—C
О
уксусный ангидрид
Существует также упрощенный способ написания структурных формул, заключающийся в том, что углеродный остов молекулы изображают только посредством валентных связей без обозначения атомов углерода и связей С—Н. Предполагают, что координационное число каждого углеродного атома дополняется до четырёх атомами водорода. Таким образом, концевые прямые линии обозначают метильные группы, а не атомы водорода.
NH2
|
|
|
О |
2-метилбутан |
циклопропан |
анилин |
фуран |
Этот способ широко используется для изображения молекул карбоциклических и гетероциклических соединений.

ВВедение В органическую химию
23
молекулярная формула. Молекулярная (брутто-) формула показывает, какие атомы и в каком количестве входят в состав молекулы. В качестве примера при-
ведены структурная и молекулярная формулы метанола:
CH3OH |
CH4O |
структурная формула |
молекулярная формула |
При составлении молекулярной формулы прежде всего указывают число атомов углерода и водорода, а затем в алфавитном порядке (по латинским названиям элементов) — число остальных элементов, входящих в состав молекулы. Например, для хлоруксусной кислоты СlСН2СООН молекулярная формула имеет вид
C2H3ClO2.
Молекулярные формулы, в отличие от структурных формул, не дают однозначного ответа о строении вещества. Одной и той же молекулярной формуле могут соответствовать два и более соединений. Так, одинаковую молекулярную формулу C2H6O имеют этиловый спирт C2H5—ОH и диметиловый эфир
CH3—O—CH3.
Из приведенных вариантов изображения молекул более широко применяют структурные формулы, которые позволяют с помощью определенной символики показать распределение электронной плотности в молекуле, выделить реакционные центры и описать предлагаемый механизм реакции. Недостаток структурных формул заключается в том, что они не отражают истинного расположения атомов в пространстве. Более полное представление о строении молекул дают стереохимические формулы и молекулярные модели (см. подразд. 5.2.1).

Глава 2
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
2.1. КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Важнейшими классификационными признаками органических соединений являются строение углеродной цепи и природа функциональной группы.
классификация по строению углеродной цепи. В зависимости от структуры углеродного скелета все органические соединения делят на две группы: ацикли-
ческие и циклические. К ациклическим (их еще называют алифатическими) отно-
сят вещества с открытой (незамкнутой) цепью. По строению углеводородного остова молекулы различают предельные (насыщенные) и непредельные (ненасы-
щенные) алифатические соединения. Предельные содержат только простые связи, непредельные — кратные (двойные и тройные) углерод-углеродные связи:
СН |
3—СН3 |
Н2С—СН2 |
СН3—С—СН |
|
предельное алифатическое соединение |
непредельные алифатические соединения |
|
Циклические органические соединения содержат в своей структуре замкнутые цепи атомов — циклы. В зависимости от природы атомов, входящих в цикл, вы-
деляют карбоциклические и гетероциклические соединения.
В молекулах карбоциклических соединений циклы состоят только из атомов углерода:
|
|
|
|
|
H |
||
H2С |
|
СH2 |
HC |
С |
|||
|
CH |
||||||
H2С СH |
|
|
|
|
|||
CH |
|||||||
HC |
|
||||||
|
СH2 СH3 |
|
|
C |
|||
|
|
|
|
|
Н |
||
карбоциклические соединения
Группа карбоциклов объединяет два ряда органических веществ, существенно различающихся по химическим свойствам,— алициклические и ароматические.
К алициклическим соединениям относят ряд карбоциклов, не обладающих ароматическим характером. Алициклические соединения по степени насыщен-
ности делят на предельные и непредельные:
|
|
|
|
|
|
|
|
СH2 |
|
|
|
|
|
|
|
СH2 |
H |
С |
|
СH |
2 |
|
H2C |
CH2 |
HС |
|
СH |
|
HC |
CH2 |
|||
|
|
|
|
|||||||||||||
|
|
|
|
|||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
С |
|
СH |
2 |
H2C |
CH2 |
H |
С СH |
2 |
HC |
CH2 |
|||||
2 |
|
|
СH2 |
|
|
СH2 |
2 |
|
СH2 |
|
|
СH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
||||||
насыщенные алициклические соединения |
ненасыщенные алициклические соединения |
|||||||||||||||
кЛассиФикаЦиЯ и номенкЛаТура органических соединениЙ
25
Для ароматических соединений характерно наличие ароматической системы. Родоначальником ароматических соединений является бензол.
H
HC С
С CH
CH
HC CH
C
Н
бензол
В гетероциклических соединениях циклы, наряду с атомами углерода, содержат атомы других элементов (чаще N, О, S). Гетероциклические соединения могут быть насыщенными, ненасыщенными и ароматическими:
H2С |
|
СH2 |
H2С |
|
СH |
HС |
|
СH |
|
|
|
||||||
H2С СH2 |
H2С СH |
HС СH |
||||||
|
О |
|
О |
|
О |
|||
насыщенный гетероцикл |
ненасыщенный гетероцикл |
ароматический гетероцикл |
||||||
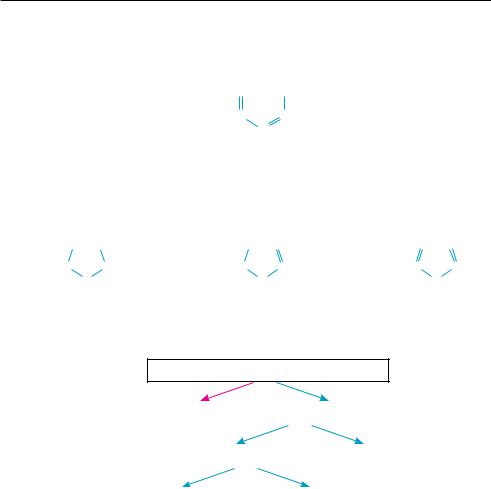
Все вышеизложенное можно представить в виде схемы:
органические соединениЯ
|
аЦикЛические соединениЯ |
|
|
ЦикЛические соединениЯ |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
КАРБОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ |
|
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ |
|||||
|
|
|
|
|
|
|
|
|
|
АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ |
|
|
|
АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ |
|
||||
|
|
|
|
|
|
|
|
|
|
В пределах каждого из названных рядов органические вещества распределяются по классам.
Соединения, молекулы которых состоят только из атомов углерода и водорода,
называют углеводородами.
При замещении в углеводородах одного или нескольких атомов водорода на функциональную группу образуются другие классы органических соединений.
классификация по природе функциональной группы. Функциональная груп па — структурный фрагмент молекулы, определяющий ее химические свойства.
Например, свойства алкенов определяются главным образом присутствием двойной углерод-углеродной связи, карбоновых кислот — карбоксильной группы
—СООН, спиртов — наличием гидроксила —ОН и т. д. По природе функциональной группы органические соединения подразделяют на разнообразные классы, главные из которых приведены в табл. 2.1.
По количеству и однородности функциональных групп органические соеди-
нения делят на монофункциональные, полифункциональные и гетерофункциональные.

26 |
|
|
|
|
|
Глава 2 |
|
|
|
|
|
|
|
||
|
|
|
|
|
Таблица 2.1 |
||
|
|
|
|
|
|
||
|
|
|
классы органических соединений |
|
|||
|
|
|
|
|
|
|
|
|
Название класса |
Общая формула |
|
Функциональная группа |
|||
|
|
|
|
||||
обозначение |
название |
||||||
|
|
|
|
||||
|
|
|
|
|
|
|
|
Галогенопроизводные |
R—Hal |
—Hal |
галоген |
||||
углеводородов |
(—F, —Cl, —Br, —I) |
||||||
|
|
|
|
|
|
||
Спирты, фенолы |
R—OH |
—OH |
гидроксильная |
||||
|
|
|
|
|
|
|
|
Тиоспирты, тиофенолы |
R—SH |
—SH |
сульфгидрильная, |
||||
меркаптогруппа |
|||||||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
Простые эфиры |
R—O—R |
—OR |
R-оксигруппа |
||||
|
|
|
|
|
|
||
Сульфиды (тиоэфиры) |
R—S—R |
—SR |
R-тиогруппа |
||||
|
|
|
|
|
|
||
Альдегиды |
R—CHO |
—C О |
альдегидная |
||||
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
Кетоны |
R |
C=O |
|
C=O |
кетогруппа |
||
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
||
Карбоновые кислоты |
R—COOH |
—C О |
карбоксильная |
||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
||
Нитрилы |
R—CN |
—C—N |
нитрильная, цианогруппа |
||||
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
||
Сульфоновые кислоты |
R—SO3H |
|
|
|
|||
—S—OH |
сульфогруппа |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
||
|
|
|
|
|
|
|
|
|
|
R—NO2 |
|
+ О |
|
||
Нитросоединения |
—N |
нитрогруппа |
|||||
|
|
|
|
|
O– |
|
|
Нитрозосоединения |
R—NO |
—N=O |
нитрозогруппа |
||||
|
|
|
|
|
|
||
Амины |
R—NH2 |
—NH2 |
аминогруппа |
||||
|
|
|
|
|
|
|
|
|
|
|
+ |
+ |
|
||
Диазосоединения |
R—N—NX– |
—N—N |
диазогруппа |
||||
Азосоединения |
R—N=N—R |
—N=N— |
азогруппа |
||||
|
|
|
|
|
|
|
|
Монофункциональные содержат одну функциональную группу, полифункциональные — несколько одинаковых, а гетерофункциональные — несколько различных групп:
СH3—CН2—ОН |
H2N—CH2—CH2—NH2 |
H2N—CH2—CH2—OH |
монофункциональное соединение |
полифункциональное соединение |
гетерофункциональное соединение |
Все классы органических соединений тесно взаимосвязаны. Существует множество путей перехода от одних классов к другим через превращения функциональных групп.

кЛассиФикаЦиЯ и номенкЛаТура органических соединениЙ
27
2.2. НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Номенклатура органических соединений складывалась на протяжении всего периода развития органической химии. В историческом аспекте следует выделить три основные номенклатурные системы: тривиальную, рациональную и междуна-
родную (IUPAC).
Тривиальная номенклатура. Первые названия, которые давали органическим соединениям, были случайными. Тривиальные, или эмпирические, названия соединений отражают природные источники соединений (муравьиная, лимонная кислоты, мочевина, индиго, кофеин), способы получения (пирогаллол, пировиноградная кислота), характерные свойства (пикриновая и капроновая кислоты, флуоресцеин, малахитовый зеленый), имена первооткрывателей (реактив Гриньяра, кетон Михлера). Тривиальные названия органических соединений прочно укоренились, и многие из них до сих пор общепризнанны. Особенно широко их применяют для обозначения сложных соединений и новых соединений неустановленного строения. Эти названия не отражают реального химического строения, их количество значительно и продолжает увеличиваться.
рациональная номенклатура. Это первая номенклатура, в которой стали учитывать в названии вещества его строение. В основе рациональных названий используется принцип деления органических соединений на гомологические ряды.
Гомологическим называют ряд соединений, в котором каждый последующий представитель отличается от предыдущего на группу СН2.
Согласно рациональной номенклатуре все вещества в определенном гомологическом ряду рассматриваются как производные простейшего представителя данного ряда, в частности, у алканов — метана1, у алкенов — этилена и т. д.:
СН4 |
СН3—СН2—СН3 |
H2С—СН2 |
СН3—СН—СН2 |
метан |
диметилметан |
этилен |
метилэтилен |
Однако для названия сложных химических структур рациональная номенклатура оказалась непригодной. В настоящее время применение этой номенклатуры ограничено.
международная номенклатура (IUPAC). Основы международной номенклатуры заложены в 1892 году на международном конгрессе химиков в Женеве (женевская номенклатура). В 1930 году на Х конгрессе химиков в Льеже она была несколько усовершенствована и дополнена (льежская номенклатура) и, наконец, на XIX конгрессе Международного союза теоретической и прикладной химии в 1957 году были разработаны правила современной номенклатуры, известной под названием «номенклатура IUPAC»2.
Номенклатурные правила IUPAC признаны во всех странах мира и позволяют дать однозначное название любому органическому соединению.
В Украине в 1992 году была создана Украинская национальная комиссия по химической терминологии и номенклатуре, основной задачей которой было упорядочение правил IUPAC применительно к украинскому языку. Использование рекомендаций дает возможность избежать тех недоразумений и отклонений от систематической номенклатуры, которые возникают в результате копирования
1 Название «метан» присваивают наиболее замещенному атому углерода.
2 The International Union of Pure and Applied Chemistry — Международный союз теоретической и прикладной химии.

Глава 2
28
русских терминов. Традиционно арены называют бензол, толуол, ксилол, стирол, кумол, нафталин и другие, хотя суффикс -ол по правилам IUPAC указывает на присутствие спиртовой группы, а суффикс -ин — тройной связи.
Рекомендованные названия бензен, толуен, ксилен, стерен, кумен, нафтален соответствуют терминам benzene, toluene, xylene, sterene, cumene, naphthalene.
Предложены названия спиртов: глицерол, пентаеритрол, инозитол, холестерол, пирокатехол, резорцинол, флороглюцинол и др.
Возрождение и становление украинской терминологии дает возможность возвратить удачные термины, возникшие в украинских словарях еще в 20-х годах ХХ века (этер, эстер, этерификация, эстерификация). Следует отметить, что становление украинской номенклатуры требует определенного времени, которое и расставит все акценты.
Номенклатура IUPAC предусматривает несколько вариантов образования названий органических соединений, из которых наиболее широко применяются заместительный и радикало-функциональный.
Иногда с целью максимального упрощения построения названий соединений используют соединительный, заменительный и другие варианты номенклатуры IUPAC.
Заместительная номенклатура. При образовании названий по заместительной номенклатуре органические соединения рассматривают как производные простейших углеводородов, в молекуле которых один или несколько атомов водорода замещены на другие атомы или группы атомов, называемые заместителями.
При составлении названия по заместительному варианту номенклатуры IUPAC прежде всего определяют, какие функциональные группы входят в состав соединения, и выбирают среди них старшую (табл. 2.2).
Таблица 2.2
основные функциональные группы, расположенные в порядке уменьшения старшинства
Название класса |
Общая |
Функциональная |
|
Обозначения |
|||
формула |
группа |
в префиксе |
|
в суффиксе |
|||
|
|
||||||
|
|
|
|
|
|
|
|
|
R O+, |
—O+, —S+, |
|
|
|
||
Катионы |
R3 S+, |
-онио-* |
|
-оний* |
|||
|
R3N+ |
=N+= |
|
|
|
||
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
—C |
О |
карбокси- |
|
-карбоновая кислота |
|
|
R—C О |
|
|
OH |
|
|
|
Карбоновые кислоты |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
OH |
** |
О |
|
|
|
|
|
|
— |
|
-овая кислота |
|||
|
|
—(C) |
OH |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
Сульфоновые кислоты |
R—SO3H |
|
—OH |
|
|
|
|
—S |
сульфо- |
|
-сульфоновая кислота |
||||
|
|
|
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
|
|
|
|
|
* Природу катиона в названии указывают перед окончанием: оксонио-(оксоний), аммонио- (аммоний), сульфонио-(сульфоний).
** Атом углерода, указанный в скобках, входит в состав главной углеродной цепи.

кЛассиФикаЦиЯ и номенкЛаТура органических соединениЙ |
29 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Окончание табл. 2.2 |
||
|
|
|
|
|
|
|
||
Название класса |
Общая |
Функциональная |
Обозначения |
|
||||
формула |
группа |
в префиксе |
в суффиксе |
|
||||
|
|
|||||||
|
|
|
|
|
|
|
||
|
|
О |
—C О |
— |
металл… карбоксилат |
|||
Соли карбоновых |
R—C |
|
OM |
|
|
|
|
|
|
|
|
|
|
|
|
||
кислот |
OM |
—(C) |
О |
|
|
|
|
|
|
|
|
|
|
||||
|
|
— |
металл… оат |
|
||||
|
|
|
OM |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
—C |
О |
R-оксикарбо- |
|
|
|
|
|
|
|
R…карбоксилат |
|
|||
|
|
О |
OR |
нил — |
|
|||
|
R′—C |
|
|
|
|
|||
Сложные эфиры |
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
OR |
—(C) |
О |
— |
R…оат |
|
|||
|
|
|
||||||
|
|
|
OR |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
—C |
О |
галоформил- |
-карбонилгалогенид |
|
|
Галогенангидриды |
R—C |
|
Hal |
|
|
|
|
|
Hal |
—(C) |
О |
— |
-оилгалогенид |
|
|||
|
|
|
||||||
|
|
|
Hal |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О |
—C |
О |
карбамоил- |
-карбоксамид |
|
|
Амиды |
R—C |
|
NH2 |
|
|
|
|
|
NH2 |
—(C) |
О |
— |
-амид |
|
|||
|
|
|
||||||
|
|
|
NH2 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Нитрилы |
R—C—N |
—C—N |
циано- |
-карбонитрил |
|
|||
—(C)—N |
— |
-нитрил |
|
|||||
|
|
|
|
|||||
|
R—C О |
—C |
О |
формил- |
-карбальдегид |
|
||
Альдегиды |
|
H |
|
|
|
|
||
|
О |
|
|
|
|
|||
|
|
H |
—(C) |
оксо- |
-аль |
|
||
|
|
|
H |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
C=O |
|
|
|
|
|
Кетоны |
C=O |
оксо- |
-он |
|
||||
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Спирты |
R—OH |
—OH |
гидрокси- |
-ол |
|
|||
|
|
|
|
|
|
|
||
Фенолы |
Ar—OH |
—OH |
гидрокси- |
-ол |
|
|||
|
|
|
|
|
|
|
||
Тиолы (тиоспирты) |
R—SH |
—SH |
меркапто- |
-тиол |
|
|||
|
|
|
|
|
|
|
||
Гидропероксиды |
R—OOH |
—OOH |
гидроперокси- |
– |
|
|||
|
|
|
|
|
|
|
||
Амины |
R—NH2 |
—NH2 |
амино- |
-амин |
|
|||
|
|
|
|
|
|
|
||
Имины |
R—CH=NH |
=NH |
имино- |
-имин |
|
|||
|
|
|
|
|
|
|
|
|
Глава 2
30
Если в соединении имеется одна такая группа, она считается старшей; если две и более, старшей из них является расположенная в табл. 2.2 выше. В названии органического соединения старшая функциональная группа обозначается в суффиксе, а все остальные — в префиксе. Согласно номенклатурным правилам IUPAC некоторые функциональные группы не рассматривают по старшинству и обозначают в названии всегда в префиксе в алфавитном порядке.
Функциональные группы, обозначаемые только в префиксе: —Br (бром-), —Cl (хлор-), —F (фтор-), —I (йод-), —N2 (диазо), —N3 (азидо-), —NO (нитрозо-),
—NO2 (нитро-), —N ОH (аци-нитро-), —OR (R-окси-), —SR (R-тио-) и др. O
ОH (аци-нитро-), —OR (R-окси-), —SR (R-тио-) и др. O
После определения старшей группы устанавливают так называемую родона-
чальную структуру соединения.
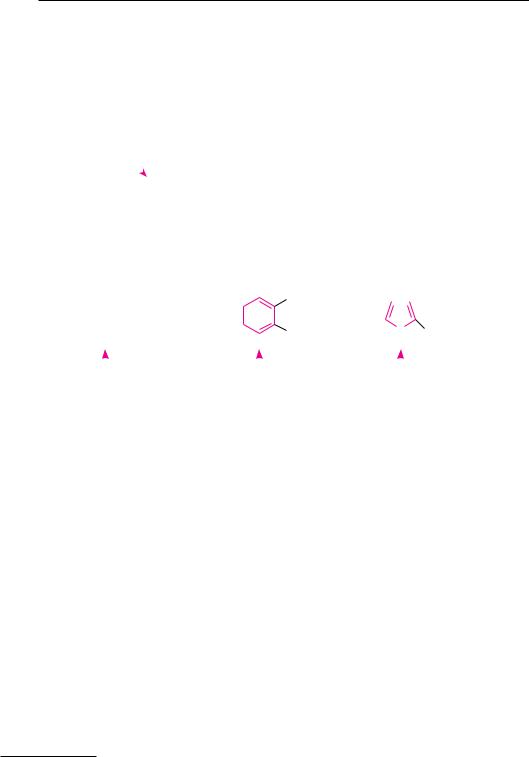
Родоначальной структурой называют структурный фрагмент молекулы, лежащий в основе названия. В ациклических соединениях родоначальной структурой является главная углеродная цепь, в карбоциклических и гетероциклических — цикл:
СН3— |
СН—СН2—OН |
|
|
COOH |
|
|
|
|||
О COOH |
||||||||||
|
|
NH2 |
||||||||
|
||||||||||
|
|
|
|
|
||||||
|
||||||||||
СН3 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Родоначальная структура |
|
|
|
|
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
В качестве главной углеродной цепи выбирают ту, которая содержит максимальное число (в порядке убывающей значимости): а) функциональных групп (см. табл. 2.2); б) кратных (двойных и тройных) связей; в) атомов углерода; г) заместителей.
Заместителем называют любой атом или группу атомов, которые не входят
вродоначальную структуру. Понятие заместитель включает в себя функциональную группу и радикал.
Радикал1 представляет собой остаток молекулы углеводорода, образующийся
врезультате удаления одного или нескольких атомов водорода.
Свободную валентность в радикалах обозначают валентным штрихом. По количеству свободных валентностей различают одно-, двух- и трехвалентные радикалы:
СН3—СН2— |
СН3—СН— —СН2—СН2— |
СН3—С— |
одновалентный радикал |
двухвалентные радикалы |
трехвалентный радикал |
В зависимости от того, у какого атома углерода (первичного, вторичного или третичного) находится свободная валентность, различают первичные, вторичные и третичные радикалы.
Первичным называют атом углерода, непосредственно связанный только с одним атомом углерода, вторичный — с двумя, третичный — соответственно с тремя:
1 Следует отличать от понятия «свободный радикал» (частица с неспаренным электроном), например •СН3.
