
- •Федеральное агентство по образованию
- •СОдержАние
- •I. Теоретическая часть предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •1.4. Структурная организация белков
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2. Контроль активности фермента.
- •2.2. Химическая модификация фермента
- •2.3. Аллостерическая регуляция
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •3.2. Водорастворимые витамины
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •1. Фосфолипиды (до 90%) – глицерофосфолипиды и сфингофосфолипиды: фосфатидилхолин
- •Церамид
- •Галактозилцерамид
- •4.2. Транспорт веществ через мембрану
- •2. Облегченная диффузия
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Генерация свободных радикалов в клетке
- •6.6. Реакции общего пути катаболизма
- •6.6.1. Окислительное декарбоксилирование пвк
- •6.6.2. Цикл трикарбоновых кислот
- •Регуляция общего пути катаболизма
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •Глюкоза → глюкозо-6-фосфат.
- •Пируват → оксалоацетат → фосфоенолпируват
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов.
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •II. Лабораторный практикум Работа 1. Анализ аминокислот и белков
- •1. Качественный анализ аминокислотных смесей методом бумажной хроматографии.
- •2. Цветные реакции на белки.
- •3. Реакции осаждения белков.
- •3. 1. Осаждение белков при нагревании.
- •3.2. Осаждение белков солями тяжелых металлов.
- •3.3. Осаждение белков концентрированными минеральными кислотами.
- •3.5. Осаждение белков органическими кислотами.
- •Контрольные вопросы
- •Работа 2. Сложные белки – фосфопротеины и гликопротеины
- •2. Гликопротеины.
- •1.2. Реакция с дифениламином.
- •2.Хромопротеины.
- •2.1. Бензидиновая проба на геминовую группировку гемоглобина.
- •Контрольные вопросы
- •4. Специфичность действия ферментов амилазы и сахаразы.
- •Контрольные вопросы
- •Работа 5. Определение активности ферментов
- •1. Действие активаторов и ингибиторов на α-амилазу слюны.
- •2. Определение активности α-амилазы слюны по Вольгемуту.
- •Контрольные вопросы
- •Работа 6. Витамины
- •9.1. Взаимодействие витамина с с к3[Fe(cn)6].
- •9.2. Реакция с метиленовой синью.
- •Контрольные вопросы
- •Работа 7. Оксидоредуктазы
- •1. Обнаружение дегидрогеназы (ксантиноксидаза, альдегиддегидрогеназа, кф 1.1.3.22) в молоке (реакция Шардингера).
- •2. Сопоставление редокс-потенциалов рибовлавина и метиленового синего.
- •3. Определение каталазы по а.Н. Баху и а.И. Опарину.
- •Контрольные вопросы
- •Работа 8. Обмен углеводов
- •3.1. Реакция Троммера с гидроксидом меди.
- •3.2. Выявление фруктозурии пробой Селиванова.
- •3.3. Энзиматический метод полуколичественного определения глюкозы в моче с помощью тест-полоски "glucophan".
- •Контрольные вопросы
- •Литература
2. Цветные реакции на белки.
2.1. Реакция Миллона.
Реактив Миллона состоит из нитратов ртути (I) и (II) в HNO3 с примесью HNO2. Реакция реактива Милона с белками обусловлена присутствием в них остатка тирозина.
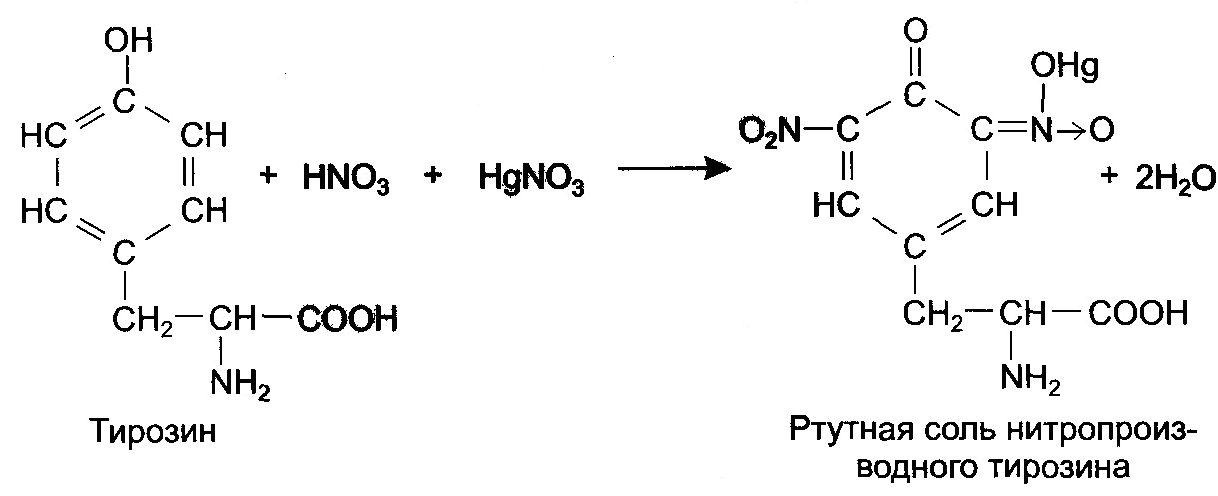
В пробирку наливают 0,5 мл раствора белка и 0,5 мл реактива Миллона. Образуется белый осадок под действием соли ртути и азотной кислоты, входящих в состав реактива Миллона. При нагревании осадок окрашивается сначала в розовый, а затем в коричнево-красный цвет.
2.2. Реакция Адамкевича.
Реакция обусловлена присутствием в белке остатков аминокислоты триптофана.
К 1 мл сыворотки добавляют 0,5 мл ледяной уксусной кислоты (содержит примесь глиоксилевой кислоты) и нагревают до растворения белка. Содержимое пробирки охлаждают и, наклонив пробирку, осторожно по стенке наслаивают 1 мл концентрированной серной кислоты. На границе двух слоев жидкости возникает красно-фиолетовое окрашивание. При нагревании окрашивание появляется быстрее.
2.3. Нингидриновая реакция.
Реакция обусловлена наличием в белке остатков α-аминокислот.

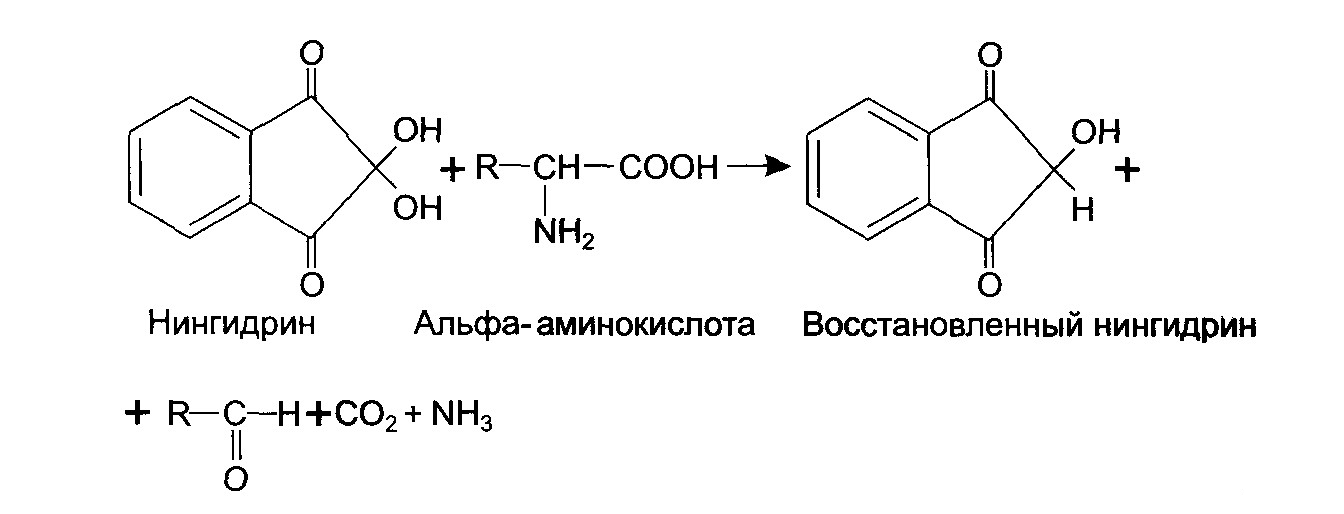
+ RСОН + СО2 + NН3

В пробирку наливают 1 мл раствора белка, добавляют 5 капель 0,2% раствора нингидрина и нагревают. Через несколько минут наблюдают появление сине-фиолетового окрашивания.
2.4. Реакция Шульце – Распайля.
Реакция Шульце - Распайля обусловлена наличием в белке остатков триптофана. Они, взаимодействуя с оксиметилфурфуролом, дают продукты конденсации, окрашенные в вишнево-красный цвет. Оксиметилфурфурол образуется из фруктозы в присутствии концентрированной серной кислоты:
К 0,5 мл сыворотки добавляют 1-2 капли 10% раствора сахарозы и по стенке пробирки наслаивают 1 мл конц. серной кислоты. Слегка встряхивают пробирку. На месте соприкосновения воды и кислоты появляется вишнево-красное окрашивание.
3. Реакции осаждения белков.
3. 1. Осаждение белков при нагревании.
В пробирку наливают 0,5 мл раствора белка и нагревают. Наблюдают появление опалесценции. При кипячении может выпасть осадок.
3.2. Осаждение белков солями тяжелых металлов.
Белки при взаимодействии с солями тяжелых металлов (медь, ртуть, свинец и др.) денатурируют и образуют нерастворимые в воде комплексные соединения вследствие адсорбции тяжелого металла на поверхности белковой молекулы. На этом основано использование белков в качестве противоядия при отравлении тяжелыми металлами.
В две пробирки наливают по 0,5 мл раствора белка. В первую добавляют 2 капли 5% раствора сульфата меди, во вторую – 2 капли 5% раствора ацетата свинца. В обеих пробирках выпадает осадок белка.
3.3. Осаждение белков концентрированными минеральными кислотами.
Выпадение белка в осадок при взаимодействии с концентрированными минеральными кислотами обусловлено дегидратацией белковых молекул, образованием нерастворимых комплексных солей белка и кислот. В избытке серной и соляной кислот осадок белка растворяется. Избыток азотной кислоты не растворяет осажденный белок. Реакция с азотной кислотой используется при клинических исследованиях мочи на присутствие в ней белка (проба Геллера).
В пробирку наливают 1 мл концентрированной азотной кислоты и затем, наклонив пробирку, осторожно приливают по стенке равный объем раствора белка. На границе двух жидкостей появляется белый осадок белка. Встряхивают пробирку и добавляют избыток азотной кислоты. Осадок не исчезает. Повторяют опыт с концентрированными соляной и серной кислотами.
