
- •Федеральное агентство по образованию
- •СОдержАние
- •I. Теоретическая часть предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •1.4. Структурная организация белков
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2. Контроль активности фермента.
- •2.2. Химическая модификация фермента
- •2.3. Аллостерическая регуляция
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •3.2. Водорастворимые витамины
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •1. Фосфолипиды (до 90%) – глицерофосфолипиды и сфингофосфолипиды: фосфатидилхолин
- •Церамид
- •Галактозилцерамид
- •4.2. Транспорт веществ через мембрану
- •2. Облегченная диффузия
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Генерация свободных радикалов в клетке
- •6.6. Реакции общего пути катаболизма
- •6.6.1. Окислительное декарбоксилирование пвк
- •6.6.2. Цикл трикарбоновых кислот
- •Регуляция общего пути катаболизма
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •Глюкоза → глюкозо-6-фосфат.
- •Пируват → оксалоацетат → фосфоенолпируват
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов.
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •II. Лабораторный практикум Работа 1. Анализ аминокислот и белков
- •1. Качественный анализ аминокислотных смесей методом бумажной хроматографии.
- •2. Цветные реакции на белки.
- •3. Реакции осаждения белков.
- •3. 1. Осаждение белков при нагревании.
- •3.2. Осаждение белков солями тяжелых металлов.
- •3.3. Осаждение белков концентрированными минеральными кислотами.
- •3.5. Осаждение белков органическими кислотами.
- •Контрольные вопросы
- •Работа 2. Сложные белки – фосфопротеины и гликопротеины
- •2. Гликопротеины.
- •1.2. Реакция с дифениламином.
- •2.Хромопротеины.
- •2.1. Бензидиновая проба на геминовую группировку гемоглобина.
- •Контрольные вопросы
- •4. Специфичность действия ферментов амилазы и сахаразы.
- •Контрольные вопросы
- •Работа 5. Определение активности ферментов
- •1. Действие активаторов и ингибиторов на α-амилазу слюны.
- •2. Определение активности α-амилазы слюны по Вольгемуту.
- •Контрольные вопросы
- •Работа 6. Витамины
- •9.1. Взаимодействие витамина с с к3[Fe(cn)6].
- •9.2. Реакция с метиленовой синью.
- •Контрольные вопросы
- •Работа 7. Оксидоредуктазы
- •1. Обнаружение дегидрогеназы (ксантиноксидаза, альдегиддегидрогеназа, кф 1.1.3.22) в молоке (реакция Шардингера).
- •2. Сопоставление редокс-потенциалов рибовлавина и метиленового синего.
- •3. Определение каталазы по а.Н. Баху и а.И. Опарину.
- •Контрольные вопросы
- •Работа 8. Обмен углеводов
- •3.1. Реакция Троммера с гидроксидом меди.
- •3.2. Выявление фруктозурии пробой Селиванова.
- •3.3. Энзиматический метод полуколичественного определения глюкозы в моче с помощью тест-полоски "glucophan".
- •Контрольные вопросы
- •Литература
Контрольные вопросы
1. Какие реакции катализируют ферменты класса оксидоредуктаз?
2. Рассмотрите роль дегидрогеназ в процессах биологического окисления.
3. Для опыта 3 составьте схему переноса водорода (электронов и ионов водорода) с учетом стандартных окислительно-восстановительных потенциалов использованных компонентов.
Работа 8. Обмен углеводов
Опыт 1. Количественное определение активности амилазы в сыворотке крови.
Моча и сыворотка крови здоровых людей обладают низкой амилазной активностью по сравнению с амилазой слюны. Определение активности амилазы в моче и сыворотке крови используется в клинической практике при диагностике заболеваний поджелудочной железы. При остром панкреатите активность фермента в крови и в моче увеличивается в 10-30 раз, при хроническом панкреатите, раке поджелудочной железы, приступе желчнокаменной болезни – в 3-5 раз. При нарушении функции почек, а также при некоторых заболеваниях крови повышенная активность фермента в крови не сопровождается увеличением его активности в моче.
Фермент амилаза катализирует гидролиз α-1,4-гликозидной связи крахмала и гликогена. Метод основан на колориметрическом определении концентрации крахмала до и после ферментативного гидролиза по окрашиванию в реакции с реактивом Люголя. Работу проводят согласно таблице 2:
Таблица 2. Определение активности амилазы.
|
Реактивы |
Количество реактива, мл | |
|
опыт |
контроль | |
|
Раствор крахмала |
1,0 |
1,0 |
|
Сыворотка крови |
0,02 |
|
|
|
Инкубировать при 370 5 минут | |
|
Реактив Люголя |
1,0 |
1,0 |
|
Дистиллированная вода |
8,0 |
8,0 |
|
Сыворотка крови |
|
0,02 |
Оба раствора фотометрируют на фотоэлектроколориметре при 630 нм (толщина кюветы 10 мм) относительно воды. Расчет активности амилазы проводят по формуле:
((Dк – Dоп)/Dк)200,
где Dк – оптическая плотность контрольной пробы, Dоп – опытной пробы.
Опыт 2. Количественное определение пировиноградной кислоты в моче.
Пировиноградная кислота (ПВК) является одним из промежуточных продуктов обмена углеводов. В анаэробных условиях (при гипоксии) она восстанавливается в молочную кислоту, а в аэробных – подвергается окислительному декарбоксилированию и превращается в ацетил-КоА. ПВК – один из основных источников глюконеогенеза. Вследствие большой скорости реакции превращения пировиноградная кислота присутствует в тканях и биологических жидкостях в небольшом количестве. В крови ее содержание составляет 0,5-1 мг/100 мл пирувата. Содержание пирувата в моче в норме составляет 2 мг/100 мл, суточное выведение его с мочой - 10-25 мг.
Наиболее резкое увеличение концентрации пирувата (ПВК) в крови и, как следствие, в моче, отмечается при мышечной работе и В1- витаминной недостаточности. Это явление отмечается также при заболеваниях печени, сахарном диабете, сердечной декомпенсации, токсикозе и др.
Принцип метода: пируват с 2,4-динитрофенилгидразином образует окрашенное соединение - 2,4-динитрофенилгидразонпируват. Его экстрагируют из реакционной смеси толуолом. При добавлении спиртового раствора щелочи развивается красно-оранжевое окрашивание, интенсивность которого прямо пропорциональна количеству ПВК.
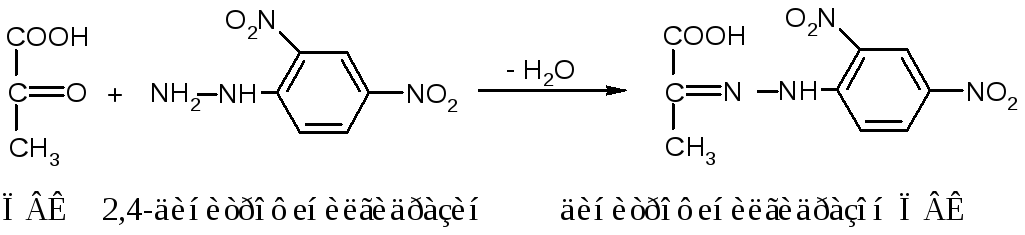
Ход работы: к 1,0 мл мочи прилить 0,5 мл 0,1% 2,4-динитрофенилгидразина, перемешать и через 5 минут добавить 2,5 мл насыщенного водой толуола. После встряхивания в течение 1 мин оставить раствор до расслоения воды и толуола. Из верхнего толуолового слоя отобрать пробу объемом 1 мл сухой градуированной пипеткой и перенести в сухую пробирку, добавить 3 мл спиртового раствора КОН. Пробу с 1 мл стандартного раствора пирувата обрабатывают так же, как опытную. В контроле на реактивы моча замещается 1 мл воды. Через 10 мин пробы фотометрировать против контроля на реактивы при длине волны 400-415 нм на фотоэлектроколориметре.
Расчет проводится по формуле: Х=(Dо*50мг)/Dс, где: Dо – оптическая плотность опытного раствора, Dс – оптическая плотность стандартного раствора, 50 мг - концентрация стандарта пировиноградной кислоты, Х - концентрация пирувата в моче.
Опыт 3. Экспресс-диагностика патологий углеводного обмена.
