- •Федеральное агентство по образованию
- •СОдержАние
- •I. Теоретическая часть предмет биохимии
- •1. Химия белков
- •1.1. Методы выделения и очистки белков
- •1.2. Функции белков
- •1.3. Аминокислотный состав белков
- •1.4. Структурная организация белков
- •1.5. Физико-химические свойства белков
- •1.6. Классификация белков
- •1.6.1. Простые белки
- •1. Альбумины и глобулины.
- •2. Протамины и гистоны.
- •3. Проламины и глютелины.
- •1.6.2. Сложные белки
- •Структура нуклеиновых кислот
- •Контрольные вопросы
- •2. Ферменты
- •2.1. Химическая природа ферментов
- •2.2. Механизм действия ферментов
- •2.3. Кинетика ферментативных реакций
- •2.4. Свойства ферментов
- •2.5. Регуляция активности ферментов
- •1. Контроль количества фермента.
- •2. Контроль активности фермента.
- •2.2. Химическая модификация фермента
- •2.3. Аллостерическая регуляция
- •2.6. Классификация и номенклатура ферментов
- •2.7. Ферменты в медицине
- •2. Приобретенные энзимопатии.
- •Контрольные вопросы
- •3. Витамины
- •3.1. Жирорастворимые витамины
- •3.2. Водорастворимые витамины
- •Контрольные вопросы
- •4. Основные принципы организации биомембран
- •4.1. Строение и функции мембран
- •1. Фосфолипиды (до 90%) – глицерофосфолипиды и сфингофосфолипиды: фосфатидилхолин
- •Церамид
- •Галактозилцерамид
- •4.2. Транспорт веществ через мембрану
- •2. Облегченная диффузия
- •Контрольные вопросы
- •5. Механизмы передачи гормонального сигнала
- •Трансмембранная передача гормонального сигнала
- •Контрольные вопросы
- •6. Введение в метаболизм
- •6.1. Общая схема катаболизма
- •6.2. Биоэнергетика
- •6.3. Организация и функционирование дыхательной цепи
- •6.4. Разобщение окисления и фосфорилирования
- •6.5. Генерация свободных радикалов в клетке
- •6.6. Реакции общего пути катаболизма
- •6.6.1. Окислительное декарбоксилирование пвк
- •6.6.2. Цикл трикарбоновых кислот
- •Регуляция общего пути катаболизма
- •Контрольные вопросы
- •7. Обмен углеводов
- •7.1. Переваривание углеводов
- •7.2. Обмен гликогена
- •7.3. Гликолиз
- •7.4. Включение фруктозы и галактозы в гликолиз
- •7.5. Челночные механизмы
- •7.6. Цикл кори
- •7.7. Спиртовое брожение
- •7.8. Пентозофосфатный путь превращения глюкозы
- •7.9. Глюконеогенез
- •7.10. Регуляция обмена углеводов
- •Глюкоза → глюкозо-6-фосфат.
- •Пируват → оксалоацетат → фосфоенолпируват
- •7.11. Нарушения углеводного обмена Нарушение гидролиза и всасывания углеводов.
- •Гликогенозы
- •Нарушения промежуточного обмена углеводов
- •Гипер- и гипогликемия
- •Глюкозурия
- •Контрольные вопросы
- •II. Лабораторный практикум Работа 1. Анализ аминокислот и белков
- •1. Качественный анализ аминокислотных смесей методом бумажной хроматографии.
- •2. Цветные реакции на белки.
- •3. Реакции осаждения белков.
- •3. 1. Осаждение белков при нагревании.
- •3.2. Осаждение белков солями тяжелых металлов.
- •3.3. Осаждение белков концентрированными минеральными кислотами.
- •3.5. Осаждение белков органическими кислотами.
- •Контрольные вопросы
- •Работа 2. Сложные белки – фосфопротеины и гликопротеины
- •2. Гликопротеины.
- •1.2. Реакция с дифениламином.
- •2.Хромопротеины.
- •2.1. Бензидиновая проба на геминовую группировку гемоглобина.
- •Контрольные вопросы
- •4. Специфичность действия ферментов амилазы и сахаразы.
- •Контрольные вопросы
- •Работа 5. Определение активности ферментов
- •1. Действие активаторов и ингибиторов на α-амилазу слюны.
- •2. Определение активности α-амилазы слюны по Вольгемуту.
- •Контрольные вопросы
- •Работа 6. Витамины
- •9.1. Взаимодействие витамина с с к3[Fe(cn)6].
- •9.2. Реакция с метиленовой синью.
- •Контрольные вопросы
- •Работа 7. Оксидоредуктазы
- •1. Обнаружение дегидрогеназы (ксантиноксидаза, альдегиддегидрогеназа, кф 1.1.3.22) в молоке (реакция Шардингера).
- •2. Сопоставление редокс-потенциалов рибовлавина и метиленового синего.
- •3. Определение каталазы по а.Н. Баху и а.И. Опарину.
- •Контрольные вопросы
- •Работа 8. Обмен углеводов
- •3.1. Реакция Троммера с гидроксидом меди.
- •3.2. Выявление фруктозурии пробой Селиванова.
- •3.3. Энзиматический метод полуколичественного определения глюкозы в моче с помощью тест-полоски "glucophan".
- •Контрольные вопросы
- •Литература
Структура нуклеиновых кислот
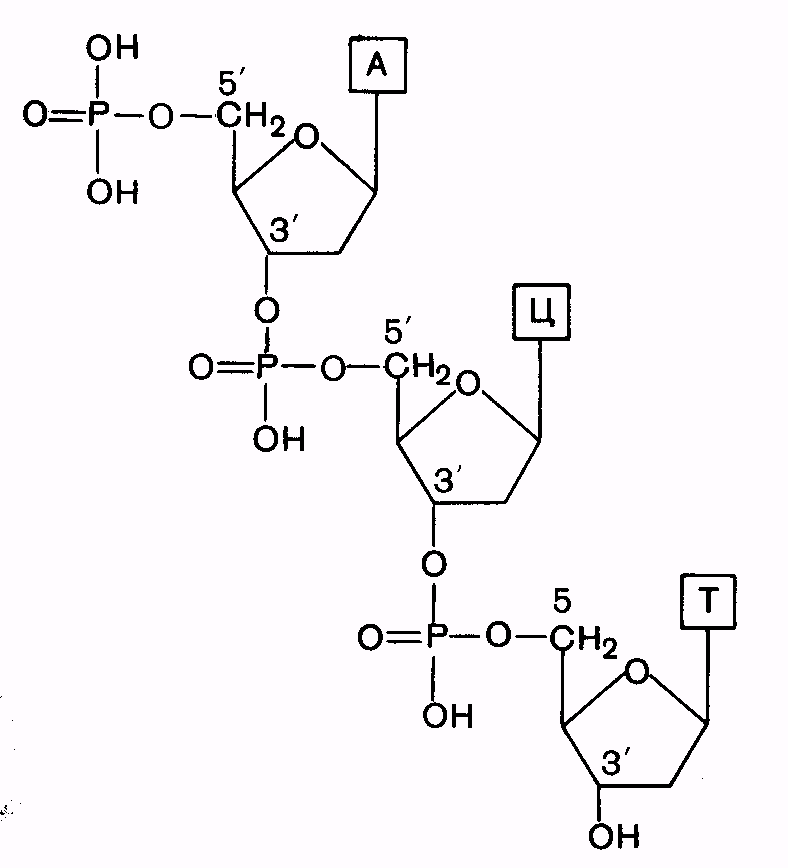
Первичная структура - последовательность расположения мононуклеотидов в полинуклеотидной цепи ДНК и РНК. Мономеры в молекулах нуклеиновых кислот соединены сложноэфирной связью, образованной фосфатным остатком одного мононуклеотида и 3’-гидроксильной группой пентозного остатка другого мононуклеотида (3’,5’-фосфодиэфирная связь).
Для изучения химического состава НК используют секвенирование – расщепление НК на фрагменты ферментами либо химическими реагентами и анализ продуктов при помощи электрофореза, хроматографии и др.
|
|
Рис. 8. Схема первичной структуры ДНК. |
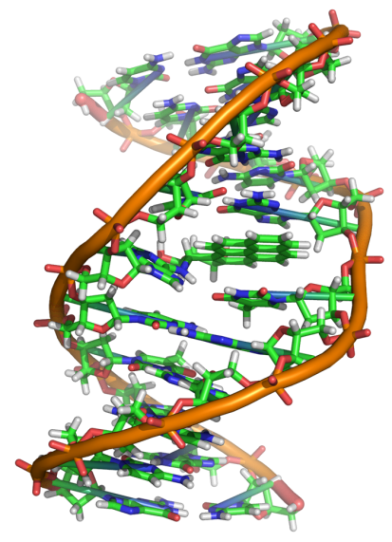
Вторичная структура. ДНК состоит из двух цепей, образующих правовращающую спираль, в которой обе полинуклеотидные цепи закручены вокруг одной и той же оси. Азотистые основания находятся внутри, а углеводные компоненты – снаружи (рис. 9).
В молекуле ДНК основания уложены парами: пуриновые из одной цепи и пиримидиновые из другой. Взаимодействие пар А-Т и Г-Ц называют комплементарностью, а соответствующие азотистые основания – комплементарными (рис. 10). Цепи ДНК комплементарны друг другу. Стабильность А-Т пар обеспечивается двумя водородными связями, а пар Г-Ц-тремя.
Между азотистыми основаниями, собранными в стопку вдоль молекулы ДНК, возникают силы гидрофобных взаимодействий (стэкинг-взаимодействия) – вносят большой вклад в стабилизацию двойной спирали.
Обе цепи в молекуле ДНК имеют противоположную полярность: межнуклеотидная связь в одной цепи имеет направление 5’3’, в другой – 3’5’.
|
|
|
|
Рис. 9. Вторичная структура ДНК. |
|
|
| |
|
Рис. 10. Комплементарность цепей в ДНК. | |
Конфигурация двойной спирали ДНК меняется от количественного содержания воды и ионной силы раствора. Существует более 10 форм ДНК.
Молекулы РНК построены из одной полинуклеотидной цепи. В этой цепи есть комплементарные участки, которые образуют двойные спирали. При этом соединяются водородными связями пары А-У и Г-Ц. Спирализованные участки РНК (шпильки) содержат 20-30 нуклеотидных пар и чередуются с неспирализованными участками.
Для тРНК Р. Холли предложил модель клеверного листа. Особенность такой структуры – спирализация полинуклеотидной цепи самой на себя в строго фиксированных зонах. Особенности структуры тРНК имеют прямое отношение к процессу трансляции, поэтому более подробно они рассмотрены в разделе биосинтеза белка.
Менее охарактеризована вторичная структура матричных и рибосомных РНК. Вторичная структура рРНК и мРНК характеризуется спирализацией самой на себя.
Во вторичной структуре ДНК и РНК есть нуклеотидные последовательности, называемые палиндромами (перевернутые повторы). Эти повторы служат основой для образования структуры шпилек или для формирования на отдельных участках тройных спиралей.
Третичная структура нуклеиновых кислот: двойная спираль ДНК на некоторых участках может подвергаться дальнейшей спирализации с образованием суперспирали или открытой кольцевой формы. Нативные молекулы тРНК имеют третичную структуру, которая отличается от «листа клевера» компактностью за счет складывания различных частей молекулы.
Нуклеиновые кислоты входят в состав нуклеопротеинов. Нуклеопротеины (НП) выполняют функции, связанные с хранением и реализацией генетической информации.
Существует 2 типа НП - дезоксирибонуклеопротеины (ДНП, содержат ДНК) и рибонуклеопротеины (РНП, содержат РНК). ДНП преимущественно находятся в ядре, а РНП - в цитоплазме. В состав НП входят гистоновые и негистоновые белки. Типичные представители НП - рибосомы (комплексы рибосомных РНК с белками), ДНП-хроматин (комплекс ДНК с гистонами и негистоновыми белками).
Гистоны - сильно щелочные белки с невысокой молекулярной массой. Содержат большое количество лизина и аргинина. 5 классов гистонов различаются по размерам, аминокислотному составу и величине заряда. Они принимают участие в структурной организации хроматина, нейтрализуя за счет положительных зарядов аминокислотных остатков отрицательно заряженные фосфатные группы ДНК.
Природа негистоновых белков пока выяснена недостаточно.
Для многих белков хроматина характерны особенности структуры, обеспечивающие их связывание с ДНК: лейциновая застежка-«молния»; мотив α-спираль – поворот – α-спираль, «цинковый палец».