
- •4. Комплексные соединения
- •4.1. Общие сведения о комплексных соединениях
- •4.2 Образование и разрушение комплексных соединений. Диссоциация комплексных соединений
- •Задачи и упражнения
- •4.2. Образование и разрушение комплексных соединений.
- •5. Окислительно-восстановительные реакции
- •6. Эквивалент, закон эквивалентов
- •6. Эквивалент. Закон эквивалентов
- •Приложение
- •Продолжение табл. 1
- •Продолжение табл. 1
- •Окончание табл. 1
- •Окончание табл. 2
- •Рекомендуемая литература
- •Оглавление
- •Учебное издание
4. Комплексные соединения
4.1. Общие сведения о комплексных соединениях
Соединения, образованные из двух или более простых соединений, каждое из которых может существовать независимо, называют комплексными соединениями. Иногда, чтобы подчеркнуть особенность образования химической связи в этих соединениях, их определяют как соединения высшего порядка, образованные из более простых, устойчивых соединений без возникновения новых электронных пар.
 Центральный
ион (атом) в комплексном соединении
называетсякомплексообразователем.
Это обычно ион d-
или f-элемента,
реже – р- или s-элемента.
Непосредственно окружающие
комплексообразователь ионы или молекулы,
называемые лигандами,
образуют вместе с комплексообразователем
так называемую внутреннюю
(координационную) сферу
комплексного
соединения. Ее обычно выделяют квадратными
скобками. Ионы (молекулы) за пределами
внутренней сферы образуют внешнюю
сферу
комплексного соединения. Например, в
соединении
Центральный
ион (атом) в комплексном соединении
называетсякомплексообразователем.
Это обычно ион d-
или f-элемента,
реже – р- или s-элемента.
Непосредственно окружающие
комплексообразователь ионы или молекулы,
называемые лигандами,
образуют вместе с комплексообразователем
так называемую внутреннюю
(координационную) сферу
комплексного
соединения. Ее обычно выделяют квадратными
скобками. Ионы (молекулы) за пределами
внутренней сферы образуют внешнюю
сферу
комплексного соединения. Например, в
соединении
Общее число лигандов во внутренней сфере называется координационным числом (к.ч.). Простейшее объяснение механизма образования химической связи в комплексных соединениях – донорно-акцепторное взаимодействие между лигандами и комплексообразователем: лиганды поставляют свободные электронные пары на пустые d-ор6итали комплексообразователя (подробнее – во второй части этого пособия). Лиганд в общем случае может занимать во внутренней сфере не одно, а два (или более) координационных мест в соответствии с числом свободных электронных пар, поставляемых лигандом на свободные орбитали комплексообразователя. Число таких координационных мест, занимаемых лигандом, называется дентатностью. Соответственно различают: монодентатные лиганды – F─, Cl─, CN─, ОН─, NH3, H2O и т.д.; бидентатные лиганды – С2О42─, этилендиамин и т.п. Возможны лиганды и большей дентатности, так, в аналитической химии широко применяется этилендиаминтетрауксусная кислота и ее динатриевая соль (ЭДТА), эти лиганды имеют дентатность, равную шести. Координационные числа обычно четные, наиболее распространены к.ч. 6 и 4. Как правило, координационное число равно удвоенной степени окисления иона-комплексообразователя, то есть комплексным соединениям Ме2+ наиболее характерно к.ч.=4, а для комплексов Ме3+ к.ч.=6. Однако следует иметь в виду, что координационные числа часто бывают и больше, чем удвоенная степень окисления иона-комплексообразователя, и, гораздо реже, меньше. Так, в водных растворах большинство ионов двухвалентных металлов представляют собой гексаакваионы [Me(H2O)6]2+.
По характеру лигандов можно выделить следующие основные типы комплексных соединений. В аквакомплексах лигандом является молекула воды, например, кристаллогидраты. В гидроксокомплексах лиганд – ОН─,
например: K2[Sn(OH)4], Na3[Cr(OH)6]. Аммиачные комплексы (лиганд – NH3), например: [Ag(NH3)2]Cl, [Cu(NH3)4](OH)2. Наиболее обширную группу составляют ацидокомплексы, в которых лигандами выступают анионы кислотных остатков, например: K[Au(CN)2], K2[HgI4].
Все приведенные выше комплексные соединения являются однородными, то есть содержат единственный лиганд; возможны и комплексные соединения с различными лигандами, например: [Cr(H2O)5Cl]Cl2.
Могут быть комплексные соединения и без внешней сферы, то есть внутрисферные комплексные соединения, например: [Pt(NH3)2Cl2].
Названия комплексных соединений строятся по принципу названий солей с указанием лигандов и степени окисления комплексообразователя. При построении названия комплексного катиона или аниона первоначально называют ионные лиганды в порядке возрастания степени их сложности. Далее называют лиганды-молекулы также в порядке возрастания степени их сложности. При этом молекулы H2O и NH3 обозначаются "аква" и "аммин". При необходимости используются соответствующие соединительные гласные. В конце названия комплексного катиона или аниона называется ион-комплексообразователь с указанием его степени окисления римскими цифрами в скобках. В случае аниона берется корень латинского названия элемента, к нему прибавляется окончание "ат", например: станнат, аурат, плюмбат. Примеры:
[Cr(NH3)4Cl2]Cl хлорид дихлоротетрамминхрома (III);
K3[Al(OH)6] гексагидроксоалюминат (III) калия;
[Co(NH3)6][Cr(CN)6] гексацианохромат (III) гексаамминкобальта (III);
[Pt(NH3)2Cl2] дихлородиамминплатина (II).
Для комплексных соединений характерно явление изомерии, рассмотрим кратко основные его типы. Ионизационная изомерия обусловлена различным распределением ионов между внутренней и внешней сферами комплексного соединения, например:
[Cr(NH3)4Cl2]Br и [Cr(NH3)4ClBr]Cl .
В случае если катион и анион являются комплексными, возможна координационная изомерия, она связана с различным распределением лигандов между комплексообразователями, например:
[Cr(NH3)6][Co(CN)6] и [Co(NH3)6][Cr(CN)6] .
Если молекулы или ионы, являющиеся лигандами, могут существовать в различных изомерных формах, возможна изомерия лигандов. Такой вид изомерии чаще характерен для комплексных соединений с органическими лигандами, например:
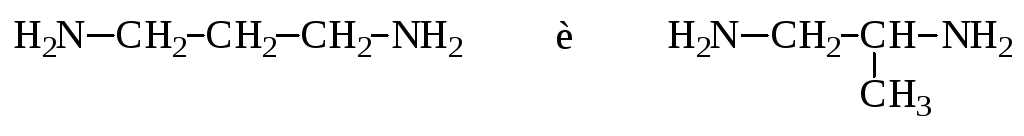
Различное пространственное расположение лигандов ведет к цис-транс-изомерии и зеркальной изомерии. Так для комплексов с к.ч.=4, име-ющих квадратное строение, существуют цис- и транс-изомеры, например:
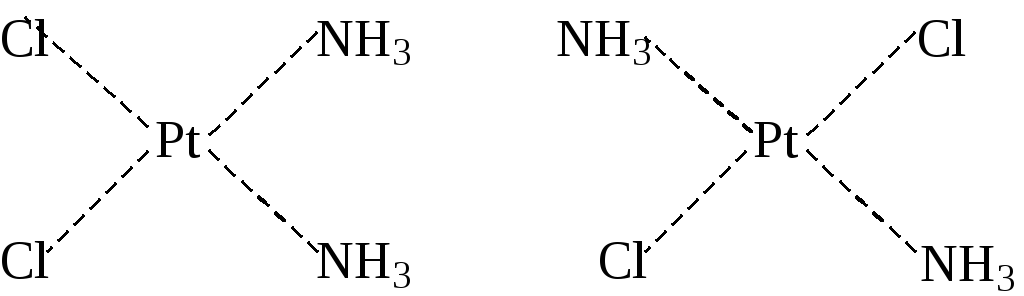
цис-изомер транс-изомер
Зеркальные изомеры комплексных соединений имеют идентичные химические и физические свойства, они различаются лишь асимметрией кристаллов и разным направлением вращения плоскости поляризации света.
