
Основные классы неорганических соединений степень окисления и составление химических формул
Состав химических соединений выражают химическими формулами, при составлении которых используется характеристика состояния элемента в соединении – степень окисления (с. о.).
-
Степень окисления – условный заряд атома в химическом соединении.
Степень окисления при необходимости указывают над символом элемента в формуле или римской цифрой в названии вещества.
Для расчета степеней окисления элементов используют следующие правила:
степень окисления элемента в простом веществе равна нулю
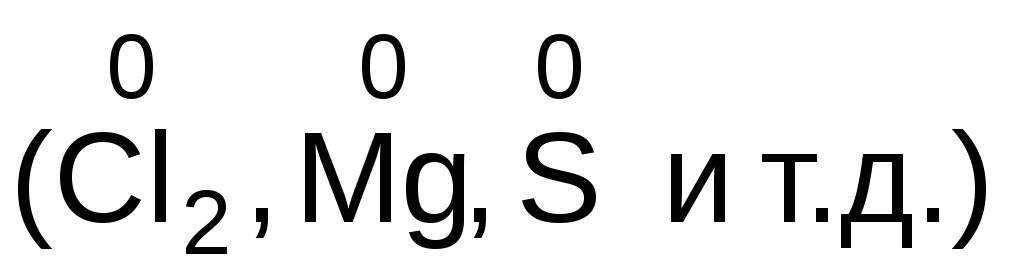 ;
;степень окисления кислорода в большинстве сложных веществ равна -2
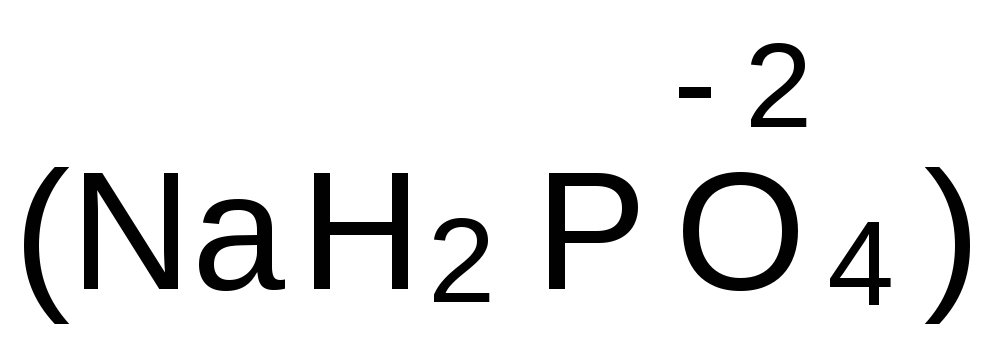 ;
;степень окисления водорода и щелочных металлов в большинстве сложных веществ равна +1
 ;
;алгебраическая сумма степеней окисления всех атомов в молекуле равна нулю, в ионе – его заряду.
Пример. Рассчитайте степени окисления элементов в соединениях: а) NH3; б) P2O5; в) NH4NO3.
Решение
а) С. о. водорода равна +1. С. о. азота рассчитываем, приравнивая алгебраическую сумму с. о. атомов, образующих данную молекулу, нулю. Сумма с.о. атома азота (x) и трех атомов водорода 3(+1)
x
+ 3(+1) = 0, откуда x
= 3.
![]() .
.
б) С.о. кислорода равна 2. Аналогично предыдущему составляем выражение алгебраической суммы с.о. двух атомов фосфора (2х) и пяти атомов кислорода:
2х
+ 5(-2) = 0, откуда х = +5.
![]() .
.
в) Большинство элементов в соединениях проявляют несколько различных степеней окисления. Рассчитать степени окисления атомов азота в соединении NH4NO3 можно, разделив эту соль на ионы NH4+ и NO3. Далее для каждого иона составляем выражение суммы степеней окисления, включая неизвестную степень окисления атома азота х, и приравниваем его заряду иона.
Для иона NH4+:
х + 4 (+1) = +1, х = 3;
для иона NO3:
х + 3(2) = 1, х = +5.
Формула
нитрата аммония с указанием с. о.
азота:
![]() .
.
Классы неорганических соединений
Химические вещества могут быть простыми и сложными. Среди простых веществ выделяют металлы и неметаллы (см. далее). Граница между металлами и неметаллами размыта, выделенные элементы проявляют двойственность свойств.
|
(H) |
Металлы Неметаллы |
H |
He | ||||||||||||||
|
Li |
Be |
|
B |
C |
N |
O |
F |
Ne | |||||||||
|
Na |
Mg |
|
Al |
Si |
P |
S |
Cl |
Ar | |||||||||
|
K |
Ca |
Sc |
Ti |
V |
Cr |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Ga |
Ge |
As |
Se |
Br |
Kr |
|
Rb |
Sr |
Y |
Zr |
Nb |
Mo |
Tc |
Ru |
Rh |
Pd |
Ag |
Cd |
In |
Sn |
Sb |
Te |
I |
Xe |
|
Cs |
Ba |
La* |
Hf |
Ta |
W |
Re |
Os |
Ir |
Pt |
Au |
Hg |
Tl |
Pb |
Bi |
Po |
At |
Rn |
|
Fr |
Ra |
Ac** |
Ku |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
La* – первый элемент семейства лантаноидов (14 лантаноидов),
Ас** – первый элемент семейства актиноидов (14 актиноидов).
Сложные неорганические соединения делят на три основных класса – оксиды, гидроксиды и соли.
Оксиды
-
Оксиды – соединения элементов с кислородом.
Если элементы проявляют переменную с.о., то образуют оксиды различного состава, что учитывают в названии оксида указанием с.о. элемента. Если элемент образует один оксид, то в названии оксида с.о. не указывают.
Например, Al2O3 – оксид алюминия (алюминий проявляет единственную с. о., равную +3); N2O3 – оксид азота (III) (азот проявляет различные с. о., в данном оксиде с. о. азота равна +3).
-
Оксиды делят на несолеобразующие и солеобразующие.
Несолеобразующие оксиды весьма немногочисленны – например CO, NO, N2O.
-
Солеобразующие оксиды по химическим свойствам делят на три группы – основные, кислотные и амфотерные.
Основные оксиды образуют только типичные металлы в степени окисления +1, +2 (не всегда), +3 (редко).
Кислотные
оксиды
образуют
неметаллы, а также металлы в высоких
степенях окисления (+6, +7). Оксиды неметаллов
‑ SO2,
P2O5,
оксиды металлов –
![]() ,
,
![]() .
.
Амфотерные оксиды образуют металлы в степени окисления +3, +4, +5, иногда +2, а также элементы, расположенные вблизи условной диагонали, разделяющей металлы и неметаллы (As ‑ As2O3, Sb ‑ Sb2O3). Амфотерные оксиды некоторых металлов в степени окисления +2 –ZnO, PbO, SnO, BeO – полезно запомнить. Амфотерные оксиды сочетают свойства основных и кислотных оксидов.
