
- •Колебательная спектроскопия
- •Спектральные области и методики
- •Определение и особенности ИКС
- ••Инфракрасная спектроскопия является универсальным методом определения важных функциональных групп, а также структурных фрагментов
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- ••Поглощение инфракрасного излучения веществом вызывает переходы между колебательными уровнями основного электронного состояния. При
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- ••Колебательная спектральная линия из-за наложения вращательных переходов превращается в полосу, состоящую из множества
- ••Менее вероятным переходам на более высокие колебательные подуровни
- •Рис 1. Потенциальные кривые, уровни энергии и схематические спектры гармонического (1) и ангармонического
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Схема энергетических уровней в молекуле, иллюстрирующая поглощение излучения
- •Правила отбора для ИК-спектроскопии
- ••Все колебания в молекуле можно разделить на два типа: валентные и деформационные. Если
- ••Молекулы, имеющие центр симметрии, лишены дипольного момента и не приобретают его в процессе
- ••Если при колебаниях молекулы изменяется угол между связями без изменения длины связей, то
- •Рис 3. Валентные и деформационные колебания метиленовой группы
- •Колебания и спектры многоатомных молекул
- •Колебания и спектры многоатомных молекул
- •Каждая полоса в ИК-спектре характеризуется следующими параметрами:
- •Рис 5. Схема ИК-спектрометра (UR-10, UR-20, ИКС-29 и др.)
- •Современный ИК-спектрометр
- •Источники излучения ИК-спектров
- •Подготовка образцов для снятия ИК-спектров
- •Пробы для ИК-спектров
- •Держатель таблеток
- •Пресс и матрица для приготовления
- •Кювета жидкостная разборная
- •Монохроматоры (монохроматизаторы)
- •Детекторы для ИК-спектров
- •Пример ИК-спектра органического вещества
- •Рис 7. Частоты колебаний связей между атомами
- •Условия идентификации веществ и расшифровки структуры
- •Условия идентификации веществ и расшифровки структуры
- •Рис 8. ИК-спектр н-гексана СН3(СН2)4СН3
- •Рис 10. ИК-спектр гексанола-2 СН3(CH2)3СН(ОН)СН3
- •Рис 11. ИК-спектр гексанона-2 СН3(CH2)3С(О)СН3
- •Рис 12. ИК-спектр толуола С6H5СН3
- •Преимущества метода ИК-спектроскопии
- ••Комбинационное рассеяние света
- ••Рассеяние, происходящее на флуктуациях плотности, называется молекулярным или рэлеевским, оно происходит без изменения
- •Спектроскопия комбинационного рассеяния
- •Основы метода
- ••Спектр рассеянного света содержит, кроме спектральных линий, характеризующих падающий на среду свет, дополнительные
- •Квантовая теория
- •Исследуемое вещество облучается световой волной с частотой, на которой данное вещество не поглощает,
- •При взаимодействии электромагнитного излучения с веществом происходит поляризация молекулы, ее деформация в поле
- •Из поляризованного состояния молекула возвращается не на первоначальный, а на какой-то другой энергетический
- •Обычно эти дополнительные комбинационные линии соответствуют изменениям во вращательном и колебательном движении атомов
- •В отличие от люминесценции, которая также представляет собой вторичное излучение с измененной частотой,
- •Спектры комбинационного рассеяния являются одним из случаев молекулярных спектров, в которых проявляется строение
- •Пример спектра КР
- •Основные блоки установки для снятия спектров КР
- •Схема установки со спектрометром ИСП-15
- •Современный КР-спектрометр (RMP-300)
- •Преимущества КР спектроскопии
- •Преимущества КР спектроскопии
•Менее вероятным переходам на более высокие колебательные подуровни
отвечают спектральные линии, называемые обертонами. Их частота в 2, 3 и т.д. раз больше, чем частота основной линии, а интенсивность гораздо меньше. Основную линию обозначают , а обертоны 2 , 3 и т.д.
11
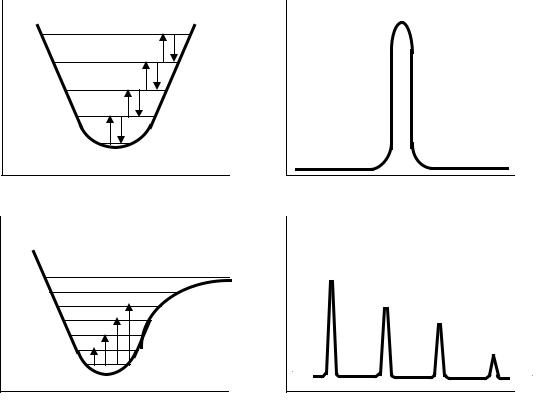
Рис 1. Потенциальные кривые, уровни энергии и схематические спектры гармонического (1) и ангармонического (2) осцилляторов
Е |
1 |
|
|
|
|
|
|
= 4 |
|
||
|
= 3 |
|
|
= 2 |
|
|
= 1 |
|
|
= 0 |
|
|
r |
|
Е |
2 |
|
|
|
|
|
|
|
|
= 3 |
|
|
V = 2 |
|
|
= 1 |
|
|
= 0 |
|
|
r |
|
= 1
|
/, см -1 |
|
|
= |
|
|
|
1 |
= |
= |
|
|
|
||
|
2 |
3 |
= |
|
|
||
|
|
|
4 |
|
/, см -1 |
|
|
12
Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Обычно при комнатной температуре большинство молекул находится в нижнем колебательном состоянии, поскольку энергия теплового возбуждения значительно меньше, чем энергия перехода из основного состояния в возбужденное.
•Поэтому экспериментально легче всего наблюдать поглощение, соответствующее переходу из основного колебательного состояния ( = 0) в первое возбужденное ( = 1).
•Для гармонического осциллятора возможны и другие переходы с изменением квантового числа на единицу, т.е. переходы между
соседними уровнями: = 1
13
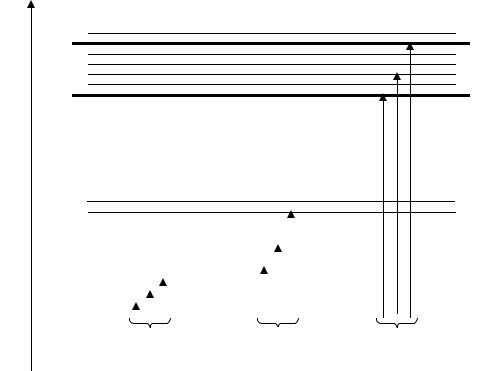
Схема энергетических уровней в молекуле, иллюстрирующая поглощение излучения
Е |
|
1 |
|
/ |
|
0 |
S1 |
/ |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Вращательные |
Колебательные |
|
|
|
|
||||||||||
|
|
|
|
Электронные |
||||||||||||
|
|
|
|
переходы |
переходы |
переходы |
||||||||||
14
Правила отбора для ИК-спектроскопии
•Необходимое условие колебательного перехода – изменение дипольного момента молекулы при колебаниях атомов.
•Способность вещества поглощать энергию ИК–излучения зависит от суммарного изменения дипольного момента молекулы при вращении и колебании, т.е. поглощать ИК–излучение может лишь молекула, обладающая электрическим дипольным моментом, величина или направление которого изменяется в процессе колебания и вращения. Дипольный момент означает несовпадение центров тяжести положительных и отрицательных зарядов в молекуле, т. е. электрическую асимметрию молекулы.
•Таким образом, не все молекулы способны поглощать инфракрасное излучение. Молекулы, имеющие центр симметрии, лишены дипольного момента и не приобретают его в процессе колебания и, следовательно, в инфракрасном спектре не активны. Примеры таких молекул – двухатомные молекулы с ковалентной связью (H2, N2, галогены, молекула СО2 с симметрично-валентными колебаниями атомов и т.д.).
15
•Все колебания в молекуле можно разделить на два типа: валентные и деформационные. Если при рассматриваемом колебании происходит главным образом изменение длин связей, а углы между
связями меняются мало, то такое колебание называется валентным и обозначается . Валентные колебания могут быть симметричными ( s) и асимметричными ( as).
•Необходимое условие колебательного перехода – изменение дипольного момента молекулы при колебаниях атомов. Симметричная молекула, не обладающая дипольным моментом, не может
поглотить ИК-излучение. Дипольный момент означает несовпадение центров тяжести положительных и отрицательных зарядов в молекуле, т. е. электрическую16 асимметрию молекулы.
•Молекулы, имеющие центр симметрии, лишены дипольного момента и не приобретают его в процессе колебания и, следовательно, в инфракрасном спектре не активны.
•Примеры таких молекул – двухатомные молекулы с ковалентной связью (H2, N2,
галогены, молекула СО2 с симметрично- валентными колебаниями атомов и т.д.).
17
•Если при колебаниях молекулы изменяется угол между связями без изменения длины связей, то такие
колебания называются
деформационными.
•Обозначают такие колебания – или . Они также могут быть симметричными ( s, s) и асимметричными ( аs, аs).
•Деформационные колебания подразделяют на веерные, крутильные,
ножничные и маятниковые. Такие же |
|
категории приемлемы и для описания |
|
колебаний отдельных групп.. |
18 |

Рис 3. Валентные и деформационные колебания метиленовой группы
19
Колебания и спектры многоатомных молекул
•Полный колебательный спектр многоатомной молекулы содержит целый набор линий и полос, частоты и интенсивности которых отражают все особенности ее сложного колебательно- вращательного движения.
•Колебания отдельных атомов в молекуле связаны друг с другом, и поэтому сложную молекулу можно представить как совокупность целого набора осцилляторов.
•Энергия, приходящаяся на один из осцилляторов (на отдельную связь в молекуле), перераспределяется по другим связям и все атомы вовлекаются в колебание.
•Сложные колебания можно разложить на ограниченное число простых, так называемых нормальных колебаний.
20
