
Gestageny_u_zhenshin_raznogo_vozrasta
.pdf
|
Иммунные аспекты эффективности прогестагенов |
достаточно) |
Цитокины |
(рецепторов |
Th2-типа |
|
|
|
Цитокины |
|
Th1-типа |
ДИДРОГЕСТЕРОН раз активнее эндогенного прогестерона) |
Цитокины |
Th2-типа |
|
|
|
(в 5 |
|
|
9 / StatusPraesens |
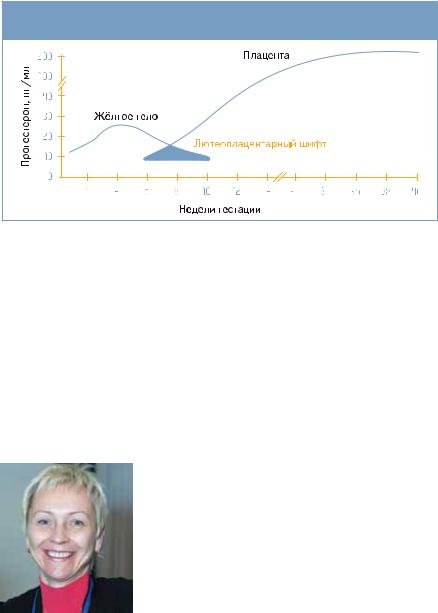
Передача прогестеронсинтезирующей функции от жёлтого тела плаценте |
Докладчик процитировал результаты изучения плодового кровотока, впервые обнародованные совсем недавно на 15-м Всемирном конгрессе по гинекологической эндокринологии (7–10 марта 2012 года, Флоренция). В рандомизированном контролируемом исследовании было сопоставлено влияние дидрогестерона и микронизированного прогестерона на субэндометриальный кровоток при идиопатическом самопроизвольном привычном невынашивании. По нескольким допплерометрическим параметрам (индекс резистентности, пульсационный индекс, максимальная систолическая активность и др.), рассчитанным на 6–7-й неделях беременности, влияние дидрогестерона оказалось достоверно эффективнее, нежели в группе прогестерона. Частота сохранения беременности составила 40% в группе дидрогестерона и 28% в группе микронизированного прогестерона35.
Иммунологические аспекты привычной потери плода
Свой доклад проф. Алина Викторовна Соловьёва (Москва)
начала с актуальных данных статистики. У 2,9% родившихся детей имеются уродства, обусловленные хромосомными аномалиями, эта же причина наиболее часто приводит к потере беременности в ранние сроки (50– 80% всех самопроизвольных абортов в I триместре)36. К сожалению, принятая в наши дни практика предусматривает выскабливание стенок матки во всех случаях госпитализации женщины с выкидышем без исследования причин произошедшего. А ведь во многих стационарах врачи вполне владеют ультразвуковой диагностикой настолько, чтобы уже при поступлении пациентки быстро
и точно выяснить, совершился ли выкидыш полностью. И при задержке плодного яйца в полости матки на фоне аборта в ходу показаны антигестагены и мизопростол, а вовсе не кюретаж. Конечно, оправдан и следующий шаг: каждую пациентку
StatusPraesens / 10

с повторным выкидышем должен кон- |
[ Cпецифическая предгравидарная |
сультировать генетик; если в анамнезе |
подготовка женщинам |
семейной пары есть две потери плода |
с антифосфолипидным синдромом |
или более, показано преконцепционное |
|
исследование кариотипа супругов. |
требуется крайне редко, |
Для выявления непосредственных |
поскольку нарушения, приводя- |
причин гибели плода необходимо про- |
щие к невынашиванию, запускают- |
вести диагностический поиск по выяв- |
|
лению ауто- и аллоиммунных нарушений |
ся лишь с началом беременности. ] |
у матери. Среди аутоиммунных факто- |
|
ров наиболее значимо наличие антифос- |
|
фолипидныхантител(АФА)—до40% |
••протромбину; |
случаев привычного невынашивания37 |
••аннексину; |
(27–42% по данным А.П. Миловано- |
••фосфатидилэтаноламину; |
ва и соавт., 200538). Другие «виновни- |
••фосфатидилинозитолу40; |
ки»: антинуклеарные, антитиреоид- |
••факторам щитовидной железы (что |
ные и антиэндотелиальные антитела, |
влияет на кровообращение в пла- |
а также аномальная активность на- |
центе и на выживаемость плода) |
туральных киллеров, изменение соот- |
к тиреоглобулину и тиреоперокси- |
ношения Th1- и Th2-цитокинов, анти- |
дазе41. |
отцовские цитотоксические антитела, |
Плацента — иммунный барьер для |
антиидиотипические антитела, ано- |
возможных реакций материнского им- |
мальная экспрессия HLA-G (антиген |
мунитета во время беременности. Тем |
гистосовместимости, человеческий лей- |
не менее трофобласт экспрессирует на |
коцитарный антиген G)37. |
поверхности антигены основного ком- |
Фосфолипидные молекулы — ос- |
плекса гистосовместимости. Во время |
новной компонент всех без исключения |
беременности иммунная система ма- |
клеточных мембран. В норме анионные |
тери распознаёт отцовские антигены |
фосфолипиды расположены во внутрен- |
лейкоцитов и запускает формирование |
ней части липидного бислоя плазмати- |
не только антиотцовских цитотоксиче- |
ческой мембраны, но при ремоделирова- |
ских (APCA) и антиидиотипических |
нии трофобласта во время беременности |
антител (Ab2), но и антител, блоки- |
они могут оказываться на внешней по- |
рующих смешанные реакции лимфоци- |
верхности, где в ассоциации с особыми |
тов (MLR-Bf). Последние укутывают |
гликопротеинами (β2-гликопротеины-I) |
трофобласт и защищают его от цито- |
ошибочно трактуются иммунной систе- |
токсического материнского иммунного |
мой как антигены. Это запускает синтез |
ответа. Дефицит антител MLR-Bf во |
антифосфолипидных антител. Класси- |
время беременности может привести |
ческим проявлением антифосфолипид- |
к потере плода42. |
ного синдрома становятся не только |
Существует методика иммуномоду- |
тромбозы и тромбоцитопении, но и по- |
ляции матери переливанием отцовских |
вторные потери плода39. |
лимфоцитов до зачатия42,43. Результа- |
Антифосфолипидные антитела мо- |
ты рандомизированных исследований |
гут вырабатываться к следующим ве- |
демонстрируют благополучное завер- |
ществам: |
шение беременности у 67% лечив- |
••кардиолипину (АКЛА); |
шихся таким образом женщин с по- |
••β2-гликопротеину-I; |
вторными потерями плода в анамнезе |
|
11 / StatusPraesens |

в сравнении с 36% женщинами контрольной группы44.
Тем не менее в связи с недостаточностью данных для постановки корректного морфологического диагноза при выкидыше диагноз антифосфолипидного синдрома слишком часто оказывается «крайним» — на его счёт записывают все неясные случаи, в том числе связанные с обычной недообследованностью женщины. В 2006 году были приняты
обновлённые (сиднейские) Международ-
ные критерии диагностики антифосфолипидного синдрома. Этот диагноз можно выставлять на основании чётких клинических и лабораторных признаков. В лабораторные критерии включено выявление антител к кардиолипину (классов IgG и IgM), волчаночного антикоагулянта, антител к β2-гликопротеину-I.
Рассматривая терапевтическую тактику, докладчик акцентировала внимание на том, что при антифосфолипидном синдроме целесообразно назначать
низкомолекулярные гепарины45, что обусловлено их структурным сходством с β2-гликопротеином-I. Применение гепаринов в очень низких дозах позво-
StatusPraesens / 12
ляет патологическим антителам соединиться с «фальшивыми антигенами» гепарина — это даёт женщине шанс выносить беременность46,47,48.
Результаты клинических исследований подтверждают целесообразность использования низкомолекулярного гепарина — антитромботический эффект не требует непрерывного мониторинга гемостазиограммы, и кроме того, препараты данной группы не проникают через плацентарный барьер49. Низкомолекуляные гепарины нарушают связывание антифосфолипидных антител с клетками эндотелия и поддерживают нормальную инвазию трофобласта50.
Для снижения риска спонтанных абортов при антифосфолипидном синдроме применяют также микродозы ацетилсалициловой кислоты, оказывающие иммуномодулирующий эффект (стимуляция выработки ИЛ-3)47,51,52.
Для успешного лечения ряда заболеваний (синдром гемолиза, повышение активности печёночных ферментов, низкое количество тромбоцитов [HELLP], тромботическая тромбоцитопеническая пурпура, криоглобу-

линемия), в том числе антифосфолипидного синдрома при беременности, можно применять плазмаферез, физически удаляющий антитела и их конечные продукты. Однако этот метод дорог, неудобен и может привести к ряду негативных последствий, таких как нарушения гемостаза и иммунного реагирования. Последующее лечение требует введения иммуноглобулинов, которые останавливают повторную выработку антител53, либо ультрафиолетового облучения крови54.
Так исторически сложилось, что для лечения беременных с антифосфолипидными антителами применяют глюкокортикоиды (преднизолон), хотя эту практику следует признать порочной — подобные назначения неблагоприятно сказываются на состоянии матери (усугубляют артериальную гипертензию, гестационный диабет) и плода (повышают риск преждевременных родов). Глюкокортикоиды обладают свойством проникать через плацентарный барьер, угнетают эндокринную систему плода, что увеличивает частоту преждевременных родов плодами с макросомией и инсулинорезистентностью.
Прогестагены наиболее часто применяют для предупреждения повторных выкидышей и преждевременных родов, а также в лютеиновой фазе программы ЭКО. Дидрогестерон, например, способствует восстановлению иммунной толерантности, стимулирует выработку лимфоцитами прогестерон-индуцированного блокирующего фактора (ПИБФ)55, который в свою очередь:
••влияет на баланс цитокинов, в результате чего продукция цитокинов Th1 снижается, а цитокинов Th2 — повышается;
••иммобилизует натуральные клетки-киллеры и обеспечивает нормальный исход беременности56*.
Такое благоприятное действие повышает вероятность вынашивания беременности.
Подтверждены высокое сродство дидрогестерона («Дюфастона») к прогестероновым рецепторам, а также достоверная эффективность препарата при длительном приёме для обеспечения физиологической имплантации и своевременного родоразрешения57,58. При этом дидрогестерон не проникает через плацентарный барьер, в связи с чем не оказывает какого-либо неблагоприятного влияния на плод, не обладает анаболическими эффектами, способствует сохранению положительного влияния эстрогенов на липидный профиль крови, не изменяет углеводный обмен и артериальное давление. В контексте повышения среднего возраста беременных, что характерно для наших дней, особенно ценным оказывается отсутствие влияния дидрогестерона на гемостаз57. Для женщин (особенно старшего репродуктивного возраста) очень важно, что дидрогестерон не повышает риска тромботических осложнений.
В завершение доклада проф. А.В. Соловьёва отметила, что специфическая предгравидарная подготовка женщинам с антифосфолипидным синдромом требуется крайне редко, поскольку нарушения, приводящие к невынашиванию, запускаются лишь с началом беременности. По показаниям применяют низкомолекулярные гепарины и микродозы ацетилсалициловой кислоты. Также за 3 мес до предполагаемой беременности показаны эффективные и безопасные иммуномодуляторы — прогестины (дидрогестерон). И если беременность наступила на фоне данной терапии, следует продолжить приём препарата как минимум до 12 нед.
* См. статью «Привычное невынашивание и хронический эндометрит», журнал StatusPraesens #2[5], с. 30.
13 / StatusPraesens

ПЕРЕСМОТРЕННЫЕ В 2006 ГОДУ (АВСТРАЛИЙСКИЕ, СИДНЕЙСКИЕ) КРИТЕРИИ АНТИФОСФОЛИПИДНОГО СИНДРОМА
Для обеспечения высокой чувствительности и специфичности антифосфолипидный синдром диагностируют, если у больного подтверждаются один клинический и один лабораторный критерии заболевания.
Клинические критерии
1.Сосудистыйтромбоз.Одинилинесколькоэпизодовартериального,венозного тромбоза или тромбоза мелких сосудов в любой ткани или органе. Тромбоз должен быть подтверждён КТ/МРТ, допплеровским исследованием или морфологически. При морфологическом исследовании тромбоз не должен сочетаться
своспалительными изменениями стенки сосуда.
2.Невынашивание беременности:
a — одна или более смертей плода в срок 10 нед и более, подтверждённых нормальной морфологией плода при ультразвуковом исследовании или морфологически, либо
b — одни или более преждевременных родов морфологически нормального новорождённого после 34 нед гестации в результате тяжёлой преэклампсии, эклампсии или плацентарной недостаточности, либо
c — три или более необъяснимых спонтанных абортов до 10 нед при исключении анатомических, гормональных и генетических причин невынашивания.
Лабораторные критерии
1.Волчаночный антикоагулянт. Положительный результат лабораторного теста на волчаночный коагулянт дважды или большее число раз с промежутком между исследованиями не менее 12 нед (комплекс скринингового обследования, подтверждающего и корректирующего коагулологических тестов
всоответствии с требованиями Международного общества изучения тромбозов и гемостаза).
2.Антикардиолипиновые антитела. Обнаружение антикардиолипиновых антител классов IgG и/или IgM в сыворотке или плазме в среднем или высоком титре (>40 GPL или MPL, или более 99-го перцентиля здоровой популяции), повторно обнаруженных через не менее чем 12 нед, выявленных с помощью стандартизованной тест-системы ИФА.
3.Антитела к β2-гликопротеину. Лабораторное обнаружение этих антител классов IgG и/или IgM в сыворотке или плазме крови в титре более 99-го перцентиля здоровой популяции, выявленных с помощью стандартизованной тестсистемы ИФА.
StatusPraesens / 14

Примечания экспертов
1.Необходимо избегать диагноза «антифосфолипидный синдром», если положительные лабораторные результаты и клинические проявления разделяют менее 12 нед или более 5 лет.
2.Присутствующие врождённые или приобретённые факторы риска тромбоза не являются поводом для исключения антифосфолипидного синдрома
убольного. Однако рекомендуется выделять отдельные группы пациентов в зависимости от отсутствия или наличия дополнительных факторов риска тромбоза. Такими факторами риска могут быть возраст (старше 55 у мужчин, старше 65 у женщин), наличие любых установленных факторов риска сердечно-сосу- дистых заболеваний (гипертензии, диабета, повышенного холестерина ЛНП или низкого холестерина ЛВП, курения, наследственности, указывающей на раннее начало сердечно-сосудистых заболеваний в семье), индекс массы тела более 30 кг/м2, микроальбуминурия, снижение скорости клубочковой фильтрации, врождённые тромбофилии, приём пероральных контрацептивов, нефритический синдром, опухоль, иммобилизация и хирургические операции в недавнем прошлом.
3.Эпизод тромбоза в прошлом может рассматриваться как положительный критерий, если он был объективно подтверждён клинически.
4.Тромбоз поверхностных вен не включён в клинические критерии.
5.Общепринятые признаки плацентарной недостаточности включают:
•отсутствие признаков жизнедеятельности плода;
•прогностически неблагоприятные формы кривой допплерограммы сосудов, указывающей на признаки гипоксемии плода;
•олигогидрамнион с индексом амниотической жидкости менее 5 см;
•постнатальный вес плода менее 10-го перцентиля срока гестации.
6.Эксперты рекомендуют разделять больных антифосфолипидным синдромом на следующие категории:
1 — присутствует более одного лабораторного критерия в любой комбинации; 2а — изолированный волчаночный антикоагулянт;
2b — только антитела к кардиолипину;
2c — только антитела к β2-гликопротеину.
15 / StatusPraesens

Парадоксы привычного невынашивания беременности
Проф. Виктор Евсеевич Радзинский (Москва) завладел вниманием аудитории, как всегда, с первых же слов. По данным официальной статистики, в структуре материнской смертности аборты (как артифициальные, так и спонтанные) занимают лишь 8,1% (Минздравсоцразвития, 2009). Однако в этой схеме не отражено, что прерывание беременности напрямую взаимосвязано с такими отдельно выделенными причинами, как эмболия, осложнения анестезии, инфекционные осложнения и экстрагенитальные заболевания. Если суммировать их все — получится значительное число женщин, гибнущих так или иначе по причине абортов.
Именно погибшие в срок до 22 нед гестации составляют значительную часть материнской смертности — до 35%, в том числе за счёт внематочной беременности и абортов. Конечно, значение самопроизвольных абортов в этой структуре также велико.
Что же касается собственно невынашивания, то важно помнить о разнице в причинах спонтанных и привычных выкидышей: спонтанные случаи чаще всего обусловлены генетическими аномалиями у плода или дефектами имплантации, а привычное невынашивание обычно связано с хроническим эндометритом и дефицитом прогестерона. Понятно, что эти различные клинические ситуации требуют дифференциальной диагностики и разного лечения. К сожалению, предгравидарная подготовка, зачастую чрезмерно усердная, почему-то находится в приоритете,
тогда как реабилитацию после неразвивающейся беременности, позднего выкидыша, внематочной беременности получают лишь 4% женщин. При этом недостаточность плацентарного ложа, наблюдаемая у 64% пациенток с привычным невынашиванием, вполне поддаётся профилактике — но её попросту не проводят.
В течение 6 лет на нескольких российских клинических базах проходило масштабное исследование. Пациенток (n=2500) со спонтанной угрозой прерывания беременности вели консервативно: полупостельный режим, регуляция стула и физиотерапия — эндоназальный электрофорез, электросон (цит.: «...потрясающая методика, даже если не включать аппарат в розетку!»). Из исследования были исключены 15% женщин, начавших принимать прогестины амбулаторно. О чудо: удалось сохранить 93% беременностей, что превышает даже общемировой результат — 86%! Объяснение очень простое: российские врачи злоупотребляют диагнозом «угроза невынашивания». Привычка госпитализировать по поводу малейшей боли в животе всегда удивляет наших зарубежных коллег. Именно гипердиагностика угрозы невынашивания позволила получить столь «выдающиеся» результаты. Можно понять и врачей женских консультаций, ведь они «отвечают за всё», в том числе за плохой исход болезней, не имеющих эффективного лечения (например, истинной угрозы
[ Гистологическое исследование соскобов из полости матки после хирургического аборта у каждой четвёртой женщины выявляет хронический эндометрит. ]
StatusPraesens / 16
невынашивания). Поэтому так высока частота госпитализаций «на всякий случай».
Проф. В.Е. Радзинский упомянул и другие парадоксы, типичные для современной российской медицины, — среди них полипрагмазия, в том числе бесплатное предоставление беременным лекарственных средств с недоказанной эффективностью и безопасностью. Минздравсоцразвития предписывает созывать консилиум с участием клинического фармаколога в тех случаях, когда планируется назначение более пяти лекарственных препаратов одному пациенту59!
К сожалению, врачи слишком часто игнорируют этот приказ, и если, по данным 2010 года, в Кемеровской области беременная получала в среднем 13 препаратов (с разбросом от одного до 30*), то Москва недалеко ушла от этих показателей — в среднем 12 препаратов, большинство которых назначают без достаточных на то оснований. Конечно, во многом здесь виноваты госгарантии, согласно которым беременным предоставляют бесплатные фармацевтические средства, однако ещё один парадокс: ни одно из них не имеет доказательной базы!
Нельзя забывать о катастрофическом доминировании хирургического аборта как единственного бесплатного метода регулирования рождаемости в системе ОМС, а также о практике опорожнения матки по медицинским показаниям хирургическим, а не медикаментозным методом. Ведь основная причина невынашивания — хронический эндометрит, а он напрямую связан с хирургическим вмешательством. Гистологическое исследование соскобов из полости матки после хирургического аборта у каждой четвёртой женщины
выявляет хронический эндометрит60,61. Однако в этом контексте докладчик озвучил и хорошую новость: инструкция по медикаментозному прерыванию беременности теперь допускает применение одной таблетки мифепристона; таким образом, стоимость вмешательства снизилась почти втрое, процедура стала более доступной для российских женщин, делающих выбор в пользу безопасности, а не бесплатности. Более того, медикаментозный аборт стал дешевле хирургического. Значит, ЛПУ должны стремиться к удешевлению процедуры и минимизации последствий аборта.
[ Реабилитацию после неразвивающейся беременности, позднего выкидыша и внематочной беременности получают лишь 4% женщин. ]
В целом создаётся впечатление, что научному врачебному сообществу не интересно исследовать беременность на ранних сроках: из 91 акушерской диссертации, защищённой в 2009– 2010 годах, ранним срокам посвящено только восемь!
Докладчик подчеркнул, что цивилизованным подходом в настоящее время считается отказ от лечения спорадического спонтанного выкидыша в I триместре, поскольку доказательная база по эффективности средств лекарственной и немедикаментозной терапии отсутствует. Часто попытки сохранить беременность обречены на неудачу, так как статистические данные указывают на чрезвычайно высокую частоту так называемого «генетического сбро-
* См. статью «Современные особенности фармакотерапии беременных в России», журнал StatusPraesens, #2[5], с. 22.
17 / StatusPraesens

са» — самопроизвольного прерывания беременности на ранних сроках в силу выраженных хромосомных аномалий эмбриона:
••82% самопроизвольных абортов в срок до 8 нед;
••72% — до 12 нед.
При угрозе невынашивания беременности, к сожалению, очень часто используют методики и средства, эффективность которых не доказана:
••лимфоцитотерапию;
••постельный режим;
••препараты магния с витамином В6 («Магне B6» вообще не имеет показаний при беременности);
••папаверин в свечах;
••дротаверин.
А применение отдельных препаратов
даже вполне определённо небезопасно:
••β-адреномиметиков до 16 нед или постоянно;
••глюкокортикоидов без абсолютных показаний.
Парадоксально, что нередко во врачебных показаниях значатся глюкокортикоиды — уже после наступления беременности, с целью купирования гиперандрогении. Это назначение не только не служит пользе, но даже вредит течению беременности, поскольку медикаментозное угнетение ДГЭА и 17-ОНП одновременно блокирует и рецепторы к прогестерону. Согласно консенсусу, достигнутому на конференции в Барселоне (2007), глюкокортикоиды следует назначать только беременным с подтверждённым эндокринологом диагнозом адреногени-
тального синдрома для предотвращения вирилизации плода установленного женского пола.
Рост числа дисбиотических и инфекционных заболеваний половых путей на ранних сроках беременности, безусловно, повышает риск невынашивания и преждевременных родов. Наиболее важными предпосылками докладчик назвал следующие:
••устойчивую тенденцию роста числа инфекций, передаваемых половым путём (с 1996 года «эпидемиологическое распространение»);
••аборт как метод регулирования рождаемости;
••рост хронических экстрагенитальных заболеваний, снижающих иммунорезистентность организма;
••рост гинекологических заболеваний воспалительной этиологии;
••нерациональноеиспользованиепротивомикробных препаратов;
••необоснованное лечение несуществующих заболеваний, в том числе отсутствующих в МКБ-10 гарднереллёза, микоплазмоза, уреаплазмоза (неправильная трактовка результатов лабораторных исследований, например качественной, а не количественной ПЦР);
••самолечение различными безрецептурными препаратами с антимикробным действием.
Конечно, качественную ПЦР нельзя исключить из диагностического арсенала: она надёжно обнаруживает безусловные патогены — трепонемы, гонококки, хламидии и трихомонады.
[ Эндогенный прогестерон подавляет опосредованную через Т-лимфоциты реакцию отторжения плода, и поэтому применение прогестагенов для сохранения беременности оправдано в первую очередь для блокировки интерлейкинового каскада, продуктивного воспаления, провоцирующего выкидыш. ]
StatusPraesens / 18
