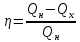- •8. Теорема Штейнера.
- •12. Кинетическая энергия. Работа силы как приращение кинетической энергии частицы, системы.
- •16. Закон сохранения полной механической энергии. Закон сохранения энергии.
- •17. Постулаты специальной теории относительности (сто). Преобразования Лоренца. Принцип относительности Галилея. Преобразования Галилея.
- •Преобразования Лоренца
- •18. Кинетическая энергия релятивистской частицы.
- •19. Идеальный газ. Уравнение состояния идеального газа.
- •20. Давление газа. Основное уравнение молекулярно – кинетической теории (мкт).
- •Вывод основного уравнения мкт[править | править исходный текст]
- •21. Внутренняя энергия, работа идеального газа. Закон Больцмана о равном распределении энергии молекул по степеням свободы. Внутренняя энергия идеального газа
- •22. Первое начало термодинамики и его применение к различным процессам. Первое начало термодинамики и его применение к различным процессам.
- •Теплоёмкость. Уравнение Майера.
- •23. Обратимые и необратимые процессы. Понятие Энтропии.
- •24. Второе и третье начало термодинамики.
22. Первое начало термодинамики и его применение к различным процессам. Первое начало термодинамики и его применение к различным процессам.
Первое начало термодинамики – это количество теплоты переданное макросистеме, идёт на приращение её внутренней энергии и на совершение работы.
Теплоёмкость. Уравнение Майера.
Теплоёмкость тела – это количество теплоты, необходимое для повышения температуры тела на один кельвин:

Удельная теплоёмкость – это количество теплоты, необходимое для повышения на 1 К 1 Кг вещества:

Молярная теплоёмкость – это количество теплоты, необходимое для повышения на 1К 1 моля вещества:

Для идеального газа:


Адиабатный процесс – это процесс, в котором отсутствует теплообмен между системой и окружающей средой (быстропротекающие процессы, например, распространение звука в воздухе).



23. Обратимые и необратимые процессы. Понятие Энтропии.
Обратимый термодинамический процесс – это процесс, допускающий возможное возвращение системы в первоначальное состояние без того, чтобы в окружающей среде остались какие – либо изменения. Равновесные процессы – обратимые, так как системы проходит ту же последовательность равновесных состояний.
Необратимый процесс – это процесс, не допускающий возможности возвращения системы в первоначальное состояние без того, чтобы в окружающей среде остались какие – либо изменения. Все реальные процессы неравновесные и необратимые (диффузия, трение, теплообмен).
Энтропия (S) – это функция состояния, дифференциал которого в элементарном обратимом процессе равен отношению бесконечно малого количества теплоты, сообщённого системе в температуре системы.

Свойства энтропии:
функция состояния;
величина аддитивная (энтропия макросистемы равна сумме энтропий её частей);
для замкнутой системы.


Возрастание энтропии при необратимом процессе соответствует переходу системы в состояние с большей вероятностью, которая соответствует большему статистическому весу.
Статистический
вес ( )
– это число микросостояний, характеризующих
макро состояния (микросостояния – это
состояния молекул). Большей вероятности
и большему статистическому весу
соответствует больший хаос (беспорядок)
в системе.
)
– это число микросостояний, характеризующих
макро состояния (микросостояния – это
состояния молекул). Большей вероятности
и большему статистическому весу
соответствует больший хаос (беспорядок)
в системе.

Энтропия – это мера хаотичности и необратимости процесса.
24. Второе и третье начало термодинамики.
Второе начало термодинамики.
Клиузис утверждал: «Невозможен процесс, единственным результатом которого бы был переход тепла от менее нагретого тела к более нагретому».
Кельвин утверждал: «Невозможен был бы процесс, единственным результатом которого было бы превращение теплоты в работу».
Третье начало термодинамики (теорема Нернста).
При приближении температуры системы к абсолютному нулю энтропия системы стремится к нулю.


25. Понятие о тепловых машинах.
Тепловая машина (Т. м.) – это устройство для получения полезной работы за счёт теплоты, выделяющейся при горении топлива.
Любой тепловой двигатель, независимо от его конструкции, имеет следующие составляющие:
нагреватель (топливо);
рабочее тело (газ);
холодильник (атмосфера).
КПД тепловой машины.

Цикл Карно. Теоремы Карно.
Цикл Карно – это равновесный обратимый процесс, состоящий из двух изотерм и двух адиабат.
Теоремы Карно.
КПД любой тепловой машины, работающей по циклу Карно, не зависит от устройства машины и рабочего тела, определяется температурой холодильника и температурой нагревателя.
КПД любой тепловой машины, работающей по необратимому циклу меньше КПД цикла Карно (устройство одного и другого двигателей должно быть одинаковым).
Цикл Карно. Теорема Карно.
P V 0 1 2 3 4





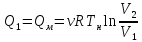
2 – 3 (изобарный процесс):

4 – 1 (адиабатный процесс):