
КХ часть 4
.pdf
Полная энергия взаимодействия между частицами получается путем сложения энергии притяжения в результате действия молекулярных сил и отталкивания в результате действия электрических сил.
U Uýë Uìîë |
K e H |
A r |
(12.8) |
|
12 H |
||||
|
|
|
Результирующая потенциальная кривая взаимодействия частиц показана на рис.12.9.
Рис. 12.9 Результирующая кривая изменения энергии взаимодействия частиц в зависимости от расстояния между ними. 1-энергия отталкивания, 2-энергия притяжения, 3-полная энергия.
При H 0 Uотт. К , Uïðèò . .
На результирующей потенциальной кривой имеется три области.
В области малых H порядка 1 нм преобладают силы притяжения, так как при H 0 Uотт. К , Uприт. . Это выражается в
существовании на результирующей кривой первичного минимума,
или ближней потенциальной ямы. Существование
определяет необратимую агрегацию частиц. В области средних расстояний H 100 нм, равных толщине ионной оболочки,
50
В объеме раствора существует электрическое поле, каждая точка которого характеризуется величиной x . Энергия притяжения
граммиона к поверхности U определяется величиной потенциала и равна:
U z e NA x z F x (11.6)
где |
x |
– |
потенциал |
на расстоянии |
x |
от |
поверхности. |
|||
Концентрация |
противоионов |
в |
точке |
x в соответствии с законом |
||||||
|
|
|
Cx C e |
z F x |
|
|
C |
|
|
|
Больцмана |
равна |
R T , |
где |
- |
концентрация |
|||||
противоионов на бесконечно большом удалении от поверхности. При
x x 0 Cx C .
Рис. 11.5. Изменение концентрации ионов в зависимости от расстояния от
поверхности.
Значение потенциала уменьшается по мере удаления от
поверхности, |
то |
есть |
значение |
обратно пропорционально |
расстоянию |
x, |
так |
как происходит |
компенсация потенциала |
|
|
|
11 |
|
www.mitht.ru/e-library
противоионами. В случае, когда потенциал поверхности 0 25 мВ и
0 F z R T , |
уменьшение |
потенциала происходит |
по |
|||
экспоненциальному закону: |
|
|
|
|
||
|
|
x |
0 |
e x (11.7) |
|
|
Найдем математическое и физический смысл коэффициента . |
||||||
При x 1/ |
x 0 /e |
(рис. 11.6). |
Следовательно, 1/ - |
|||
толщина слоя, |
при |
которой |
значение 0 |
убывает в e раз. |
Эту |
|
величину называют эффективной толщиной ДЭС. Величина 1/
равна расстоянию между обкладками плоского конденсатора, одной из которых является поверхность, а другая электрически эквивалентна диффузной части ДЭС. В теории сильных электролитов Дебая-Гюккеля называют радиусом экранирования.
Величина связана с характеристиками растворителя и электролитов, имеющихся в системе, следующим образом:
|
1 |
|
k T |
|
|
|
k |
T |
(11.8) |
||
|
|
|
|
|
|
|
|
||||
|
c z |
2 |
I |
||||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||
где I – ионная сила раствора; – диэлектрическая постоянная растворителя.
12
давления. Если стабилизатором является электролит, и имеется двойной электрический слой, то действует электростатический фактор устойчивости. Отталкивание между частицами нельзя рассматривать как отталкивание между одноименно заряженными точечными зарядами, и силы отталкивания нельзя рассчитать по закону Кулона
f |
q1 q2 |
. Силы отталкивания |
возникают |
за счет перекрывания |
|
ε r2 |
|||||
|
|
|
|
||
двойных электрических слоев, |
и когда |
происходит нарушение |
|||
симметрии распределения ионов при H 1 .
χ
Б.В.Дерягин установил экспоненциальный закон изменения электрических сил, определяющих отталкивание частиц, с
расстоянием
Uэл R e χ H |
(12.7) |
где - величина обратная толщине ДЭС.
В отличие от энергии притяжения при H 0, Uотт. К .
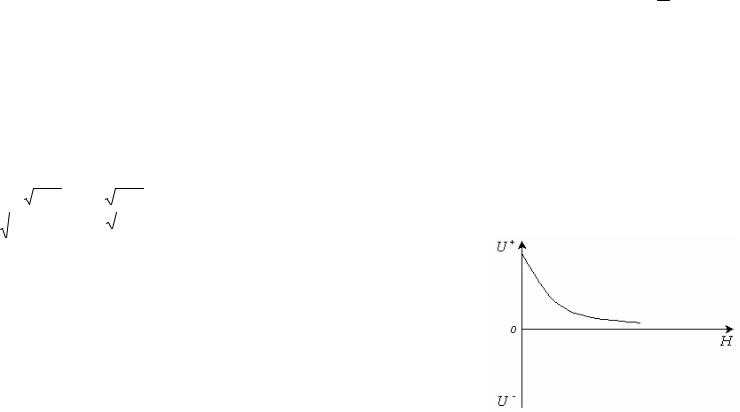
Зависимость энергии отталкивания от расстояния между частицами изображена на рис. 12.8.
Рис. 12.8 Зависимость энергии отталкивания от расстояния между частицами.
49
www.mitht.ru/e-library

1015 c 1 и расстояних порядка 100 нм волны, излучаемые разными атомами, имеют разность фаз, близкую к , что приводит к ослаблению взаимодействия, и выражение для энергии притяжения имеет вид:
Uприт |
K |
A |
|
(12.6) |
|
H3 |
|||||
|
|
|
|||
Следует отметить, что при H 0 |
энергия притяжения частиц |
||||
Uприт . При рассмотрении сил, действующих между частицами,
силы притяжения обычно принимают отрицательными, силы отталкивания – положительными. Поэтому изменение энергии притяжения в зависимости от расстояния между частицами изображается так, как это показано на рис. 12.7.
Рис. 12.7. Изменение энергии притяжения в зависимости от расстояния между
частицами.
Силы отталкивания
Долговечность лиофобных систем говорит о существовании сил отталкивания между частицами. Силы отталкивания, действующие между частицами, приводят к повышению устойчивости коллоидных систем, являются факторами устойчивости. Они имеют различную природу и соответствуют различным компонентам расклинивающего
48
Рис. 11.6. Эффективная толщина двойного электрического слоя.
11.4.2 Внутренняя часть ДЭС
Эта часть представляет плотный слой ионов, расположенный в непосредственной близости от поверхности. Вблизи поверхности поведение ионов определяется тремя факторами, обуславливающими строение ДЭС: межмолекулярными адсорбционными взаимодействиями, электростатическими взаимодействиями ионов с поверхностью и друг с другом и тепловым движением ионов.
Электростатические (кулоновские) взаимодействия ионов являются более дальнодействующими, чем Ван-дер-Вальсовы взаимодействия молекул.
Поскольку ион имеет конечные размеры, то центр иона может приблизиться к поверхности только в пределах радиуса гидратированного иона, не подвергаясь специфической адсорбции,
обусловленной действием межмолекулярных сил. Штерн предложил модель, в которой ДЭС состоит из двух частей, разделенных плоскостью, расположенной на расстоянии от поверхности равном радиусу гидратированного противоиона. Эту плоскость называют
плоскостью наибольшего приближения ионов.
13
www.mitht.ru/e-library

Штерн рассмотрел также возможность специфической ионной
адсорбции, обусловленной адсорбционными взаимодействиями
некулоновской природы.
Рис. 11.7. Строение ДЭС по Штерну и изменение потенциала поверхности с
изменением расстояния от поверхности.
Таким образом, к модели Гуи-Чепмена, Штерн предложил две поправки: учитывать реальные размеры ионов и адсорбционный потенциал Ф, который имеет некулоновскую природу и приводит к образованию специфически адсорбированных ионов, то есть ионов,
14
друг от друга на расстоянии H , составляющем величину от 10 до 20
нм и при условии H r лондоновская энергия притяжения
Uприт A r , где величина A является константой молекулярного
12H
взаимодействия и называется константой Гамакера. Она учитывает природу взаимодействующих тел и выражается в единицах измерения энергии. Значение константы Гамакера в вакууме обычно составляет
10 12 эрг (10 19 Дж ). Константа Гамакера зависит от числа атомов в единице объема и поляризуемости молекул. Значение этой константы складывается из отдельных констант, характеризующих адгезионное и когезионное взаимодействие.
В жидкости значение энергии притяжения меньше, чем в вакууме. Значение эффективной константы Гамакера определяется
выражением A (
 A2
A2 
 A1 )2 , где индексы 1 и 2 относятся к среде и частице. Когда частица и среда химически подобны, энергия притяжения мала, т. к. значения A1 и A2 близки, и A мала.
A1 )2 , где индексы 1 и 2 относятся к среде и частице. Когда частица и среда химически подобны, энергия притяжения мала, т. к. значения A1 и A2 близки, и A мала.
Силы притяжения не зависят от перемены мест фазы и среды.
Два воздушных пузырька в воде так же сильно притягиваются друг к другу, как две капли воды того же размера в воздухе.
Для двух параллельных полубесконечных пластин энергия притяжения равна:
Uприт |
1 |
|
A |
(12.5) |
|
2 H 2 |
|||
|
12 π |
|
||
где H - расстояние между пластинами. Уравнение (12.5)
применимо для расстояний не больше 100 нм. При больших расстояниях на дисперсионное взаимодействие влияет эффект электромагнитного запаздывания. При частотах 1 и 2 , близких к
47
www.mitht.ru/e-library
Дисперсионные силы между частицами действуют на большем
расстоянии, чем между молекулами, т. е. являются
дальнодействующими. Причиной дальнодействия дисперсионных сил между частицами является их аддитивность. Для частицы,
представляющей собой ансамбль атомов и молекул, дисперсионные силы, действующие между многими атомами, складываются. Энергия притяжения между частицами может быть подсчитана как сумма взаимодействий молекул, входящих в разные частицы. Благодаря аддитивности лондоновских сил энергия взаимодействия между частицами гораздо медленнее убывает с расстоянием, чем энергия
взаимодействия между молекулами.
Соответствующая теория связана с эффектом
электромагнитного запаздывания, который основан на том, что флуктуирующие электромагнитные поля атомов распространяются со
скоростью света в рассматриваемой среде. При частоте 1015 c 1 за один период свет проходит расстояние около 100 нм. Если расстояние между атомами превышает 100 нм, то происходит
изменение фазы колебания прежде, чем электромагнитная волна дойдет от одного атома до следующего. Электромагнитные волны,
исходящие от атомов, разделенных расстоянием более 100 нм, не совпадают по фазе, имеют разность фаз, близкую к , что приводит к
ослаблению взаимодействия. Это явление называется
электромагнитным запаздыванием. Соответствующая теория
приводит к выводу, что энергия взаимодействия между частицами
является степенной функцией расстояния и изменяется обратно пропорционально некоторой степени расстояния между частицами
( H ). Показатель степени зависит от формы поверхности и от расстояния между ними. Для двух сфер радиусом r , находящихся
46
которые присоединяются к поверхности электростатическими и Ван-
дер-Ваальсовыми силами в достаточной степени, чтобы преодолеть тепловое движение. Они могут быть гидратированы, по меньшей мере со стороны поверхности. Центры любого специфически адсорбированного иона расположены между поверхностью и плоскостью наибольшего приближения ионов, в так называемом слое Штерна. Ионы с центрами, расположенными за плоскостью наибольшего приближения ионов, образуют диффузную часть ДЭС,
подчиняющуюся теории Гуи-Чемпена. Строение ДЭС по Штерну и изменение потенциала с изменением расстояния от поверхности показаны на рис. 11.7.
Потенциал изменяется от 0 (потенциал поверхности) до
(потенциал Штерна) в слое Штерна и уменьшается от до нуля в диффузном слое. Энергия притяжения граммиона в адсорбционный слой Uприт. равна:
Uприт. z F Ф (11.9)
Поэтому в адсорбционном слое скапливается много ионов, и
падение потенциала в слое Штерна резкое. В диффузном слое падение потенциала происходит медленнее и по экспоненциальному закону.
Значение потенциала является определенной, но неизмеримой величиной, так как электрод нельзя поместить в плоскость наибольшего приближения ионов, т.е. в центр иона.
15
www.mitht.ru/e-library

11.5. Электрокинетические явления.
Вторым основным вопросом этого раздела является теория
электрокинетического потенциала, или - потенциала. Для его понимания необходимо рассмотреть электрокинетические явления.
В электрокинетических явлениях устанавливается взаимосвязь между электрическим полем и движением фаз (твердой и жидкой)
относительно друг друга. При наложении внешнего электрического поля возникает движение фаз относительно друг друга. И наоборот,
при перемещении фаз возникает разность потенциалов. Переход от движения жидкости к движению взвешенных частиц определяется соотношением объемов фаз и наличием жесткой структуры системы.
Рис. 11.8. Схема электрофореза ( а) и электроосмоса ( б).
Перемещение частиц во внешнем электрическом поле называется электрофорезом. Схема электрофореза, впервые обнаруженного профессором Московского университета Ф.Ф. Рейссом в 1808 г. изображено на рис. 11.8, а. В мокрую глину помещаются две заполненные водой стеклянные трубки, в которых расположены электроды, и прикладывается внешнее электрическое поле. В анодном
16
К третьему типу сил межмолекулярного взаимодействия относятся дисперсионные, или лондоновские силы. Они возникают вследствие того, что нейтральные атомы представляют системы колеблющихся зарядов вследствие наличия положительного заряженного ядра и отрицательно заряженных электронов. Причиной дисперсионных сил является квантово-механический эффект,
связанный с флуктуациями электрических полей атомов и молекул.
Эти флуктуации происходят на ультрафиолетовых частотах и приводят к возникновению переменного диполя, способного наводить диполи в других молекулах. Дисперсионное взаимодействие синхронно с несколькими молекулами без взаимной конкуренции, в
отличие от ориентационных и индукционных сил, при действии которых наблюдается конкуренция между разными диполями. Если два диполя расположены оптимально друг к другу, то они не могут быть расположены оптимально по отношению к третьему диполю.
Дисперсионные силы являются наиболее универсальными силами, определяющими энергию притяжения. Для молекул они также убывают пропорционально шестой степени расстояния между атомами. Энергия ориентационного, индукционного и дисперсионного взаимодействия зависит от дипольного момента молекул ,
поляризуемости атомов или молекул , 2 , характеристических
энергий |
h , |
h 2 |
и |
расстояний |
между |
молекулами |
H |
и |
|||||||||||
определяется выражениями: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Uор |
|
|
μ4 |
; U |
инд α |
μ2 |
; Uдисп |
3 |
|
α α |
2 |
|
|
1 |
|
||||
|
|
|
|
1 |
|
|
|
|
|
||||||||||
K T 2 H6 |
H6 |
2 |
1 |
|
|
|
1 |
|
H6 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
h ν1 |
h ν2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(12.4) |
|||
|
|
|
|
|
45 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
www.mitht.ru/e-library
в действие силы между разнородными молекулами или частицами.
Если последние много больше первых, то это благоприятствует диспергированию, если меньше, то наоборот, диспергирование затрудняется, протекает коагуляция. Таким образом, устойчивость дисперсий определяется природой сил, действующих между частицами.
При кинетическом рассмотрении устойчивости принимается во внимание баланс сил притяжения и отталкивания между частицами.
Процесс слипания определяется преобладанием сил притяжения над силами отталкивания. При этом частицы теряют свою индивидуальность, и вначале образуются агрегаты частиц, а затем макрофаза.
12.3.2. Природа сил, действующих между частицами.
Силы притяжения.
Силы притяжения между частицами по своей природе являются силами Ван-дер-ваальса. Известно, что силы Ван-дер-Ваальса имеют тройственную природу. Если молекулы являются электростатическими диполями, то между разноименно заряженными концами действуют электростатические (кулоновские) силы притяжения, называемые
ориентационными. Энергия ориентационного притяжения убывает обратно пропорционально шестой степени расстояния между диполями.
Если неполярную молекулу поместить в электрическое поле,
образованное полярной молекулой, то в неполярной молекуле наводится (индуцируется) дипольный момент. Молекулы начинают взаимодействовать друг с другом. Эта энергия называется энергией
индукционного взаимодействия.
44
пространстве появляется взвесь частиц, движущихся к аноду. Это указывает на то, что частицы глины заряжены отрицательно.
Если в электрическом поле движутся малые ионы, то это явление называется ионной проводимостью, а если крупные частицы или макромолекулы белка – то электрофорезом.
При электроосмосе (рис. 11.8, б) U – образная трубка заполняется песком, над которым находится слой воды и прикладывается разность потенциалов. Перемещение жидкости вызывается движением ионов диффузного слоя, которые увлекают всю массу жидкости, заполняющую капилляры воды и поры.
Разность уровней жидкости в катодном и анодном пространстве,
называемая электроосмотическим поднятием, может быть очень велика. При 100В значение электроосмотического поднятия достигает
20 см.
При течении жидкости через пористое тело под действием разности давлений возникает явление, называемое потенциалом течения (рис. 11.9, а). Это явление было обнаружено Квинке в 1859 г.
Причина его состоит в том, что движущаяся дисперсионная среда увлекает за собой противоионы, что вызывает образование
поверхностного электрического тока (ток течения). На концах капиляров возникает разность потенциалов, которая вызывает встречный объемный ток ионов противоположного знака. При установлении потока ионов выравнивается и устанавливается постоянная разность потенциалов, равная потенциалу течения.
Потенциал течения - это явление, обратное электроосмосу.
17
www.mitht.ru/e-library

Рис. 11.9. Схема потенциала течения ( а) и потенциала седиментации ( б).
Явление, обратное электрофорезу и называемое потенциалом седиментации, было обнаружено Дорном в 1878 г. При седиментации суспензии кварца в центробежном поле он обнаружил возникновение разности потенциалов. Седиментация может происходить под действием как силы тяжести, так и центробежного поля (рис. 11.9, б).
При осаждении ионы диффузного слоя вследствие трения отстают от движущейся частицы, что приводит к образованию потока заряженных частиц, и возникновению электрического тока. С помощью электродов,
установленных на различной высоте, можно измерить разность потенциалов, т.е. потенциал седиментации. Возникновение потенциала седиментации при оседании частиц, приводит к образованию грозовых разрядов в атмосфере.
Электрокинетические явления группируются попарно либо по признаку причинности, либо по признаку объекта.
Потенциал течения по характеру причинно-следственной связи является явлением, обратным электроосмосу, а потенциал седиментации – электрофорезу. Схема классификации электрокинетических явлений приведена на рис. 11.11.
18
поверхностной энергии за счет увеличения поверхности, то
происходит самопроизвольное диспергирование.
12.3. Теория агрегативной устойчивости и коагуляции
лиофобных дисперсных систем (теория ДЛФО)
Втеории устойчивости лиофобных дисперсных систем,
разработанной Дерягиным, Ландау, Фервеем и Овербеком и называемой теорией ДЛФО, рассматривается действие электрических и молекулярных сил. Другие факторы устойчивости не поддаются количественному рассмотрению и не учитываются в теории ДЛФО. В теории ДЛФО гидрофобные коллоиды рассматриваются как термодинамически неустойчивые системы. Их временная агрегативная устойчивость определяется присутствием энергетического или силового барьера при сближении частиц, и имеет чисто кинетический характер. Тепловое движение молекул среды, вызывающее броуновское движение частиц, является дестабилизирующим фактором, перемещая частицы в зону действия Ван-дер-Вальсовых сил притяжения.
12.3.1. Кинетический подход к устойчивости дисперсных
систем
Проблема образования устойчивых коллоидных систем имеет общность с проблемой растворения в классической химии. Два газа всегда образуют газовый раствор, т. к. газы неограниченно смешиваются вследствие слабых межмолекулярных сил. В
конденсированных фазах между молекулами действуют значительные силы, препятствующие испарению. При растворении или диспергировании силы между одинаковыми молекулами или частицами как фазы так и среды должны быть преодолены, и вступают
43
www.mitht.ru/e-library

Рис. 12.6. Изменение потенциала поверхности между пластинами при
отсутствии перекрывания ( а) и при перекрывании ( б) ДЭС.
При уменьшении расстояния между частицами и перекрывании ДЭС потенциал между частицами нигде не достигает нулевого значения (рис. 12.6.б). Наличие в прослойке потенциала того же знака, что и на поверхности, приводит к отталкиванию частиц.
Адсорбционная компонента расклинивающего давления
связана с неравномерным распределением растворенного вещества в прослойке, т. е. изменением состава поверхностного слоя по сравнению с объемом.
Стерическая компонента возникает в результате перекрывания адсорбционных слоев ПАВ с длинными углеводородными радикалами и полимеров. Это связано с тем, что в тонких прослойках число конформаций гибких радикалов меньше, чем при большом расстоянии между частицами, и энтропия системы также меньше. Поэтому за счет энтропийного фактора частицы отталкиваются и сохраняют свою индивидуальность. Следует иметь в виду, что энтропийный фактор устойчивости коллоидных систем имеет и другое проявление: при дроблении энтропия системы увеличивается и ее устойчивость повышается. Если увеличение энтропии перекрывает увеличение
42
Рис. 11.10. Схема классификации электрокинетических явлений.
11.6. Электрокинетический потенциал.
По скорости электрокинетических явлений можно определить потенциал на поверхности сдвига между заряженной поверхностью и раствором электролита. Этот потенциал оказался меньше, чем потенциал, определенный из электрохимических явлений и называется электрокинетическим, или -потенциалом, который служит мерой интенсивности электрокинетических явлений. Опыт показывает, что 0 и зависит от введения в раствор любых
электролитов, тогда как на 0 влияют только электролиты,
содержащие потенциалопределяющие ионы.
При перемещении фаз разрыв ДЭС происходит не по границе раздела фаз, а по поверхности скольжения, расположенной в диффузном слое. Точнее говоря, поверхность скольжения является областью с быстро изменяющейся вязкостью, и ее точное расположение неизвестно. Кроме ионов, расположенных в слое Штерна, с заряженной поверхностью связано некоторое количество растворителя, входящего в состав электрокинетической единицы.
19
www.mitht.ru/e-library

Поэтому поверхность скольжения расположена дальше от поверхности, чем плоскость Штерна, там, где вязкость уменьшается до значения, равного среднему значению вязкости в объеме, и величина .
Для лиофобных поверхностей значения и близки.
Различие между и велико при высоких значениях потенциала и при высоких концентрациях электролита. ДЭС, характеризуемый параметрами и , определяет устойчивость коллоидной системы.
Чем шире ДЭС, тем меньше притяжение частиц, и тем устойчивее система. Адсорбция неионных ПАВ приводит к удалению поверхности скольжения от плоскости Штерна и существенному снижению .
Уравнение Гельмгольца-Смолуховского позволяет установить связь между скоростью электрокинетических явлений V и величиной
-потенциала V f ( ). Уравнение выводится на примере электроосмоса. В основе вывода уравнения лежат следующие предпосылки: ДЭС можно рассматривать как плоский конденсатор,
одной обкладкой которого является заряженная поверхность и противоионы до плоскости скольжения, а второй - противоионы диффузного слоя, которые расположены на одинаковом расстоянии от поверхности. Толщина ДЭС много меньше размера частицы, то есть
1/ a. Твердая поверхность, на которой образован ДЭС, является диэлектриком, а раствор проводит ток. Движение жидкой фазы относительно твердой поверхности ламинарно. Схема конденсатора показана на рис. 11.11.
Приложим к конденсатору внешнее электрическое поле,
потенциал которого равен E . Если расстояние между электродами
20
Если нет перекрывания двойных электрических слоев частиц, то нет отталкивания между ними (рис. 12.5 а). Силы отталкивания возникают только при перекрывании ионной атмосферы коллоидных частиц, т. е. диффузных слоев противоионов. (рис. 12.5. б)
Рис. 12.5. Перекрывание двойных электрических слоев.
При этом в зоне перекрывания происходит перераспределение ионов с изменением их концентрации, вследствие чего появляются дополнительные электростатические силы отталкивания.
Пока ДЭС не перекрываются (рис. 12.6. а), потенциал в середине слоя между пластинами равен нулю.
41
www.mitht.ru/e-library
