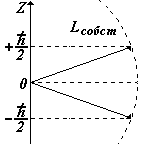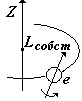- •Квантовая физика.
- •Распределение энергии в спектре ачт.
- •Гипотеза и формула Планка.
- •2) Для элементарных процессов взаимодействия частиц применимы законы сохранения импульса и энергии.
- •Ядерная модель атома.
- •Постулаты Бора:
- •Атом водорода и водородоподобные атомы (впа) по теории Бора.
- •Корпускулярно-волновой дуализм материи. Гипотеза и формула де Бройля.
- •Принцип неопределенности Гейзенберга.
- •1). Входит ли электрон в состав атомного ядра?
- •Уравнение Шрёдингера.
- •Гармонический осциллятор.
- •Частица в одномерной потенциальной яме (ящике)
- •Электрон в атоме водорода в основном состоянии.
- •Описывается с помощью 4-х квантовых чисел: n, l, m, ms.
- •Принцип Паули. Периодическая система элементов.
- •Элементы квантовой статистики и физики твердого тела.
- •Сверхтекучесть.
- •Сверхпроводимость.
- •Температурная зависимость сопротивления различных веществ.
- •Собственные полупроводники.
- •Контакт р - и n - полупроводников.
- •105 - 104 См, для металлов порядка 108 см.
Описывается с помощью 4-х квантовых чисел: n, l, m, ms.
|
1) n = 1, 2, 3, … , главное квантовое число |
входит в выражение для энергии электрона xvi Для основного состояния атома Н (n = 1) – см. ранее. |
|
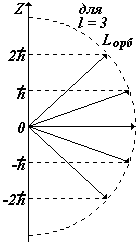
2) l = 0, 1, 2, … , (n 1) орбитальное квантовое число, Входит в выражения для орбитальных механического Lорб и магнитного pорб моментов электрона в атоме. Показывает, что орбитальные моменты квантуются, т.е. могут принимать только дискретные значения. |
|
|
|
О Как векторы они направлены противоположно |
|
механический орбитальный момент (момент импульса) |
|
|
|
|
|
магнитный орбитальный момент me – масса электрона |
|
|
|
магнетон Бора; (магнитные моменты принято выражать в магнетонах Бора) |
|
3) m = l, … , 1, 0, +1, … , +l магнитное квантовое число Входит в выражение для проекций орбитальных моментов на направление Z внешнего поля (например, магнитного). Показывает,
что плоскость, в которой движется
электрон во внешнем поле ориентируется
только определенным образом, так чтобы
проекция момента была кратна
|
|
|
|
|
|
|
|
|
|
|
|
4)
Входит в выражение для проекций собственного механического Lсобст и магнитного рсобст моментов на направление Z внешнего поля (например, магнитного). Показывает, что ориентация Lсобст (спина –см. дальше) может иметь только два значения. |
||
|
|
|
|
|
|
отношение собственных магнитного и механического моментов |
|
|
Спин
(от англ. spin
- веретено). Спином называется собственный
механический момент (момент импульса)
электрона
|
|
||
|
|
Спин собственный механический момент (момент импульса) электрона – имеет только одно значение. Спин связан со спиновым квантовым числом s, имеющим также только одно значение ½. |
||
|
|
спиновое квантовое число |
||
|
В
квантовой механике различают частицы
с «целым»
спином
(бозоны) и «полуцелым»
спином
(фермионы, например, электрон, см.
дальше).Это условная терминология. Из
формулы для спина видно, что он не
может быть целым числом. В этих словах
подразумевается, что проекция спина
либо кратна
|
|||
Таким образом,
из квантовой механики следует, что
энергия электрона, его орбитальные
моменты, проекции орбитальных моментов
на внешнее поле
квантуются. Они не могут иметь любые
значения, а только те, которые определяются
приведенными выше соотношениями.
Собственный момент электрона имеет
только одно значение, а его проекция на
внешнее поле – два значения
![]() /
2. Часто условно говорят «спин вверх»,
«спин вниз».
/
2. Часто условно говорят «спин вверх»,
«спин вниз».
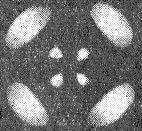 Чтобы представить
сложность поведения электрона даже в
простейшем атоме Н, на рисунке представлена
плотность вероятности для электрона в
состоянии с n
= 4, l
= 2, m
=
1. Светлые пятна - это области, в которых
наиболее вероятно пребывание электрона.
Это только плоский срез, в действительности
вероятность имеет объемное распределение.
Чтобы представить
сложность поведения электрона даже в
простейшем атоме Н, на рисунке представлена
плотность вероятности для электрона в
состоянии с n
= 4, l
= 2, m
=
1. Светлые пятна - это области, в которых
наиболее вероятно пребывание электрона.
Это только плоский срез, в действительности
вероятность имеет объемное распределение.

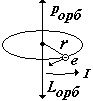 тношение
орбитальных
магнитного и механического моментов
тношение
орбитальных
магнитного и механического моментов